Lipidai 200401
CHEMIJA IR LIPIDŲ MEDŽIAGA.
LIPIDAI – tai gyviems organizmams būdingos organinės medžiagos, netirpios vandenyje, bet tirpios organiniuose tirpikliuose ir viena kitai.
Lipidų grupės skiriasi hidrofobiškumo laipsniu. Fosfolipidai ir glikolipidai yra poliniai lipidai.
Cholesterolis užima tarpinę padėtį tarp polinių ir absoliučiai hidrofobinių lipidų.
Trigliceridai ir cholesterolio esteriai yra visiškai hidrofobiniai.
Daugumoje lipidų (išskyrus sterolius ir kai kuriuos nedidelius lipidus) yra daugiau riebalų rūgštis(VZHK).
Membranose yra tik FOSFOLIPIDAI (PL), GLIKOLIPIDAI (GL) ir CHOLESTEROLIS (CS).
ŽMOGAUS KŪNUI BŪDINGOS RIEBALŲ RŪGŠTYS
Rūgštis vadinama riebaline, jei jos molekulėje yra daugiau nei keturi anglies atomai. Vyrauja ilgos grandinės riebalų rūgštys (anglies atomų skaičius yra 16 ir daugiau Anglies atomų ir dvigubų jungčių skaičius rodomas dvigubu indeksu). Pavyzdžiui: C18:1 (9-10). Šiuo atveju 18 yra anglies atomų skaičius, o 1 yra dvigubų jungčių skaičius. Dvigubų jungčių vieta (pagal anglies atomų skaičių) nurodyta skliausteliuose.
Mokiniai turėtų žinoti anglies atomų ir dvigubų jungčių skaičių šiose riebalų rūgščių molekulėse:
C16:0 – palmitinė,
C18:0 – stearinas,
C18:1 – oleinas (9:10),
C18:2 – linolo (9-10,12-13),
C18:3 – linolenas (9-10, 12-13, 15-16),
C20:4 - arachidoninis (5-6, 8-9, 12-13, 15-16).
Riebalų rūgštys, turinčios dvigubą ryšį 3 padėtyje, turi labai ryškų antiaterosklerozinį poveikį (linoleno rūgštis). Ypač daug 3 turinčių riebalų rūgščių yra žuvų taukuose ir kitose jūros gėrybėse. Tokios riebalų rūgštys žmogaus organizme nesintetinamos.
Riebalų rūgštys, sudarančios žmogaus organizmą, turi bendrų bruožų pastatai:
Lyginis anglies atomų skaičius.
Linijinė (nešakota) anglies grandinė.
Polinesočiosios riebalų rūgštys turi TIK IŠSKYRIUSIUS dvigubus ryšius (tarp gretimų dvigubų jungčių yra mažiausiai dvi viengubos jungtys).
Dvigubos jungtys turi tik cis konfigūraciją.
Remiantis dvigubų jungčių skaičiumi, riebalų rūgštys gali būti skirstomos į SOČIAS (nėra dvigubų jungčių), mononesočiąsias (viena dviguba jungtis) ir POLESOčiąsias (dvi ar daugiau dvigubų jungčių).
Laisvųjų riebalų rūgščių yra labai mažais kiekiais. Daugiausia jų yra kituose lipiduose. Be to, jie yra sujungti su kitais lipidų komponentais esteriu (esterifikuotu).
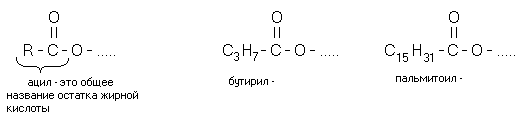
LIPIDŲ EGYVIMO FORMOS ŽMOGAUS KŪNE
Riebaliniai intarpai, kurių daugiausiai yra adipocituose. Tai yra trigliceridų egzistavimo forma.
Biomembranos. Juose nėra trigliceridų, tačiau yra fosfolipidų, glikolipidų ir cholesterolio.
Lipoproteinai. Gali būti visų klasių lipidų.
Lipoproteinai
Lipoproteinai yra sferinės dalelės, kuriose galima išskirti hidrofobinę šerdį, susidedančią iš trigliceridų (TRG) ir cholesterolio esterių (ECS) bei amfifilinio apvalkalo, kuriame yra fosfolipidų, glikolipidų ir baltymų.
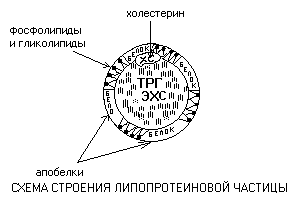
Lukšto baltymai vadinami apoproteinais. Cholesterolis (CS) paprastai užima tarpinę padėtį tarp apvalkalo ir šerdies. Dalelės komponentai yra sujungti silpnų tipų ryšiais ir yra nuolatinės difuzijos būsenoje – gali judėti vienas kito atžvilgiu.
Pagrindinis lipoproteinų vaidmuo yra lipidų pernešimas, todėl jų galima rasti biologiniuose skysčiuose.
Tiriant kraujo plazmos lipidus paaiškėjo, kad juos galima suskirstyti į grupes, nes skiriasi vienas nuo kito komponentų santykiu. Skirtingi lipoproteinai turi skirtingą lipidų ir baltymų santykį dalelių sudėtyje, todėl skiriasi ir tankis.
Lipoproteinai yra atskiriami pagal tankį ultracentrifuguojant, jie nenusėda, o plūduriuoja (plūduriuoja). Flotacijos matas yra plūduriavimo konstanta,žymimas S f (Svedberg flotacija). Pagal šį rodiklį išskiriamos šios lipoproteinų grupės:

Lipoproteinai taip pat gali būti atskirti elektroforezės būdu. Atliekant klasikinę šarminę elektroforezę, skirtingi lipoproteinai elgiasi skirtingai. Kai lipoproteinai patenka į elektrinį lauką, chilomikronai lieka pradžioje. VLDL ir DILI galima rasti pre-β-globulinų frakcijoje, MTL - β-globulino frakcijoje, o DTL - β-globulinų frakcijoje:
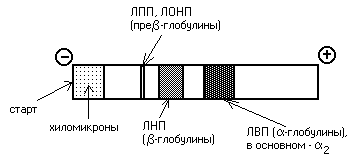
Kraujo plazmos lipoproteinų spektro nustatymas medicinoje naudojamas aterosklerozei diagnozuoti.
Visi šie lipoproteinai skiriasi savo funkcija.
1. Chilomikronai (HM)- susidaro žarnyno ląstelėse, jų funkcija yra: egzogeninių riebalų perkėlimas iš žarnyno į audinius (daugiausia riebalinį audinį), taip pat egzogeninio cholesterolio pernešimas iš žarnyno į kepenis.
2. Labai mažo tankio lipoproteinai (VLDL)- susidaro kepenyse, jų vaidmuo: endogeninių riebalų, sintezuojamų kepenyse iš angliavandenių, transportavimas į riebalinį audinį.
3. Mažo tankio lipoproteinai (MTL)- susidaro kraujyje nuo VLDL iki vidutinio tankio lipoproteinų (IDL) susidarymo stadijos. Jų vaidmuo: endogeninio cholesterolio pernešimas į audinius.
4. Didelio tankio lipoproteinai (DTL)- susidaro kepenyse, pagrindinis vaidmuo yra cholesterolio transportavimas iš audinių į kepenis, tai yra cholesterolio pašalinimas iš audinių, o tada cholesterolis išsiskiria su tulžimi.
Nustatant skirtingo tankio lipoproteinų kiekį kraujyje, jie dažniausiai atskiriami elektroforezės būdu. Šiuo atveju CM lieka pradžioje, VLDL patenka į pre--globulino frakciją, MTL ir LPP randami -globulino frakcijoje, o DTL - 2-globulinai. Jei kraujyje padidėja β-globulinų (MTL) kiekis, tai reiškia, kad cholesterolis nusėda audiniuose (vystosi aterosklerozė).
APO BALTYMŲ VAIDMUO LIPOPRETINŲ SUDĖTIJE
Ypač svarbūs lipoproteinų baltyminiai komponentai. Jie vadinami " apolipoproteinai“ ir žymimi lotyniškomis raidėmis (apoA, apoB, apoC ir tt iki apoG).
APO BALTYMŲ FUNKCIJOS.
1. Apoproteinai veikia kaip emulsikliai, nes yra amfifilinės medžiagos.
2. Dalis apolipoproteinų yra lipidų apykaitos fermentų aktyvumo reguliatoriai.
3. Gali turėti savo fermentinį aktyvumą.
Jie gali veikti kaip lipoproteinų ląstelių receptorių ligandai.
Daugelis apoproteinų perneša lipidus iš vieno lipoproteino į kitą.
RIEBALŲ METODIKA (TRIAGLICEROLIS)
Cheminis riebalų pavadinimas yra acilgliceroliai, tai yra riebalai. Tai glicerolio ir aukštesnių riebalų rūgščių esteriai. „Acil-“ reiškia „riebalų rūgšties likutį“ (nepainioti su „acetil-“ – acto rūgšties likučiu). Priklausomai nuo acilo radikalų skaičiaus, riebalai skirstomi į mono-, di- ir trigliceridus. Jei molekulėje yra 2 riebalų rūgščių radikalai, tai riebalai vadinami DIACYLGLYCEROL. Jei molekulėje yra 1 riebalų rūgšties radikalas, tada riebalai vadinami MONOACYLGLYCEROL.
Žmogaus ir gyvūnų organizme vyrauja TRIacilGLICEROLIAI (sudėtyje yra trys riebalų rūgščių radikalai).
Riebalų savybes lemia riebalų rūgščių sudėtis.
Riebalų funkcijos:
1. ENERGIJA.
Skirtingai nuo angliavandenių, riebalai sudaro organizmo energijos rezervą. Riebalų, kaip energijos rezervo, pranašumas yra tas, kad riebalai yra labiau redukuotos medžiagos, palyginti su angliavandeniais (angliavandenių molekulės turi deguonies prie kiekvieno anglies atomo - „–CHOH-“ grupės; riebalai turi ilgus angliavandenilių radikalus, kuriuose vyrauja „“ grupės). CH 2 -“ - jie neturi deguonies). Iš riebalų galima pašalinti daugiau vandenilio, kuris vėliau pereina per mitochondrijų oksidacijos grandinę ir gamina ATP.
Angliavandenių ir baltymų kalorijų kiekis: ~ 4 kcal/gram.
Riebalų kaloringumas: ~ 9 kcal/gram.
Riebalų, kaip energijos rezervo, privalumas, skirtingai nei angliavandenių, yra jų hidrofobiškumas – jie nesusiję su vandeniu. Tai užtikrina riebalų atsargų kompaktiškumą – jie laikomi bevandenėje formoje, užimdami nedidelį tūrį.
Vidutinis grynų triacilglicerolių kiekis žmogui yra maždaug 13 kg. Šių atsargų galėtų pakakti 40 dienų badavimui vidutinio fizinio krūvio sąlygomis. Palyginimui: bendros glikogeno atsargos organizme yra maždaug 400 g; badaujant šio kiekio neužtenka net vienai dienai.
2. APSAUGINĖ.
Riebalinis audinys:
a) apsaugo organus nuo mechaninių pažeidimų.
b) dalyvauja termoreguliacijoje.
Riebalų atsargų susidarymas žmonių ir kai kurių gyvūnų organizme laikomas prisitaikymu prie netaisyklingos mitybos ir gyvenimo šaltoje aplinkoje. Ypač didelę riebalų atsargą turi ilgai žiemos miegu miegantys gyvūnai (meškos, kiaunės) ir prisitaikę gyventi šaltomis sąlygomis (vėpliai, ruoniai). Vaisius praktiškai neturi riebalų ir pasirodo tik prieš gimimą.
RIEBALŲ ŠALTINIAI KŪNE:
1. Valgomieji riebalai ( egzo genetinis)
2. Endo genų riebalai, sintetinami kepenyse iš angliavandenių.
Lipidai netirpsta vandenyje, todėl kartu su baltymais pernešami kraujyje. Riebalų rūgštys kraujyje yra susijusios su albuminu, kiti lipidai yra transportuojami kaip lipoproteinų (LP) dalis.
Vienas iš veiksnių, prisidedančių prie aterosklerozinio proceso vystymosi, yra lipidų apykaitos pažeidimas. Per pastaruosius 25 metus šis faktas paskatino atlikti išsamius vaistų struktūros, jų sintezės, metabolinių transformacijų ir vaistų dalelių internalizavimo ląstelių tyrimus. Daugelyje darbų pateikiami duomenys apie skirtingų klasių vaistų dalelių savybes ir sudėtį, taip pat apie lipidų ir baltymų komponentų biosintezės ir katabolizmo ypatybes.
Fig. 1.5 pateikiamos pagrindinių kraujo plazmos lipidų struktūrinės formulės.
Laisvos arba neesterifikuotos riebalų rūgštys yra pagrindinis energijos tiekėjas organizme. Žmogaus kraujyje taip pat yra sočiųjų, mononesočiųjų ir polinesočiųjų riebalų rūgščių (1.7 lentelė).
1.7 lentelė. Riebalų rūgštys, esančios plazmoje Riebalų rūgštys Pavadinimas Ilgis
grandinė Šaltinis Myristic C 14:0 Kokosų aliejus Sočiųjų palmitų C 16:0 Gyvūniniai riebalai Stearino C 18:0 Gyvūniniai riebalai Mononesotieji Palmitoleic C 16:1 co 7 Riebalai Oleino C 18:1 co9 Sviestas Polinesočiosios linoleno C 18:2 Soob daržovės
aliejus (polienas) Arachidonic C 20:4 co8 Daržovių
Eikozapentaeno aliejus C 20:5 SOZ Žuvies taukai Pastaba. Sutrumpinta formulė nurodo anglies atomų skaičių ir dvigubų jungčių skaičių. Arčiausiai metilo galo esanti dviguba jungtis pažymėta simboliu co.
TG yra glicerolio ir riebalų rūgščių esteriai; jos, kaip ir riebalų rūgštys, yra svarbus energijos šaltinis.
Fosfolipidai yra glicerolio arba sfingozino esteriai su riebalų rūgštimis ir fosforo rūgštimi. Fosfolipidams taip pat priskiriami azoto turintys junginiai (cholinas, etanolaminas, serinas) arba kitos hidrofilinės grupės, esteriu sujungtos su fosfatu. Fosfolipidai yra visų komponentai ląstelių membranos ir LP.
CH3(CH2)„SOSG riebalų rūgštys (n> 14)
Trigliceridai ®
O CH2 - O - C - (CH,)" -CH3II I
CH, -(CH2)„ - s - O-sn apie
II
sn, - o - s - k.
Fosfolipidai O
CH, - O - C - (CH,)" -SN,
aš
CH, ~(CH2)„ - s - o-cn o
сн2 - О - Р - о -1
aš
O
Ryžiai. 1.5. Struktūrinės formulės lipidai.
Cholesterolis yra steroidas, kurio pagrindu susidaro steroidiniai hormonai ir tulžies rūgštys. Apie 2/3 kraujyje esančio cholesterolio yra riebalų rūgščių cholesterolio esterių pavidalu, o apie 1/3 – laisvojo cholesterolio pavidalu. Laisvas cholesterolis yra visų ląstelių membranų dalis; Vaiste yra ir laisvojo, ir esterinto cholesterolio.
IN klinikinė praktika Lipidų apykaitos sutrikimams nustatyti nustatomas cholesterolio ir TG kiekis kraujo serume.
LIPOPROTEINAI
Vaistų dalelės yra stambiamolekuliniai kompleksai, vidinė dalis kuriame yra neutralių lipidų (TG ir cholesterilo esterių), o paviršinis sluoksnis susideda iš fosfolipidų, neesterifikuoto cholesterolio ir specifinių lipidų transportavimo baltymų, vadinamų apolipoproteinais (apoLP).
Vaistai klasifikuojami pagal jų mobilumą elektriniame lauke (EP metu) arba hidratacijos tankį padidintos gravitacijos sąlygomis preparatinės ultracentrifugos metu (flotacija arba sedimentacija). Vykdant EF, LP skirstomi į frakcijas, iš kurių viena lieka pradžioje (chilomikronai), kitos migruoja į globulino zonas - R-LP, pre-r-LP, a-LP. Remiantis hidratuoto tankio verte, vaistai paprastai skirstomi į 5 klases: chilomikronai (CM), labai mažo tankio vaistai (VLDL), vidutinio tankio vaistai (IDL), mažo tankio vaistai (MTL), LP. didelio tankio(DTL). Pagal elektroforezinį mobilumą VLDL atitinka pre-r-LP, MTL - R-LP, DTL - a-LP, o CM lieka pradžioje (1.6 pav.).
ApoLP skatina LP micelių susidarymą hepatocitų endoplazminiame tinkle, tarnauja kaip ligandai specifiniams receptoriams ląstelių plazminės membranos paviršiuje ir kofaktoriais (aktyvatoriais ir inhibitoriais) lipolizės ir LP metabolizmo procesų kraujagyslių sluoksnyje (lentelė). 1.8).
Priklausomai nuo apoLP vaidmens organizuojant pirmines vaisto daleles ir jų vėlesnes transformacijas, sąlygų apoproteinai
bet galima suskirstyti į dvi klases. Viename iš jų turėtų būti apoLP, kurie sudaro LP kompleksų micelinę struktūrą ir tarnauja kaip LP dalelių šerdis. Tokių apoproteinų ypatybė yra ta, kad baltymai nepalieka lipidų dalelės, kurių susidaryme jie dalyvauja. Šiai apoLP grupei priklauso apoB (apoB-100 ir apoB-48) ir apoA (A-1 ir A-H), atsakingi už aferentinį ir eferentinį lipidų transportavimą. ApoB yra pagrindinis trigliceridų turinčių lipidų dalelių struktūrinis baltymas; nepalieka micelinio
1.8 lentelė. Apolipoproteinų savybės ir funkcijos DpoLP Įtraukta Vieta
sintezė Mol.
svoris,
kD Funkcijos C* in
plazma, mg/l A-1 DTL,
hmm Plonas
žarnynas,
kepenys 28.3 LCAT aktyvinimas, lipidų pernešimas, ligandas HDL receptoriams 100-1600 A-N HDL Thin
žarnynas,
kepenys 17 Struktūrinis baltymas, DTL receptorių ligandas 300-500 A-1U hmm,
lpvp,
lpon Plonas
žarnynas 46 LCAT, DTL receptorių ligando, 150 B-100 MTL aktyvinimas,
lppp,
lpon Kepenys 549 Lipidų pernešimas iš kepenų, prisijungimas prie B-, E-receptorių 500-900 B-48 hmm Plonas
žarnynas 265 Lipidų pernešimas iš plonosios žarnos lpon,
HDL kepenų 6.5 aktyvatorius LCAT lponp,
HDL kepenų 8.8 aktyvatorius LPL 30-80 S-Sh hmm,
lponp.
DTL kepenys 8.9 LPL aktyvumo inhibitorius 8-150 B HDL3 20 LCAT aktyvatorius ~100 E lponp,
hm,
DTL Kepenys 36.5 Prisijungimas prie B ir E receptorių 30-50 (a) LP(a) Kepenys 270-1000 Kompleksas vykstant nuosekliai metabolinei VLDL transformacijai į MTL ir toliau į MTL, kurio kaupimasis kraujagyslėse siena tarnauja kaip patogenetinis ryšys aterosklerozinis procesas. Apoproteinai A-1 ir A-H yra pagrindiniai DTL baltymai. Prielaidos, kad apoB ir apoA sudaro skirtingų sudėties ir funkcijų vaistų klases, pagrindas buvo tai, kad apoB ir apoA kartu nėra ilgai cirkuliuojančiose vaistų dalelėse. Genetiniai šių apoproteinų sintezės sutrikimai yra aferentinio ir eferentinio lipidų transportavimo sutrikimų priežastis.
Kita klasė apima apoLP, kurių pagrindinis vaidmuo yra vaistų metabolizmo reguliavimas kraujagyslių dugne ir ląstelių internalizacijos procesas. Šie apoproteinai vaiste yra žymiai mažesniais kiekiais ir, vykstant vaistų dalelių tarpusavio konversijai kraujyje, baltymų ir lipidų kompleksų pavidalu juda tarp skirtingų klasių vaistų. Metaboliškai aktyvūs apoLPs išlieka kraujagyslių dugne ilgiau nei vaisto dalelės, į kurias jie buvo įtraukti sintezės metu. Pagrindiniai metaboliškai aktyvių apoLP grupės atstovai yra apoE (su izoformomis E2, E3, E4) ir apoC (C-1, C-H, S-III).
ApoLP turi didelę reikšmę vaistų metabolizmui, vaidindami vaistų dalelių ligandų, kurie sąveikauja su specifinių vaistų ląstelių receptoriais, vaidmenį. ApoB-100 ir apoE sąveikauja su MTL receptoriais, pradėdami absorbcijos endocitozę, kurią lydi MTL katabolizmas. ApoE sąveikauja su likusių CM komponentų receptoriais, kurie atlieka svarbų vaidmenį pašalinant šiuos komponentus kepenyse. Manoma, kad apoA-1 sąveikauja su DTL receptoriais ir palengvina cholesterolio pašalinimą iš periferinių ląstelių, kad būtų grąžintas į kepenis.
Plazmoje yra 4 pagrindinės vaistų klasės: cholesterolis, VLDL, MTL ir DTL bei keletas kitų palyginti mažų koncentracijų vaistų: MTL ir LP(a). Lentelėje 1.9 pateikia kai kurias LP savybes.
ChM sintetinami žarnyne ir naudojami eksogeniniams lipidams transportuoti. Pagrindinis atsirandančių (pirminių) CM baltymas yra apoB-48. Netrukus po to, kai enterocitai išskiria CM, į jų sudėtį į kraujagyslių dugną įtraukiami 2 papildomi apoproteinai, esantys DTL, apoC-H ir apoE. ApoC-H aktyvuoja nuo heparino priklausomą lipoproteinų lipazę – fiksuotą fermentą
P R a Formavimosi vieta Plonoji žarna Kepenų katabolizmas
VLDL VLDL katabolizmas per MTL Kepenys, plonoji žarna, CM ir VLDL katabolizmas Pagrindinė funkcija Egzogeninio TG transportavimas Endogeninio TG transportavimas MTL transportavimo pirmtakas
Cholesterolis atvirkštinis
transporto
Cholesterolis Sudėtis: TG 90 % 65 % 20 % 5 % 5 % cholesterolis 5 % 15 % 25 % 50 % 20 % fosfolipidai 4 % 10 % 35 % 25 % 25 % baltymai 1 % 10 % 20 % 20 % 50 % apoproteinai A B-48, C, E B-100, C, E B-100, E B-100 A, C, E 1.9 lentelė. Lipoproteinų savybės
1.5. Lipidai ir lipoproteinai -f-143
ant kapiliarų endotelio. Lipoproteinų lipazė hidrolizuoja chilomikronų TG, sudarydama laisvas riebalų rūgštis. LP hidrolizės metu dalelės praranda apie 96 % savo masės, daugiausia dėl TG, taip pat apoLP A ir C. Dėl to LP dalelė paverčiama mažesne, cholesteroliu praturtinta CM liekana, kurie apoB ir apoE tarnauja kaip pagrindiniai apoLP . Gauti likutiniai CM komponentai turi hidratuotą VLDL ir LDPP tankį, ir paprastai juos iš kraujo serumo pašalina hepatocitai per specifinius receptorius (apoE receptorius). Todėl sveikiems asmenims tarpinės LP formos turi trumpas laikotarpis gyvybei ir fiziologinėmis sąlygomis kraujo serume randama mažomis koncentracijomis. Tačiau su kai kuriomis HLP formomis kraujo serume kaupiasi DILI. Dėl šių metabolinių transformacijų pašalinamas trumpalaikis HLP, atsirandantis per kelias valandas po nurijimo, o po to kepenyse panaudojami egzogeniniai lipidai. Į kepenis patenkančių lipidų riebalų rūgščių sudėtis atitinka egzogeninius lipidus. Kepenų į kraują išskiriamos LP dalelės turi žmogaus organizmui būdingą riebalų rūgščių sudėtį.
VLDL susidaro kepenyse, hepatocitai išskiria juos į kraują ir perneša endogeninį TG. Atsirandančiame VLDL yra tik apoB-100. Kraujyje VLDL taip pat apima apoLP iš DTL – apoC-P ir apoE. Metabolizmo tyrimai parodė, kad iš pradžių VLDL frakcijoje esantis radioaktyvumas greitai patenka į hidratuotas MTL tankio lipidų daleles. Sveikiems žmonėms beveik visas MTL susidaro kraujagyslių dugne iš VLDL. Metabolizmo metu daug TG turinčių vaistų, kurių sudėtyje yra apoB, dėl mažesnio tankio ir TG vaistų hidrolizės. dideli dydžiai paverčiami tankesniu ir mažesniu DILP, o paskui MTL. Kai kurie liekamieji VLDL ir LDPP komponentai pasišalina kraujagyslių lova sąveikaujant su specifiniais apoB/E receptoriais endotelio ląstelių paviršiuje. Metabolinio LDPP virsmo į MTL procese, be nuo heparino priklausomos lipoproteinų lipazės, dalyvauja ir kitas lipolitinis fermentas – kepenų trigliceridų lipazė. Šis fermentas gali veikti ne tik kaip TG hidrolazė, bet ir kaip fosfolipazė.
Žmogaus organizme yra MTL dauguma cirkuliuojančio cholesterolio ir pernešti jį į periferinius audinius membranų formavimuisi ir steroidogenezės procesams. MTL sąveikauja su kepenų ląstelių, antinksčių ir periferinių audinių plazmos membranos receptoriais, įskaitant SMC ir fibroblastus. Po sąveikos su receptoriumi MTL patiria endocitozę, o MTL komponentai katabolizuojami lizosomose. Dėl šių procesų susidaro atskiros lipidų klasės; apoproteinai suskaidomi į aminorūgštis.
Lp(a) yra daug cholesterolio ir baltymų turinti dalelė, panaši į MTL, turinti 2 apo(a) molekules, be 1 apoB molekulės. Padidėjęs Lp(a) kiekis siejamas su ankstyvu vainikinių arterijų ligos išsivystymu: 50 % pacientų, sergančių vainikinių arterijų liga, Lp(a) lygis buvo didesnis nei 40 mg/l, palyginti su 17 % kontrolinėje grupėje. Lipoproteino(a) koncentracijos padidėjimas kraujyje laikomas nepriklausomu aterosklerozės rizikos veiksniu.
DTL susidaro keliais būdais, įskaitant atsirandančio DTL sintezę ir sekreciją kepenyse ir žarnyne, lipolizuojant TG turtingus lipoproteinus arba dėl naujai susidarančių apoproteinų sąveikos su ląstelių membranomis. Atsirandantys DTL yra dvisluoksniai diskai, susidedantys iš apoLP ir fosfolipidų. Laisvasis cholesterolis difunduoja į DTL iš endotelio ląstelių, raudonųjų kraujo kūnelių ir kitų ląstelių. Be to, VLDL arba CM lipolizės metu paviršiaus lipidai (fosfolipidai ir cholesterolis) ir baltymai (apoA-1, apoA-P, C grupės apoproteinai) perkeliami į DTL frakciją. Šie komponentai gali sudaryti atsirandančias diskoidines DTL daleles arba būti įtrauktos į jau egzistuojančias DTL daleles. Diskoidinis atsirandantis DTL kraujo plazmoje sąveikauja su fermentu LCAT, todėl susidaro cholesterolio esteriai, kurie greitai pereina į dalelių branduolį; susidaro sferinės (brandos) DTL dalelės – DTL3.
Žmonėms dauguma cholesterolio esterių, susidarančių HDL, perkeliami į didesnius TG turtingus lipidus. Baltymas,
perkeliant cholesterolio esterius, skatinamas cholesterolio esterių keitimas iš DTL į TG iš lipidų, turinčių apoB, dėl to sumažėja cholesterolio esterių kiekis ir padidėja TG kiekis DTL. Dėl bendro lipolizės ir lipidų pernešimo poveikio DTL dalelės praturtėja papildomais lipidais ir apoproteinais, todėl padidėja DTL dalelių dydis ir sumažėja tankis, kartu DTL3 dalelės virsta DTLg-DTL2 dalelėmis. tada veikiama kepenų trigliceridų lipazės, fermento, daugiausia randamo endotelio ląstelėse, kepenų sinusoiduose. Kepenų trigliceridų lipazė turi ir trigliceridų hidrolazės, ir fosfolipazės aktyvumą, todėl sumažėja TG ir fosfolipidų kiekis DTL ir mažėja dalelių dydis.
Taigi kraujo plazmos vaistai, tradiciškai suskirstyti į klases fiziniais, cheminiais ir imunocheminiais metodais, metaboliškai sudaro vieną sistemą.
Vaistų klasių kiekis kraujo serume gali būti išmatuotas kiekybiškai. Tokie matavimai atliekami analitiniu ultracentrifugavimu, kuriam reikalinga sudėtinga analitinė įranga. Taip pat galima apskaičiuoti vaisto koncentraciją remiantis kiekvieno komponento analize. Šis metodas reikalauja kiekybinio kiekvienos vaistų klasės išskyrimo ir gryninimo naudojant preparatinį ultracentrifugavimą. Plazmos vaistų lygis klinikinėje biochemijoje paprastai vertinamas pagal cholesterolio kiekį juose. Paprastai TG kiekis atskirose vaistų klasėse nėra tiriamas, nes jis svyruoja daugiau nei cholesterolio kiekis. Pabrėžtina, kad dauguma epidemiologinių duomenų apie vaistų ryšį su širdies ir kraujagyslių ligų išsivystymu yra pagrįsti cholesterolio kiekio matavimais atskirose vaistų klasėse.
Santykis bendro cholesterolio pagrindinių vaistų klasių kraujo plazmą ir cholesterolį galima išreikšti šia formule:
cholesterolio kiekis kraujyje = VLDL cholesterolis +
+ MTL cholesterolis (- DTL cholesterolis.
Norėdami išmatuoti vaistų cholesterolio klases, nustatykite bendrą cholesterolio kiekį ir TG kraujo serume bei DTL cholesterolio koncentraciją supernatante, nusodinus vaistus, kurių sudėtyje yra apoB (VLDL ir MTL). Koncentracija MTL cholesterolio apskaičiuojama pagal Friedwaldo formulę:
MTL cholesterolis = bendras cholesterolis -
- DTL cholesterolis - VLDL cholesterolis.
Apytiksliai VLDL cholesterolio koncentracijai įvertinti naudojama vertė TG/5, jei cholesterolio ir TG koncentracijos išreiškiamos mg/dL, arba TG/2,2, jei cholesterolio ir TG koncentracijos išreiškiamos mmol/l. Naudojant šią formulę, kai TG koncentracija viršija 400 mg/dl, VLDL cholesterolio kiekis pervertinamas ir MTL cholesterolio kiekis yra nepakankamai įvertintas. Norint įvertinti LP pasiskirstymą pacientams, kurių TG lygis labai aukštas ir didelis CM kiekis, būtina atlikti išankstinę ultracentrifugavimą, kad būtų galima atskirti CM ir VLDL. Atskyrus VLDL frakciją ir nusodinus MTL supernatante, galima nustatyti DTL cholesterolio koncentraciją.
Patikimas metodas atskirų klasių vaistų kiekiui kraujo serume įvertinti yra EF metodas vienoje iš pagalbinių terpių: agarozės gelio, poliakrilamido gelio, celiuliozės acetato, popieriaus. Šie metodai pateikia tik atskirų vaistų klasių procentą, įskaitant HM, |3-, pre-f- ir a-LP. EF yra HLP fenotipo nustatymo pagrindas pagal Fredricksono pasiūlytą klasifikaciją (1.10 lentelė). Galutinis sprendimas dėl HLP fenotipo priimamas remiantis LP EF duomenimis, atsižvelgiant į cholesterolio ir TG koncentraciją kraujyje bei MTL cholesterolį.
Lipoproteinų kiekio kraujyje nustatymo klinikinė reikšmė
Daugybė klinikinių ir epidemiologinių tyrimų parodė, kad padidėjęs cholesterolio kiekis kraujyje yra vienas pagrindinių aterosklerozės rizikos veiksnių. Kartą-
1.10 lentelė. Hiperlipoproteinemijų klasifikacija, patvirtinta PSO tipo CM LPD MTL cholesterolio TG charakteris
sutrikimai I t N N N TT T hm Pa - N TT TT N t lpn Pp - t t t T lpn ir lpd III - plūduriuojantis r-LP t t t ACC ir DILI IV - t N N (T) t T lpn V t 1 N N (T) tt T hm ir lponp Pastaba. | - skatinimas; OKH - liekamieji cheminių junginių komponentai.
HLP vystymąsi gali sukelti genetinės anomalijos ir aplinkos veiksniai (pirminis HLP), taip pat ligos, pvz. diabetas, kepenų, inkstų patologija, hormoniniai sutrikimai(antrinė GLP). Paveldimas polinkis vaidina svarbų vaidmenį formuojant pirminį HLP. Baltųjų amerikiečių populiacijoje 63% cholesterolio kiekio svyravimų atsiranda dėl genetinės variacijos. Remiantis mono- ir dvizigotinių dvynių apklausa Rusijoje, 82% bendro cholesterolio kiekio kintamumo lemia genetiniai veiksniai.
Šiuo metu ištirta daug paveldimų lipidų apykaitos sutrikimų, tačiau tik kai kuriems yra žinomi tikslūs biocheminiai defektai, leidžiantys diagnozuoti ligą. Šios HLP formos apima šeiminę disbetalipoproteinemiją (III tipo HLP) ir šeiminę hiperchilomikronemiją (I tipo HLP).
ŠEIMOS HIPERCHOLESTEROLEMIJA
Tarp pacientų, sergančių pirmine hipercholesterolemija, dažniausiai tiriami lipidų apykaitos sutrikimai sergant šeimine hipercholesterolemija. Tai paveldima monogeninė liga, kurios aukštas lygis serumo ir MTL cholesterolio, taip pat ankstyvas vystymasis aterosklerozė ir išeminė širdies liga.
Klubo paveldėjimas šeiminė hipercholesterolemija- autosominis dominuojantis. Homozigotų liga yra sunkesnė nei heterozigotų. 60% homozigotų IŠL išsivysto iki 10 metų amžiaus. Cholesterolio kiekis serume heterozigotuose svyruoja nuo 250 iki 550 mg/dl, pastebėtas padidėjimas iki 800 mg/dl. Sausgyslių ksantomos laikomos patognominėmis pacientams, sergantiems šeimine hipercholesterolemija. Šeimos hipercholesterolemijos dažnis tarp Europos ir Amerikos populiacijų yra 1: 1 000 000 homozigotų ir 1: 500 heterozigotų, nors yra populiacijų, kuriose yra didesnis šios ligos dažnis - 1: 100 (Prancūzijos kanadiečiai, suomiai, baltaodžiai Pietų Afrikoje).
Molekulinį defektą, lemiantį šeiminės hipercholesterolemijos išsivystymą, aprašė Brownas ir Goldsteinas. Hipercholesterolemijos priežastis yra MTL receptorių defektas, dėl kurio smarkiai sumažėja MTL absorbcija, todėl kaupiasi MTL dalelės ir atitinkamai padidėja jų koncentracija kraujyje. MTL receptorių aktyvumo sumažėjimo laipsnis pacientams, sergantiems šeimine hipercholesterolemija, koreliuoja su MTL cholesterolio kiekiu, bet ne su klinikinėmis ligos apraiškomis. ankstyvos apraiškos IHD, sausgyslių ksantomų buvimas). Yra 4 MTL receptorių genetinių defektų tipai:
visiškas receptoriaus baltymo nebuvimas;
receptorių baltymų transportavimo į ląstelės paviršių sutrikimas;
receptorių defektas, neleidžiantis prisijungti prie MTL;
receptoriaus defektas, neleidžiantis jam internalizuotis po prisijungimo prie MTL. Šiuo metu nustatyta daugiau nei 150 šio baltymo mutacijų.
Nepaisant genetinio defekto, lemiančio šeiminės hipercholesterolemijos išsivystymą, nustatymo, savybės klinikinės apraiškos ligų ir lipidų apykaitos sutrikimų, šeiminės hipercholesterolemijos diagnozavimo kriterijai iki galo nenustatyti. Deja, MTL receptorių aktyvumo nustatymas šeiminės hipercholesterolemijos diagnozei nėra plačiai naudojamas. Manoma, kad šeimyninei hipercholesterolemijai diagnozuoti nedera naudoti DNR tyrimo dėl didelis kiekis mutacijos. Padidėjęs cholesterolio kiekis – neryškus diagnostinis kriterijusšeiminė hipercholesterolemija, nes aprašyta, kad pacientams sumažėjęs apoB receptorių aktyvumas ir normalus cholesterolio kiekis.
MTL dalelių prisijungimo prie receptoriaus sumažėjimą gali lemti ne tik genetiniai defektai, sąlygojantys MTL receptorių nebuvimą arba jo funkcinius sutrikimus, bet ir paveldimi ligando apoB-100 pokyčiai. Hipercholesterolemija sergančių pacientų DNR analizė atskleidė apoB-100 sintezę koduojančio geno mutaciją, dėl kurios argininas 3500 padėtyje pakeičiamas glutaminu. Ši patologija vadinama „paveldimu apoB-100 defektu“. Šio defekto pasiskirstymo dažnis populiacijoje yra panašus į šeiminės hipercholesterolemijos dažnį (1: 500), kitais duomenimis, žymiai mažesnis (1: 1300).
ŠEIMOS KOMBINUOTA HIPERLIPIDEMIJA Terminą „šeiminė kombinuota hiperlipidemija“ (FCHL) pirmą kartą pasiūlė Goldstein ir kt. 1973 m. apibūdinti paveldimą lipidų apykaitos sutrikimą, kuriame pažymėtas pirmojo laipsnio probandas ir jo giminaičiai. skirtingi tipai GLP (Na, Hn, IV). Lipidų apykaitos sutrikimai dažniausiai pasireiškia po 20 metų, tačiau juos galima nustatyti ir vyresniame amžiuje. ankstyvas amžius. Sergamumas SCHF populiacijoje, įvairių tyrėjų duomenimis, yra nuo 0,5 iki 2%, o tarp sergančiųjų miokardo infarktu – 5%, o tarp pacientų iki 60 metų, sergančių angiografiškai dokumentuota vainikinių arterijų liga – 15-20. %. Kilmės dokumentų tyrimas parodė, kad SKGL - paveldima liga su autosominiu dominuojančiu paveldėjimo tipu. Nepaisant daugybės tyrimų, SCHF biocheminis žymuo nebuvo nustatytas; Tikslus molekulinis defektas, dėl kurio susidaro SCGL, vis dar nežinomas.
POLIGENINĖ HIPERCHOLESTEROLEMIJA Tarp paveldimų lipidų apykaitos sutrikimų dažniausiai yra poligeninė hipercholesterolemija. Sergant šia liga, cholesterolio kiekio pasiskirstymas narių tokių
šeimos perkeliamos į daugiau didelės vertės nei gyventojų vidurkis. Be to, pasiskirstymas yra unimodalinis, o tai rodo, kad nėra monogeninio paveldėjimo. Manoma, kad poligeninė hipercholesterolemija atsiranda dėl kelių genų kumuliacinės įtakos, o poligeninės hipercholesterolemijos pasireiškimą daugiausia išprovokuoja aplinkos veiksniai, ypač mitybos pobūdis. Terminas „poligeninė hipercholesterolemija“ vartojamas apibūdinti pacientus, sergančius paveldima hipercholesterolemija su nežinomu genetiniu defektu ir nesant monogeninio paveldėjimo požymių.
Atsižvelgiant į poligeninį hipercholesterolemijos paveldėjimo pobūdį, ligą apibrėžiantis genetinis defektas ir jos biocheminis žymeklis (ar žymenys) nežinomi. Poligeninės hipercholesterolemijos paplitimas populiacijoje ir tarp pacientų, sergančių vainikinių arterijų liga, priklauso nuo cholesterolio kiekio, priimto kaip normalus, rodiklių: kai norma mažėja, natūraliai didėja pacientų, sergančių poligenine hipercholesterolemija, dalis.
ŠEIMOS HIPERTRIGLICERIDEMIJA
Šeiminė hipertrigliceridemija yra paveldimas lipidų apykaitos sutrikimas, kai probandui ir jo artimiesiems vidutiniškai arba reikšmingai padidėja TG kiekis esant normaliai MTL cholesterolio koncentracijai – IV arba V tipo HLP. Liga dažniausiai pasireiškia sulaukus 30 metų. Šiems pacientams dažnai, bet ne visada, sumažėja DTL cholesterolio kiekis. Paveldėjimo tipas yra autosominis dominuojantis. Šeiminė hipertrigliceridemija populiacijoje pasireiškia 1%, o pacientams, sergantiems vainikinių arterijų liga iki 60 metų amžiaus - 5-8%. Genetinis defektas, sukeliantis šeiminės hipertrigliceridemijos išsivystymą, ir šios ligos biocheminis žymuo šiuo metu nežinomi.
Hiperlipoproteinemijos diagnostikos kriterijai
Norint nustatyti HLP, reikalingi aiškūs biocheminiai kriterijai. Šiuo metu yra du požiūriai į šią problemą. Daugelį metų, remiantis epidemiologinių tyrimų rezultatais, buvo nustatytas normalus cholesterolio ir TG, taip pat MTL ir DTL cholesterolio kiekis serume. Kiekvienai populiacijai buvo nustatyti savi lipidų apykaitos rodiklių normos kriterijai, atsižvelgiant į 5–10% minimalių ir didžiausių verčių su Gauso pasiskirstymu. Šiuo atveju hiperlipidemija buvo laikoma cholesterolio ir TG koncentracija, viršijusi 90 arba 95 % Gauso grafike (pagal lytį ir amžių). Būtent šie normaliųjų verčių kriterijai yra Fredrickson ir kt. pasiūlytos GLP klasifikacijos pagrindas. ir po kai kurių PSO priimtų papildymų. Vėliau, atsižvelgiant į sukauptus duomenis apie santykius Aukštesnis lygis cholesterolio ir koronarinės širdies ligos rizikos, Nacionalinės ekspertų grupės edukacinę programą dėl cholesterolio JAV ir Europos aterosklerozės tyrimo draugijoje buvo pasiūlyta kitokia GLP klasifikacija. Vyresniems nei 20 metų vyrams ir moterims, atsižvelgiant į vainikinių arterijų ligos riziką, norimą cholesterolio kiekį kraujyje siūloma skirti atitinkamai 6,2 arba > 6,5 mmol/L. Remiantis šiais kriterijais, siūloma skirti vidutinio sunkumo hipercholesterolemiją (6,2-7,5 arba 6,5-7,8 mmol/l) ir sunkią hipercholesterolemiją (> 7,5 arba > 7,8 mmol/l).
Atitinkamai buvo pakeisti MTL cholesterolio kriterijai, o normalus TG ir DTL cholesterolio lygis liko toks pat. Nors Amerikos populiacijai vidutinio sunkumo hipercholesterolemija atitinka 75–95% Gauso pasiskirstymo lygį, šie kriterijai naudojami HLP tipavimui JAV ir Rusijoje. Mažesnių normalių verčių pasirinkimas neabejotinai pagrįstas pirminės ir antrinės vainikinių arterijų ligos prevencijos požiūriu. Be to, taikant vienodus diagnozavimo kriterijus, galima palyginti HLP paplitimą populiacijose, kurių vidutinis cholesterolio kiekis yra skirtingas. Kita vertus, 95% žmonių, sergančių HLP, nustatyta pagal epidemiologinius kriterijus, turi paveldimą HLP. Atitinkamai, mažėjant normalios vertės padidės žmonių, kurių SLP sukelia tik aplinkos veiksniai, dalis. Atsižvelgiant į tai, ieškant pacientų, sergančių sunkiomis paveldimomis hipercholesterolemijos formomis
pagal lytį ir amžių vis dar vartojamas epidemiologiškai nustatytas 90-95% cholesterolio kiekis
kantrus.
Hipolipoproteinemija
Hipolipoproteinemijos atsiranda dėl tam tikrų lipidų apykaitą reguliuojančių fermentų defektų arba apoB geno mutacijų.
Abetalipoproteinemija ir hipobetalipoproteinemija yra paveldimi sutrikimai, kuriuos sukelia apoLP B geno, pagrindinio apoLP XM ir VLDL, mutacijos. Specifinis šių sutrikimų gydymas nebuvo sukurtas.
Abetalipoproteinemija: kraujyje nėra p-lipoproteinų, CM, lipoproteinų, kurių tankis mažesnis nei 1,063 (MTL ir VLDL), raudonieji kraujo kūneliai turi daugybe smailių projekcijų (akantocitų), atsiranda vitaminų E ir A trūkumas (rezultatas). dėl MTL, pernešančio riebaluose tirpius vitaminus, nebuvimo). Žarnyno malabsorbcija yra dažna, taip pat koordinacijos sutrikimai (dėl aksonų demielinizacijos), ataksija, nistagmas, tinklainės pigmentinė degeneracija ir protinis atsilikimas. Steatorėja atsiranda dėl apoB trūkumo, kuris lemia cholesterolio susidarymą žarnyno ląstelėse. Plonosios žarnos biopsija atskleidžia riebalų intarpus epitelio ląstelėse.
Hipobetalipoproteinemiją lydi p-lipoproteinų kiekio sumažėjimas ir ji dažnai būna besimptomė. DTL kiekis yra normalus arba padidėjęs, trigliceridai 70-120 mg%, MTL 20-70 mg%. Riebalų pasisavinimas dažniausiai nesutrinka.
TRIGLICERIDAI
Trigliceridai (TG; triacilgliceroliai) yra trihidroalkoholio glicerolio ir ilgos grandinės riebalų rūgščių esteriai, tarp kurių žmogaus organizme vyrauja stearino, palmitino, palmitooleino, oleino ir linolo rūgštys. Rečiau yra polinesočiųjų linoleno ir arachidono rūgščių. Žmogaus audinių ląstelės nesintetina linolo rūgšties, todėl ji priskiriama nepakeičiamoms rūgštims. Riebalų rūgščių pasiskirstymas TG molekulėje priklauso nuo grandinės ilgio ir unaturated™ laipsnio. Vidurinę padėtį dažnai užima rūgštis, turinti ilgiausią grandinės ilgį ir didžiausias skaičius dvigubos jungtys, kraštutines pozicijas dažniausiai užima sočiosios rūgštys.
Riebalų rūgštys su maistu į organizmą patenka triacilglicerolių pavidalu, kurie plonoji žarna veikiami lipazės jie hidrolizuojasi. Gautas glicerolis ir laisvosios riebalų rūgštys absorbuojami epitelio ląstelėse, kur vyksta TG resintezė. TG susidaro kepenyse; riebalų rūgštys į kepenis patenka iš riebalinio audinio arba sintetinamos hepatocituose. TG riebalų rūgščių sudėtis organizme labiau nei fosfolipidų priklauso nuo maisto riebalų sudėties. Ilgos grandinės riebalų rūgštys, kurios yra TG dalis, yra optimalus didelės energijos junginių, susidarančių mitochondrijose riebalų rūgščių β oksidacijos metu, šaltinis. Dauguma valdžios institucijų įgyvendina TG energijos poreikiams patenkinti. Išimtis yra smegenys; jo energijos tiekimas vyksta per gliukozės metabolizmą (aerobinę glikolizę).
Kraujo plazmoje TG, kaip ir kiti lipidai (cholesterolis ir jo esteriai, fosfolipidai), pernešami kaip makromolekulinių micelinių kompleksų – LP – dalis. TG yra visose vaistų klasėse VLDL ir CM, jie sudaro didžiąją dalį lipidų. Su tam tikra patirtimi išvaizda plazma leidžia apytiksliai nustatyti TG kiekį joje. Jei kraujo plazma skaidri, TG lygis joje neviršija 180-200 mg%; ryškus kraujo plazmos opalescencija būdinga 300–500 mg% hipertrigliceridemijai, kai TG lygis viršija 600 mg%, plazma ir serumas yra neskaidrūs. CM buvimą kraujyje galima nustatyti atlikus „stovintį testą“ – „grietinėlės“ atsiradimą ant plazmos paviršiaus, kai ji laikoma 16 valandų 4 °C temperatūroje. Skaidrus kraujo serumas ir CM buvimas rodo I HLP tipą, CM nebuvimas su ryškia opalescencija arba pieniška serumo spalva rodo IV HLP tipą; CM buvimas serumo mėginio paviršiuje su ryškia opalescencija arba pieno spalva rodo, kad pacientas turi III arba V tipo HLP.
Klinikinė TG koncentracijos nustatymo reikšmė
Reikia atsiminti, kad CM gali būti sveiko žmogaus, kuris valgė mažiau nei 12 valandų iki kraujo paėmimo, kraujo serume. Dėl didelės substrato indukcijos įtakos TG lygiui TG kiekis kraujyje dienos metu gali svyruoti reikšmingose ribose. Hipertrigliceridemija gali būti apibūdinama kaip fiziologinė arba patologinė. Fiziologinė hipertrigliceridemija atsiranda pavalgius ir gali trukti 12-14 valandų; jo pasireiškimo laipsnis priklauso nuo suvartoto maisto pobūdžio ir kiekio. Hipertriglio iceridemija N-III trimestras nėštumas taip pat yra fiziologinis. Patologinė hipertrigliceridemija pagal patogenetines savybes gali būti suskirstyta į pirminę ir antrinę. Pirminę hipertrigliceridemiją sukelia genetiniai lipidų apykaitos sutrikimai arba sustiprėjusi substrato indukcija (persivalgymas). TG metabolizmo sutrikimai, atsirandantys kaip pagrindinio patologinio proceso komplikacija, priskiriami antrinei hipertrigliceridemijai.
Yra žinomos kelios pirminės hipertrigliceridemijos formos, kurias sukelia paveldimi vaistų metabolizmo defektai: šeiminė hipertrigliceridemija, šeiminė kombinuota hiperlipidemija, šeiminė disbetalipoproteinemija (III tipo HLP), šeiminė hiperchilomikronemija (I tipo HLP). Hipotrigliceridemija, kurią sukelia genetiniai apoB sintezės ar sekrecijos pokyčiai, taip pat gali būti priskiriama pirminėms TG metabolizmo sutrikimų formoms. Sergant šiomis ligomis (paveldima abetalipoproteinemija arba homozigotinė hipobetalipoproteinemija) trigliceridų kiekis gali būti sumažintas iki 19-20 mg%.
Antrinės hipertrigliceridemijos išsivystymas buvo pastebėtas sergant cukriniu diabetu, hipotiroze, nefroziniu sindromu, vartojant geriamuosius kontraceptikus ir gydant gliukokortikoidais. Paprastai, patogenetinis gydymas, nukreiptas į pagrindinį patologinis procesas, lydi TG lygio sumažėjimas.
Glikemijos lygio koregavimas insulinu arba geriamaisiais hipoglikeminiais vaistais padeda normalizuoti TG kiekį kraujyje. Palengvėjus nefroziniam sindromui, TG lygis kraujyje taip pat sumažėja, tačiau kartais išlieka padidėjęs ilgą laiką. Hormoninių kontraceptikų, gliukokortikoidų ir daugelio kitų vaistų (β adrenoblokatorių) vartojimo nutraukimas taip pat padeda normalizuoti TG lygį.
Hipertrigliceridemija pastebima su riebalų infiltracija kepenyse. Šios ligos patogenezė grindžiama, viena vertus, padidėjusiu laisvųjų riebalų rūgščių aprūpinimu kepenyse (padidėjusi lipolizė) arba padidėjusia jų sinteze (resinteze), kita vertus, VLDL sekrecijos pažeidimu kepenyse. . Daug toksiškų junginių, alkoholio, farmakologiniai preparatai prisideda prie apoLP, ypač apoB, sintezės sutrikimo, kurio nesant arba trūkstant VLDL nesusidaro. Tokiomis sąlygomis iš kraujo gaunami arba naujai susintetinti TG patenka į kepenis, sudarydami „kiaulienos kepenų“ struktūrą, sukeldami riebalų infiltraciją ir cirozę.
Hipertrigliceridemija paprastai stebima pacientams, sergantiems ūminis pankreatitas. Tačiau TG lygio padidėjimas nėra būdingas ūminiam kasos pažeidimui, priešingai, sunki hipertrigliceridemija (>1000 mg%), tiek pirminė, tiek antrinė, prisideda prie kasos ligų išsivystymo ir dažnai komplikuojasi; dėl pankreatito. Pankreatitas laikomas vienu iš klinikinių šeiminės hipertrigliceridemijos formų apraiškų. Pankreatito išsivystymas dažnai pastebimas pacientams, sergantiems cukriniu diabetu, alkoholizmu ir moterims, vartojančioms hormoninius kontraceptikus.
Duomenys apie ryšį tarp hipertrigliceridemijos ir koronarinės širdies ligos yra prieštaringi, nors daugelio populiacijų epidemiologiniai tyrimai parodė, kad TG yra koronarinės širdies ligos rizikos veiksnys. Įvertinti TG, kaip koronarinės širdies ligos rizikos veiksnio, nepriklausomumą yra labai sunku, nes yra neigiamas ryšys tarp TG ir DTL cholesterolio kiekio, nepriklausomo. neigiamas veiksnys išeminės širdies ligos rizika. Tačiau jei TG koncentracijos padidėjimas nėra savarankiškas IŠL rizikos veiksnys, glaudus TG ir DTL metabolizmo ryšys nesuteikia pagrindo paneigti hipertrigliceridemijos svarbos IŠL genezei. Biocheminis pagrindas Tai gali būti dėl DILI kaupimosi kraujyje, kuris turi ryškų aterogeniškumą.
Hipertrigliceridemijos reikšmė formuojantis periferinių ir smegenų kraujagyslių patologijoms, priešingai nei išeminės širdies ligos atveju, yra aiškesnė. Japonijos specialistų atlikti tyrimai parodė, kad šioje populiacijoje, esant žemam cholesterolio kiekiui kraujyje ir miokardo infarkto dažniui, hipertrigliceridemija yra periferinių arterijų patologijos rizikos veiksnys. Panašūs duomenys gauti ir kitose populiacijose.
TG kiekio kraujo serume tyrimas turi daug bendro su cholesterolio kiekiu. Ir cholesterolis, ir TG - konstrukciniai komponentai Vaistai, kuriuos reikia sunaikinti, kad lipidai būtų prieinami cheminėms ar fermentinėms reakcijoms. Abu junginiai yra hidrofobiniai ir mažai tirpūs vandeniniai tirpalai. Tačiau yra didelių skirtumų nustatant TG kiekį kraujo serume: norint įvertinti TG kiekį, nustatomas po TG hidrolizės išsiskyręs glicerolis.
TG kiekio kraujyje nustatymo metodai
Yra du būdai nustatyti TG kiekį kraujo serume – cheminis ir fermentinis; kiekvienas iš jų apima daugybę metodinių metodų. Šiuo metu TG galima nustatyti ir „sausosios chemijos“ metodu.
Cheminiai metodai. Norint nustatyti TG, tiesioginiai cheminiai metodai (be išankstinio ekstrahavimo organiniu tirpikliu) yra nepriimtini, nes kraujo serume yra daug junginių, kurie cheminės hidrolizės (riebalų rūgščių muilinimo) metu taip pat gali virsti gliceroliu, pavyzdžiui, fosfolipidais. ir gliukozę. Šiuo atžvilgiu į cheminiai metodai TG nustatymas, pirmasis etapas yra TG ekstrahavimas ir trukdančių junginių pašalinimas. Ekstrahavimui naudojami organiniai tirpikliai: metanolis, etanolis, izopropanolis ir chloroformas. Tirpikliai denatūruoja vaistą ir skatina TG disociaciją. Trukdantys junginiai pašalinami ekstrahuojant organiniais tirpikliais (heksanu, nonanu) arba naudojant adsorbentus (ceolitą, silicio rūgštį, florisilį).
Antrasis cheminio TG nustatymo etapas - TG hidrolizė, susidarant gliceroliui ir laisvosioms riebalų rūgštims - paprastai atliekamas reaguojant su kalio hidroksido tirpalu etanolyje aukštesnėje temperatūroje (muilinimas).
Glicerolį oksidavus iki formaldehido, jis nustatomas viena iš šių reakcijų:
formaldehido reakcija su chromotropinių ir sieros rūgščių mišiniu (matavimas esant 570 nm);
reakcija su fenilhidrazino, geležies cianido ir druskos rūgšties mišiniu (matavimas esant 540 nm);
reakcija su 3-metil-2-benzotiazolino ir geležies chlorido mišiniu (matavimas esant 620 nm);
reakcija su amonio acetatu ir acetilacetonu.
Reakcijos produktas gali būti matuojamas kolorimetriškai
412 nm arba fluorometrinis. Fluorometrinis metodas yra labiau pritaikytas pusiau automatiniams analizatoriams.
Fermentiniai metodai. Taikant fermentinius TG nustatymo metodus, lipidų kompleksų naikinimas ir TG hidrolizė atliekami naudojant ploviklius, lipazę ir proteazę. Fermentinės TG hidrolizės sąlygomis glicerolis neišsiskiria iš fosfolipidų ir gliukozės, todėl nustatymo specifiškumas didėja.
Gliceroliui, susidariusiam TG hidrolizės metu, nustatyti naudojama daug metodinių metodų, kiekvienu atveju taikant kelias susietas fermentines reakcijas. Fermentiniai metodai leidžia nustatyti TG sumažinus arba padidinus NADH koncentraciją, kai bangos ilgis 340 nm. Taip pat buvo pasiūlyti kolorimetriniai metodai: nitromėlynųjų tetrazolio druskų redukcija naudojant NADH ir susidariusio formazano (bangos ilgis 505 nm) matavimas arba 4-aminofenazono oksidacija, esant peroksidazei, kad susidarytų chromogenas (bangos ilgis 510 nm).
Naudojant fermentinį metodą išvengiama organinių tirpiklių naudojimo, ekstraktų valymo, kad būtų pašalinti trukdantys junginiai, nenaudojamas koncentruotas kalio hidroksidas ir hidrolizė aukštos temperatūros. Palyginti su cheminiais metodais, fermentinis TG nustatymas pasižymi didesniu specifiškumu ir tikslumu, o tai patogu automatizuoti.
Pagrindiniai fermentinio TG nustatymo sunkumai yra galimybė nevisiškai sunaikinti vaistų kompleksą ir nepilną hidrolizę, kai išsiskiria laisvasis glicerolis. Iš eksperimentinių tyrimų žinoma, kad TG, susidarę iš sočiųjų ir nesočiųjų riebalų rūgščių, lipazei veikiant hidrolizuojasi skirtingu greičiu; Trumpos ir ilgos grandinės riebalų rūgščių santykis taip pat turi įtakos hidrolizės greičiui.
Kadangi TG kiekis kraujo serume tiek cheminiais, tiek fermentiniais metodais nustatomas remiantis glicerolio išsiskyrimu, būtina atsižvelgti į laisvo glicerolio kiekį kraujo serume. Daugumos šviežių serumo mėginių, kurių TG lygis mažesnis nei 700 mg %, laisvojo glicerolio pokyčiai reikšmingos įtakos gautiems rezultatams neturi. Laisvo glicerolio kaupimasis kraujo serume atsiranda sergant cukriniu diabetu, kai kuriomis kepenų patologijomis, hemodializės sąlygomis, ūminiu ir lėtiniu. inkstų nepakankamumas, vartojant nitrogliceriną, gydymą heparinu. Ūminės infekcijos, trumpalaikės streso būsenos, suvartojimas vaistai, kurie turi lipolitinių savybių, žymiai padidina laisvojo glicerolio kiekį kraujyje. Spontaniška TG hidrolizė taip pat vyksta kraujo serume, ypač kai mėginiai laikomi kambario temperatūroje.
Norint tiksliai nustatyti TG lygį, reikia išmatuoti laisvo glicerolio kiekį ir atimti rezultatą iš bendrą reikšmę. Laisvo glicerolio kiekį nustatant kolorimetriniu ir fluorometriniu metodu, tame pačiame kraujo plazmos mėginyje jis gali skirtis. Fluorometrija duoda stabilesnius rezultatus, bet yra ne toks specifiškas: esant inkstų nepakankamumui ir aktyvuotai proteolizei, fluorescenciniai peptidai gali gerokai padidinti rezultatus.
Norint gauti tikslius duomenis nustatant TG, būtina naudoti pirminis standartas- triacilglicerolių tirpalas organiniuose tirpikliuose. Trioleinas paprastai naudojamas kaip standartas, nors trioleino ir tripalmitino mišinys (2:1 pagal svorį) yra panašesnis į žmogaus TG riebalų rūgščių neprisotinimo laipsnį. Standartiškai trioleino tirpalas izopropanolyje gali būti naudojamas tik cheminiams tyrimo metodams, nes izopropanolis nespecifiškai aktyvina fermentus, naudojamus TG nustatyti. Šiuo atžvilgiu, nustatant TG fermentiniais metodais, naudojami antriniai standartai (kalibratoriai) - žmogaus kraujo serumas, kuriame TG kiekis nustatomas etaloniniais metodais, naudojant pirminius standartus.
Kraujo paėmimas TG nustatymui turėtų būti atliekamas praėjus 12–14 valandų po valgio. Kraujo plazmoje nustatytos TG vertės yra 2-4% mažesnės nei serume. Taip yra dėl praskiedimo dėl skysčių, kuriuos praranda raudonieji kraujo kūneliai veikiant antikoaguliantui. Kai kurie antikoaguliantai (fluoridas, citratas ir oksalatas) sukelia didesnį skysčių netekimą iš raudonųjų kraujo kūnelių, o tai atsispindi didesniu TG sumažėjimu (iki 10%). Kaip antikoaguliantą, nustatant TG, geriau naudoti EDTA (1 mg/ml viso kraujo). Siekiant sumažinti praskiedimo efektą, būtina centrifuguoti kraujo mėginius ir atskirti gautą plazmą per 2 valandas po kraujo paėmimo.
CHOLESTEROLIO
Cholesterolis, 3-hidroksicholest-5-enas, yra mononesotusis sterolis, kurio sudėtis yra C27H40(0H)b; Autorius cheminė struktūra tai monohidroksis antrinis alkoholis (cholesterolis). Cholesterolio molekulė paremta ciklopentanperhidrofenantreno struktūra, trečioje padėtyje yra hidroksilo grupė, yra dviguba jungtis tarp 5 ir 6 anglies atomų bei šoninė alifatinė 8 anglies atomų grandinė. Terminas „cholesterolis“ apibrėžia šaltinį, iš kurio jis pirmą kartą buvo išskirtas (iš graikų kalbos cbo1e – tulžis). Molekulinė masė cholesterolio 387 D, in gryna forma tai milteliai baltas. Cholesterolis
gerai tirpsta organiniuose tirpikliuose (ypač gerai 6-7 anglies atomus turinčiuose alkoholiuose). Cholesterolio tirpumas vandenyje yra labai mažas, 4,7 µmol/l esant 25 °C temperatūrai.
Cheminė cholesterolio struktūra riboja biocheminių reakcijų, į kurias jis patenka, skaičių. Pagrindinė cholesterolio (kaip alkoholio) biocheminė transformacija yra esterio ryšio su rūgštimis, ypač su laisvosiomis riebalų rūgštimis, susidarymas, susidarant cholesterolio esteriams. 80% organizme esančio cholesterolio yra laisvasis cholesterolis, beveik visas jis yra biologinių membranų dalis. Tuo pačiu metu 2/3 cholesterolio kraujo serume yra esterių su riebalų rūgštimis pavidalu.
Cholesterolis yra visų gyvų ląstelių dalis. Biologinėse membranose cholesterolis vaidina struktūrinį vaidmenį. Jos funkcija, lemianti membranos pralaidumą ir mikroaplinkos kūrimą membranoje įmontuotiems fermentams, yra neatsiejamai susijusi su jos struktūra. Svarbi funkcija cholesterolis – jo, kaip steroidinių hormonų sintezės pirmtako, vaidmuo.
Visos organizmo ląstelės sintetina cholesterolį iš acetato, nuosekliai pereinamos per acetoacetato, metilglutarilo-CoA ir galiausiai mevalono rūgšties stadijas. Metilglutaril-CoA pavertimas mevalono rūgštimi veikiant hidroksimetilglutaril-CoA (HMG-CoA) reduktazei pagrindinis momentas cholesterolio sintezė. Susidariusi mevalono rūgštis gali būti naudojama tik cholesterolio sintezei, todėl HMG-CoA reduktazės aktyvinimas visada sukelia hipercholesterolemiją.
Didžioji dalis cholesterolio sintetinama kepenyse ir gaunama su maistu; Per dieną organizmas susintetina 1 g cholesterolio. Dalis cholesterolio oksiduojasi į tulžies rūgštis, dalis pašalinama su išmatomis. Yra abipusis ryšys tarp su maistu tiekiamo cholesterolio ir organizme susintetinto cholesterolio. Cholesterolis, kaip ir kiti lipidai, pernešamas kraujo serume kaip vaistų dalis.
Didesnėje serumo cholesterolio dalyje yra MTL; jų pagrindinis apoLP yra apoB-100. MTL yra pagrindinė cholesterolio ir polieno riebalų rūgščių transportavimo forma iš
Kepenų ir periferinių audinių klinikinė biochemija. MTL, sąveikaudamas su apoB receptoriais plazmos membranoje, yra internalizuojamas; liposomose lipidų dalelės sunaikinamos, kai išsiskiria laisvas cholesterolis. Ląstelė naudoja cholesterolį membranoms kurti, o dalis jo yra esterinama. Cholesterolio molekulės plazminės membranos Patekę į kraujo serumą, jie pradeda aferentinį kelią į kepenis kaip DTL dalis. Cholesterolis, patekęs į kepenis kaip DTL dalis, yra mikrosomiškai hidroksilinamas, virsdamas tulžies rūgštimis, taip pat išsiskiria su tulžimi laisvo cholesterolio arba jo esterių pavidalu.
Cholesterolio kiekiui įtakos turi maisto ir alkoholio vartojimo pobūdis, intensyvus fizinis rengimas, farmakologiniai vaistai, įskaitant hormoninius kontraceptikus, steroidus, lipidų kiekį mažinančius vaistus. Sezoniniai ir paros svyravimai neturi reikšmingos įtakos cholesterolio kiekiui serume. Individualūs cholesterolio dydžių svyravimai, įvairių autorių duomenimis, svyruoja nuo 3 iki 14 proc. Kasdieniai vyrų ir moterų cholesterolio kiekio svyravimai (0,7-4,3 proc.) yra žymiai mažesni nei svyravimai per
mėnesių (2,0-12,2 proc.) ir 1 metų (3,9-10,9 proc.).
Klinikinė hipercholesterolemijos reikšmė
Hipercholesterolemija yra labiausiai dokumentuotas vainikinių arterijų aterosklerozės rizikos veiksnys. Tai patvirtino daugybė epidemiologinių ir klinikiniai tyrimai kurie nustatė ryšį tarp hipercholesterolemijos ir vainikinių arterijų aterosklerozės, vainikinių arterijų ligos klinikinių apraiškų (krūtinės anginos ir miokardo infarkto) dažnio. At antrinė prevencija Koronarinė aterosklerozė regresavo lipidų kiekį mažinančio gydymo metu klinikinis vaizdas IŠL ir kardiosklerozė su normalizavus cholesterolio kiekį serume. Norint detaliau apibūdinti koronarinės aterosklerozės rizikos veiksnius, tiriamas cholesterolio kiekis atskirose vaistų klasėse; Plačiausiai naudojamas tyrimas yra MTL ir DTL cholesterolis, kurie yra patikimi koronarinės aterosklerozės rizikos ir rizikos veiksniai.
Cholesterolio tyrimas nesuteikia diagnostinės informacijos apie konkrečią ligą, bet apibūdina lipidų ir lipidų apykaitos patologiją. Cholesterolio kiekio nustatymas yra socialiai svarbus, nes padidėjus gyventojų cholesterolio kiekiui reikia įgyvendinti organizacines priemones pirminė prevencija vainikinių arterijų aterosklerozė. Didžiausias hipercholesterolemijos skaičius stebimas su genetiniais lipidų apykaitos sutrikimais: šeimine homo- ir heterozigotine hipercholesterolemija, šeimine kombinuota hiperlipidemija, poligenine hipercholesterolemija.
Su numeriu patologinės būklės išsivysto antrinė hipercholesterolemija. Tokie procesai apima hipotirozę, nefrozinis sindromas, cukrinis diabetas ir kt. Hipocholesterolemija pasireiškia esant hipertirozei, sunkiomis klinikinėmis situacijomis, lydinčiomis įvairias nosologinės formos ligų, su ūminė stadija uždegiminis procesas, taip pat vėžys.
Cholesterolio kiekio serume nustatymo metodai
Cholesterolio kiekio serume nustatymo metodų yra daug; Galima išskirti cheminius ir fermentinius metodus. Savo ruožtu tarp cheminių metodų yra tiesioginiai ir netiesioginiai (ekstrahavimo) metodai.
CHEMINIAI CHOLESTEROLIO KONCENTRACIJOS NUSTATYMO METODAI
Tiesioginiai metodai. Tiesioginių cholesterolio nustatymo metodų pagrindas yra Liebermanno-Burkhardo reakcija, kurios metu cholesterolis reaguoja su sieros ir acto rūgščių mišiniu, taip pat su acto rūgšties anhidridu. Reakcija vyksta stipriai rūgščioje bevandenėje terpėje. Reakcijos metu cholesterolio molekulė nuosekliai oksiduojasi ir susidaro spalvotas junginys cholestageksaenas – sieros rūgštis, kurių absorbcijos maksimumai ties 410 ir 610 nm. Besivystanti spalva yra nestabili, todėl reikia tiksliai išlaikyti fotometrinį laiką. Literatūroje galite rasti skirtingus ingredientų santykius Liebermann-Burkhard reagente; Kuo didesnis acto anhidrido kiekis, tuo greičiau vyksta reakcija. Reak
cholesterolio reakcija su Liebermann-Burkhard mišiniu yra nespecifinė tiesioginis apibrėžimas cholesterolio, reakcijos mišinio su standartiniu tirpalu spalva yra smaragdas; Serumo mėginiai gali būti žalios, mėlynos arba rudos spalvos. Taip yra dėl to, kad daugelis kraujo serumo komponentų reaguoja. Be to, Liebermanno-Burkhardo reakcijoje laisvasis cholesterolis ir jo esteriai sudaro spalvotus kompleksus su skirtingais molinės absorbcijos koeficientais: cholesterolio esterių atveju optinis tankis yra didesnis. Tai iš esmės įtraukia į tyrimą klaidų, nes laisvo cholesterolio / cholesterolio esterių santykis kiekviename mėginyje nežinomas.
Killiany-Zak reakcija yra dar vienas paplitęs cholesterolio nustatymo metodas (cholesterolio reakcija su geležies druskomis, acto ir sieros rūgštimis). Tai cheminė reakcija atsiranda esant geležies geležies jonams, nuosekliai susidarant 2, 3 ir 4 dviguboms konjuguotoms jungtims cholesterolio molekulėje, o susidariusių junginių sugerties maksimumas svyruoja nuo 420 iki 563 nm. Killiany-Zak reakcijoje laisvasis cholesterolis ir jo esteriai suteikia panašių spalvų kompleksus.
Netiesioginiai metodai. Netiesioginiai metodai apima metodus, kai lipidai iš kraujo serumo pirmiausia ekstrahuojami organiniais tirpikliais, o po išgarinimo atliekama Liebermann-Burkhard reakcija. Šis metodas yra labiau atkuriamas ir tikslesnis, nes galima pašalinti trikdančias medžiagas, likusias vandeninėje fazėje. Ekstrahavimui naudojamos etanolio-dietilo eterio, etanolio-acetono, metanolio-chloroformo sistemos; dažniausiai naudojamas heksanas ir izopropilo alkoholis. Ekstrahavimo žingsnio įtraukimas padidina metodo specifiškumą; cholesterolio nustatymo rezultatai yra 7% mažesni nei tiesioginiu metodu.
Pamatiniai cholesterolio kiekio nustatymo metodai yra 3 etapai; tai apima lipidų ekstrakciją į nepolinį tirpiklį, cholesterolio esterių muilinimą ir pakartotinį cholesterolio ekstrahavimą iš muilinto mišinio. Labiausiai pageidaujamas pamatinis metodas yra Abell-Kendall metodas, pasiūlytas 1952 m.: lipidų ekstraktas muilinamas alkoholiniu kalio hidroksido tirpalu ir ekstrahuojamas petroleteriu. Liebermanno-Burkhardo reakcija atliekama išgarinus petroleterio eterį.
Sunkumai ruošiant standartinius cholesterolio tirpalus yra susiję su jo hidrofobiškumu. Ilgas laikas Kaip standartinis tirpalas buvo naudojamas cholesterolio tirpalas ledinėje acto rūgštyje. Be to, kaip standartas buvo pasiūlytas cholesterolio tirpalas izopropanolyje, tačiau toks standartas pasirodė esąs nepatogus fermentiniams cholesterolio nustatymo metodams, nes izopropanolis aktyvuoja fermentų sistemas, didindamas optinį tankį. Norint nustatyti cholesterolio kiekį dirbant su biocheminiais analizatoriais, visuotinai priimta naudoti antrinius etalonus (kalibratorius) – kraujo serumą, kurio cholesterolio lygis nustatomas etaloniniais metodais.
Nepaisant santykinio įgyvendinimo paprastumo ir mažos procedūros kainos, cheminiai metodai yra toksiški, o jų naudojimas šiuolaikiniuose analizatoriuose yra susijęs su sistemos korozija.
FERMENTINIAI KONCENTRACIJOS NUSTATYMO METODAI
CHOLESTEROLIO
Fermentinio nustatymo privalumai: reakcijos vykdymas vandeninėje fazėje; automatizavimo paprastumas; didelis jautrumas ir specifiškumas.
Fermentinis cholesterolio nustatymas taip pat apima kelis etapus: fermentinė cholesterolio esterių hidrolizė, veikiant cholesterolio esterazei, susidarant laisvajam cholesteroliui ir laisvosioms riebalų rūgštims; cholesterolio oksidacija deguonimi, ištirpusiu reakcijos terpėje, veikiant cholesterolio oksidazei, susidarant cholest-4-en-3-oliui ir H2O2. Taikant plačiausiai naudojamus metodus, susidaręs vandenilio peroksidas oksiduoja tam tikrus junginius, kad susidarytų chromogenai, kuriuos galima išmatuoti fotometriškai. Tokie chromogenai gali apimti 4-aminofenazoną (absorbcijos maksimumas 500-525 nm), taip pat Henacho heterociklo susidarymą reaguojant su metanoliu (absorbcijos maksimumas 405 nm). Galima registruoti reakcijoje susidariusį vandenilio peroksidą su nuo NAD priklausomomis dehidrogenazėmis ir išmatuoti optinį tankį esant 340 nm bangos ilgiui.
Kaip ir naudojant cheminius metodus, kai kurie serumo cholesterolio komponentai gali turėti įtakos nustatymo rezultatams. Bilirubinas slopina peroksidazės reakciją su 4-aminoantipirinu ir fenoliu. Sulfhidrilo grupių reduktoriai (glutationas, cisteinas, ditiotreitolis) taip pat turi įtakos reakcijos rezultatams. Skirtingomis fermentinėmis reakcijomis pagrįsti metodai gali duoti skirtingus rezultatus.
Cholesterolio fermentinio nustatymo metodologiniai sunkumai yra susiję su cholesterolio pasiskirstymo tarp vaistų nevienalytiškumu, taip pat su jo esterifikacija kraujyje. Choleesterio esterių hidrolizės užbaigtumas priklauso nuo fermento šaltinio. Mikrobinė cholesterolio esterazė aktyviau hidrolizuoja sočiųjų riebalų rūgščių suformuotus cholesterolio esterius, o kasos cholesterolio esterazė – polinesočiąsias riebalų rūgštis.
Kraujo paėmimas visiems lipidams nustatyti paprastai atliekamas po 12–16 valandų nevalgius. Cholesterolio koncentracija kraujyje prieš ir po valgio nekinta, tačiau nustatymui gali trukdyti ryškus kraujo serumo opalescencija dėl CM ir VLDL. Patartina, kad pacientas nekeistų įprastos dietos mažiausiai 2 savaites iki kraujo paėmimo. Serumas arba plazma gali būti naudojami cholesterolio kiekiui nustatyti. Sausas EDTA (1 mg/ml kraujo) dažniausiai naudojamas kaip antikoaguliantas plazmos gamybai, kuris taip pat turi antioksidacinių savybių. Cholesterolio koncentracija kraujo serume yra 2-4% mažesnė nei kraujo plazmoje.
Lipidai– į riebalus panašios medžiagos, kurios yra visų gyvų ląstelių dalis. Tai plati grupė organiniai junginiai, įskaitant riebalų rūgštis, taip pat jų darinius – tiek radikalų, tiek karboksilo grupę. Lipidai vaidina labai svarbų vaidmenį gyvybės procesuose.
Lipidai atlieka labai įvairias funkcijas. Jie yra ląstelių membranų dalis ir tarnauja kaip steroidinių hormonų, tulžies rūgščių, prostaglandinų ir fosfoinositidų pirmtakai.
Kraujyje yra atskirų lipidų komponentų – sočiųjų riebalų rūgščių (SFA), mononesočiųjų riebalų rūgščių (MUFA) ir polinesočiųjų riebalų rūgščių (PUFA), trigliceridų, cholesterolio, cholesterolio esteriai ir fosfolipidai.
Lipidai yra pagrindiniai biologinių membranų komponentai, turintys įtakos ląstelių pralaidumui ir daugelio fermentų aktyvumui, taip pat dalyvaujantys nervinis impulsas, raumenų susitraukime, tarpląstelinių kontaktų kūrime, imunocheminiuose procesuose.
Lipidai pasižymi jų tirpumu organiniuose tirpikliuose ir, kaip taisyklė, netirpsta vandenyje; yra visose gyvose ląstelėse. Lipidai sudaro energijos rezervą ir sukuria apsauginį vandenį atstumiantį ir šilumą izoliuojantį dangą gyvūnams ir augalams, taip pat saugo įvairius organus nuo mechaninio įtempimo. (pagal TSB, Vikipedijos, SMT medžiagas).
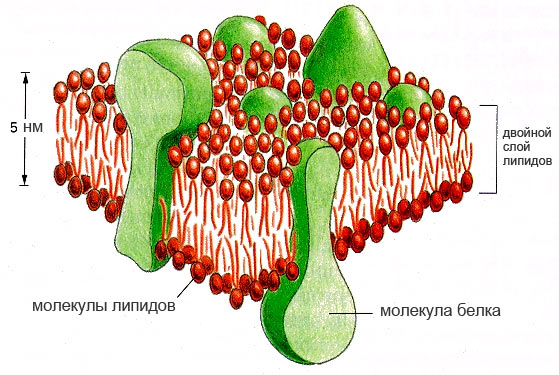
Ląstelės membrana
Lipidai per kraują pernešamas į įvairius organus ir audinius kaip sudėtinių makromolekulinių junginių dalis - lipoproteinai , kurie yra įvairių baltymų (apoproteinų) ir lipidų junginiai.
Lipoproteinai skirstomi į:
Lipoproteinai skiriasi dydžiu, sudėtimi ir vaidmeniu aterogenezėje.
Klinikinėje praktikoje didžiausia vertė MTL ir DTL vaidina svarbų vaidmenį vystant kraujagyslių patologiją.
MTL daugiausia sudarytas iš cholesterolio esterių. Jų funkcinis apoproteinas yra apoB-100.
Kad MTL taptų aterogeninis, jis turi būti modifikuotas, o tai dažniausiai sukelia jo peroksidacijos procesas. Oksiduotas MTL keičia savo savybes. Pirmiausia sutrinka jų sąveika su kepenų receptoriais, vėliau jie tampa aktyviais monocitų dirgikliais. Suaktyvinti kraujo monocitai prasiskverbia pro kraujagyslės subendotelinę erdvę, virsdami makrofagais, kurie fagocituoja modifikuotą MTL ir virsta putplasčio ląstelėmis, t.y. ląstelės, perpildytos cholesterolio esteriais. Būtent MTL cholesterolis, atsižvelgiant į jo svarbų vaidmenį formuojantis aterosklerozinėms plokštelėms, yra pagrindinis lipidų kiekį mažinančios terapijos tikslas.
DTL atlikti atvirkštinį cholesterolio transportavimą iš kraujagyslių sienelė ir makrofagai į kepenis, iš kurių jie išsiskiria iš organizmo kaip tulžies rūgščių dalis. Yra du DTL poklasiai: DTL-2 ir DTL-3. Būtent DTL-3 sulaiko cholesterolį iš periferinių ląstelių ir makrofagų ir virsta DTL-2, kurį sudaro cholesterolio esteriai ir fosfolipidai. DTL jungiasi prie kepenų receptorių ir kraujagyslių sienelių ląstelių per apoproteinus (apoA-1 ir apoA-2).
Mažo tankio lipoproteinai– Tai baltymų junginiai su cholesteroliu, pernešantys pastarąjį iš kepenų į audinius. MTL neša reikalingą cholesterolį į audinius, tačiau didėjant jų koncentracijai, didėja rizika susirgti ateroskleroze.
Pagal aterogeninis būtina suprasti lipoproteinus, kurių didelė koncentracija kraujo plazmoje patikimai siejama su aterosklerozės išsivystymu.
Makrofagai- didelės ląstelės, susidarančios iš monocitų, galinčios fagocitozei - aktyvaus gyvų ir negyvų dalelių gaudymo ir absorbcijos procesas vienaląsčių organizmų arba specialių daugialąsčių gyvūnų organizmų ląstelių (fagocitų).
Literatūra
Lipidų apykaitos sutrikimų diagnostika ir korekcija aterosklerozės profilaktikai ir gydymui. Rusijos rekomendacijos. Sukūrė GFOC ekspertų komitetas. M., 2004 m.
Lipidų apykaitos sutrikimų diagnostika ir korekcija aterosklerozės profilaktikos ir gydymo tikslais // Trumpos Rusijos rekomendacijos. Sukūrė VNOK ekspertų grupė. M., 2005 m.
Orlovas R.S., Nozdrachevas A.D. Normali fiziologija: Vadovėlis. – M.: GEOTAR-Media, 2009 m.
Pogoževa A.V. Širdies ir kraujagyslių ligų racionalios dietos terapijos pagrindai // Klinikinė dietologija. 2004. T.1. Nr. 2.
Pogoževa A.V. Šiuolaikinės reprezentacijos apie arterinės hipertenzijos dietos terapiją // Medicina. Gyvenimo kokybė. 2005. Nr.3.
Dieta, mityba ir prevencija lėtinės ligos. PSO. Ženeva, 1993 m.
Reabilitacija nuo ligų širdies ir kraujagyslių sistemos/ Red. I.N. Makarova. M., 2010 m.


