Алдостеронът при хората е основният представител на минералкортикоидните хормони, производни на холестерола.
Синтез
Осъществява се в зоната гломерулоза на надбъбречната кора. Прогестеронът, образуван от холестерол, претърпява последователно окисление по пътя си до алдостерон. 21-хидроксилаза, 11-хидроксилаза и 18-хидроксилаза. В крайна сметка се образува алдостерон.

Схема за синтез на стероидни хормони (пълна схема)
Регулиране на синтеза и секрецията
Активирате:
- ангиотензин II, освободени при активиране на системата ренин-ангиотензин,
- повишена концентрация калиеви йонив кръвта (свързано с деполяризация на мембраната, отваряне на калциеви канали и активиране на аденилат циклаза).
Активиране на системата ренин-ангиотензин
- За да активирате тази система, има две начални точки:
- намаляване на наляганетов аферентните артериоли на бъбреците, което се определя барорецепториклетки на юкстагломеруларния апарат. Причината за това може да бъде всяко нарушение на бъбречния кръвен поток - атеросклероза бъбречни артерии, повишен вискозитет на кръвта, дехидратация, загуба на кръв и др.
- намаляване на концентрацията на Na + йонив първичната урина в дисталните тубули на бъбреците, което се определя от осморецепторите на клетките на юкстагломеруларния апарат. Възниква в резултат на безсолна диета, при продължителна употреба на диуретици.
Постоянната и независима от бъбречния кръвен поток секреция на ренин (базална) се поддържа от симпатиковата нервна система.
- При изпълнение на една или и двете точки на клетката юкстагломеруларен апаратсе активират и от тях ензимът се отделя в кръвната плазма ренин.
- За ренин в плазмата има субстрат - протеин от α2-глобулиновата фракция ангиотензиноген. В резултат на протеолизата се образува декапептид т.нар ангиотензин I. На следващо място, ангиотензин I с участието ангиотензин конвертиращ ензим(APF) се превръща в ангиотензин II.
- Основните мишени на ангиотензин II са гладките миоцити кръвоносни съдовеИ zona glomerulosa cortexнадбъбречни жлези:
- стимулирането на кръвоносните съдове предизвиква техния спазъм и възстановяване кръвно налягане.
- секретирани от надбъбречните жлези след стимулация алдостерон, въздействащи върху дисталните тубули на бъбреците.
Когато алдостеронът действа върху бъбречните тубули, реабсорбцията се увеличава Na+ йони, следва натрий вода. В резултат на това налягането в кръвоносната система се възстановява и концентрацията на натриеви йони се повишава в кръвната плазма и следователно в първичната урина, което намалява активността на RAAS.

Активиране на системата ренин-ангиотензин-алдостерон
Механизъм на действие
Цитозолен.
Цели и ефекти
Влияе слюнчените жлези, върху дисталните тубули и събирателните канали на бъбреците. Укрепва в бъбреците реабсорбция на натриеви йонии загуба на калиеви йони чрез следните ефекти:
- увеличава количеството на Na +,K + -ATPase с базална мембранаепителни клетки,
- стимулира синтеза на митохондриални протеини и увеличаване на количеството енергия, генерирана в клетката за работата на Na +,K + -ATPase,
- стимулира образуването на Na канали върху апикалната мембрана на бъбречните епителни клетки.
Патология
Хиперфункция
Синдром на Кон (първичен алдостеронизъм) – възниква при аденоми на zona glomerulosa. Характеризира се с триада от симптоми: хипертония, хипернатремия, алкалоза.
Вторихипералдостеронизъм - хиперплазия и хиперфункция на юкстагломерулните клетки и прекомерна секреция на ренин и ангиотензин II. Има повишаване на кръвното налягане и появата на оток.
Системата ренин-ангиотензин-алдостерон е комплекс от ензими и хормони, които поддържат хомеостазата. Регулира баланса на солта и водата в организма и нивата на кръвното налягане.
Механизъм на действие
Физиологията на системата ренин-ангиотензин-алдостерон произхожда от границата на кората и там, където има юкстагломерулни клетки, които произвеждат пептидаза (ензим) - ренин.
Ренинът е хормон и началната връзка на RAAS.
Ситуации, при които ренин се освобождава в кръвта
Има няколко състояния, при които хормонът навлиза в кръвта:
- Намален кръвен поток в бъбречната тъкан - по време на възпалителни процеси (гломерулонефрит и др.), с диабетна нефропатия, тумори на бъбреците.
- Намален (с кървене, многократно повръщане, диария, изгаряния).
- Падащи нива на кръвното налягане. Артериите на бъбреците съдържат барорецептори, които реагират на промените в системното налягане.
- Промяна в концентрацията на натриеви йони. В човешкото тяло има клъстери от клетки, които реагират на промените в йонния състав на кръвта чрез стимулиране на производството на ренин. Солта се губи, когато обилно изпотяване, както и при повръщане.
- Стрес, психо-емоционален стрес. Бъбреците се инервират от симпатиковите нерви, които се активират от негативни психологически влияния.
В кръвта ренинът се среща с протеин - ангиотензиноген, който се произвежда от чернодробните клетки и отнема фрагмент от него. Образува се ангиотензин I, който е източник на действие на ангиотензин-конвертиращия ензим (ACE). Резултатът е ангиотензин II, който служи като втора връзка и е мощен вазоконстриктор артериална система(свива кръвоносните съдове).
Ефекти на ангиотензин II
Цел: увеличаване артериално налягане.
- Насърчава синтеза на алдостерон в гломерулната зона на надбъбречната кора.
- Въздейства върху центъра на глада и жаждата в мозъка, предизвиквайки „солен” апетит. Човешкото поведение става мотивирано да търси вода и солена храна.
- Влияе симпатикови нерви, насърчаване на освобождаването на норепинефрин, който също е вазоконстриктор, но по-малко слабо действие.
- Той засяга кръвоносните съдове, причинявайки им спазми.
- Участва в развитието на хронична сърдечна недостатъчност: насърчава пролиферацията, фиброзата на кръвоносните съдове и миокарда.
- Намалява
- Инхибира производството на брадикинин.

Алдостеронът е третият компонент, който действа върху крайните тубули на бъбреците и насърчава освобождаването на калиеви и магнезиеви йони от тялото и реабсорбцията (реабсорбцията) на натрий, хлор и вода. Поради това се увеличава обемът на циркулиращата течност, кръвното налягане се повишава и бъбречният кръвоток се увеличава. Рецептори за алдостерон се намират не само в бъбреците, но и в сърцето и кръвоносните съдове.
Когато тялото достигне хомеостаза, започват да се произвеждат вазодилататори (вещества, които разширяват кръвоносните съдове) - брадикинин и калидин. И компонентите на RAAS се разрушават в черния дроб.
Диаграма на системата ренин-ангиотензин-алдостерон

Като всяка система, RAAS може да се провали. Патофизиологията на системата ренин-ангиотензин-алдостерон се проявява при следните състояния:
- Увреждане на надбъбречната кора (инфекция, кръвоизлив и травма). Развива се състояние на дефицит на алдостерон и тялото започва да губи натрий, хлор и вода, което води до намаляване на обема на циркулиращата течност и понижаване на кръвното налягане. Състоянието се компенсира чрез въвеждане солеви разтвории стимулатори на алдостероновия рецептор.
- Туморът на надбъбречната кора води до излишък на алдостерон, който реализира своите ефекти и повишава кръвното налягане. Също така се активират процесите на клетъчно делене, настъпва миокардна хипертрофия и фиброза, развива се сърдечна недостатъчност.
- Патология на черния дроб, когато разрушаването на алдостерона е нарушено и настъпва неговото натрупване. Патологията се лекува с блокери на алдостеронови рецептори.
- Възпалителни бъбречни заболявания.

Значението на RAAS за живота и медицината
Системата ренин-ангиотензин-алдостерон и нейната роля в организма:
- приема Активно участиеза поддържане на нормално кръвно налягане;
- осигурява баланса на вода и соли в организма;
- поддържа киселинно-алкалния баланс на кръвта.
Системата може да се провали. Като повлияете на неговите компоненти, можете да се борите с хипертонията. Механизмът на бъбречната хипертония също е тясно свързан с RAAS.
Високо ефективни групи лекарства, които са синтезирани чрез изследване на RAAS
- — Прили. APF. Ангиотензин I не се превръща в ангиотензин II. Няма вазоконстрикция - няма повишаване на кръвното налягане. Лекарства: Амприлан, Еналаприл, Каптоприл и др. АСЕ инхибиторите значително подобряват качеството на живот на пациентите с диабет, като осигуряват профилактика на бъбречна недостатъчност. Лекарствата се приемат в минимална доза, която не води до намаляване на налягането, а само подобрява локалния кръвен поток и гломерулната филтрация. Лекарствата са незаменими при бъбречна недостатъчност, хронично заболяванесърце и служи като едно от средствата за лечение на хипертония (ако няма противопоказания).
- "сартани". Ангиотензин II рецепторни блокери. Съдовете не реагират на него и не се свиват. Лекарства: Лозартан, Епросартан и др.

Обратното на системата ренин-ангиотензин-алдостерон е кининовата система. Следователно, блокирането на RAAS води до увеличаване на компонентите на кининовата система (брадикинин и др.) В кръвта, което има благоприятен ефект върху сърдечната тъкан и съдовите стени. Миокардът не изпитва глад, тъй като брадикининът увеличава локалния кръвен поток и стимулира производството на естествени вазодилататори в клетките на бъбречната медула и микроцитите на събирателните канали - простагландини Е и I2. Те неутрализират пресорния ефект на ангиотензин II. Съдовете не се спазмират, което осигурява адекватно кръвоснабдяване на органите и тъканите на тялото, не се задържа кръв и се намалява образуването на атеросклеротични плаки и кръвни съсиреци. Кинините имат благоприятен ефект върху бъбреците и повишават диурезата (дневното отделяне на урина).
Ренин
– ензим, синтезиран от юкстагломерулни клетки на бъбречни аферентни артериоли, имащ MW около 40 kDa. Образуването на ренин се проявява особено интензивно по време на бъбречна исхемия. Местоположението на юкстагломерулните клетки ги прави особено чувствителни към промени в кръвното налягане, както и към концентрацията на Na + и K + йони в течността, протичаща през бъбречните тубули. Поради тези свойства всяка комбинация от фактори, която причинява намаляване на обема на течността (дехидратация, спад на кръвното налягане, загуба на кръв и др.) или намаляване Концентрация на NaCl, стимулира отделянето на ренин.
В същото време повечето регулатори на синтеза на ренин действат чрез бъбречни барорецептори.Освобождаването на ренин се влияе от състоянието на централната нервна система, както и от промените в позицията на тялото в пространството. По-специално, при преминаване от легнало положение в седнало или изправено положение (клиностатичен тест), секрецията на ренин се увеличава. Тази рефлексна реакция се причинява от повишаване на тонуса на симпатиковата част на вегетативната нервна система, предаващи импулси към b-адренергичните рецептори на юкстагломерулните клетки.
Основният субстрат, засегнат от ренина, е ангиотензиноген– протеин, включен във фракцията на a2-глобулините и произвеждан от черния дроб. Под влияние на глюкокортикоидите и естрогените синтезът на ангиотензиноген се увеличава значително. В резултат на действието на ренина ангиотензиногенът се превръща в декапептид ангиотензиназТова съединение има изключително слаб ефект и не оказва значително влияние върху нивата на кръвното налягане.
Междувременно ангиотензиназпод влиянието на т.нар ангиотензин конвертиращ ензим (ACE)се превръща в мощен вазоконстрикторен фактор - ангиотензинII. APF(дипептид карбоксипептидаза) е интегрален протеин, разположен основно върху мембраната на ендотелните клетки, епитела, мононуклеарните клетки, нервните окончания, клетките на репродуктивните органи и др. Разтворимата форма на ACE присъства в почти всички телесни течности.
Обичайно е да се разграничават две изоформи на АСЕ. Първият от тях получи условното наименование "соматичен". Тази изоформа има MW от 170 kDa и включва хомоложни C и N домени. Втората форма на ACE („репродуктивна“) се намира в семенната течност, има MW от около 100 kDa и съответства на С-домена на първата изоформа на ACE. Всеки от 2-те посочени домена съдържа аминокиселинни остатъци, които могат да участват в образуването на връзка с цинковия атом. Такива Zn 2+ структури са типични за много металопротеинази и са основните места на взаимодействие на ензима както със субстрата, така и с АСЕ инхибиторите.
Трябва да се отбележи, че АСЕ води не само до формирането ангиотензин II,но и унищожава брадикинин –разширителна връзка кръвоносни съдове. Следователно повишаването на кръвното налягане при излагане на ACE е свързано както с образуването на ангиотензин II, така и с разграждането на брадикинина (фиг. 32).
Важна роля за действието на АСЕ играе йонният състав и по-специално съдържанието на хлорни йони. По този начин, при високи концентрации на Cl, С домейнът на ACE хидролизира брадикинина и ангиотензин I по-бързо от N домейна. В извънклетъчните области, където концентрацията на хлоридни аниони е висока, N-доменът е отговорен основно за превръщането на ангиотензин-I. Въпреки това, вътреклетъчно, където концентрацията на Cl е ниска, N-доменът може да участва в хидролизата на други пептидни вещества.
Отзад последните годиниУстановено е, че АСЕ играе важна роля в хематопоезата, тъй като под негово влияние се образуват хематопоетичен пептид, инхибирайки образуването на хемопоетични клетки в костния мозък.
Ролята на АСЕ в организма е разкрита при мишки без АСЕ ген. Такива животни са имали ниско кръвно налягане, различни съдови дисфункции, нарушена бъбречна структура и функция и безплодие при мъжете.
ангиотензинII
повишава кръвното налягане чрез причиняване на артериоларна констрикция и е най-мощният познат вазоактивен агент. В допълнение, чрез механизъм за обратна връзка, той инхибира образуването и освобождаването на ренин от юкстагломерулните клетки на бъбреците, което в крайна сметка трябва да възстанови нормалните нива на кръвното налягане. Под влияние ангиотензинIIпроизводството на основния минералкортикоид рязко се увеличава - алдостерон.Въпреки че това действие е директно, ангиотензин II не повлиява производството на кортизол. Основната цел на алдостерона е задържането на Na + (чрез засилване на неговата реабсорбция в бъбречните тубули) и освобождаването на K + и H + (главно през бъбреците). Тези реакции се провеждат както следва.
Алдостерон
прониква от извънклетъчната течност в цитоплазмата на клетката и там се свързва със специфичен рецептор, след което полученият комплекс (алдостерон + рецептор) прониква в ядрото. Алдостеронът също така стимулира отварянето на Na + канали, което позволява на Na + йони да навлязат в клетката през апикалната мембрана от лумена на тубула.
Увеличаването на секрецията на К + под въздействието на алдостерон се дължи на увеличаване на пропускливостта на апикалната мембрана по отношение на тези йони, поради което К + навлиза в лумена на тубула от клетката.
Задържането на Na+ в тялото, подобно на ангиотензин II, допринася за повишаване на кръвното налягане.
ангиотензинIIе способен да се свързва със специфични рецептори на гломерулните клетки на надбъбречната жлеза. Съдържанието на тези рецептори до голяма степен зависи от концентрацията на K + йони. По този начин, ако нивото на K + се повиши, тогава броят на рецепторите за ангиотензин II в гломерулните клетки се увеличава. При намаляване на концентрацията на K + йони се наблюдава обратен ефект. Следователно K + йони играят основна роля в действието на ангиотензин II върху надбъбречните жлези.
Отзад напоследъкопредели това ангиотензинIIе в състояние да активира макрофагите, като по този начин повишава агрегацията на тромбоцитите и ускорява съсирването на кръвта. В същото време се освобождава инхибитор на активатора плазминоген-аз (IAP-1),което може да бъде придружено от потискане на фибринолизата. А ангиотензинIIе един от факторите, допринасящи за развитието на атерогенезата, инхибирането на апоптозата и повишения оксидативен стрес в тъканите, като по този начин провокират тромбоцитната агрегация и образуването на тромби.
ангиотензинIIе в състояние да подобри функцията на миокарда, участва в биосинтезата на норепинефрин и други физиологично активни вещества. В същото време той може да действа като растежен фактор, водещ до съдова и сърдечна хипертрофия.
При някои животни и при хората ангиотензинIIпод въздействието на ензим аминопептидазисе превръща в хептапептид ангиотензинIII.При хората нивото на ангиотензин II е приблизително 4 пъти по-високо от ангиотензин III. И двете съединения влияят върху кръвното налягане и производството на алдостерон и се разграждат доста бързо от ензимите ангиотензиназа.
При тежки бъбречни заболявания, придружени от исхемия, поради повишено образуване и секреция на ренин, се наблюдава постоянно повишаване на кръвното налягане ( бъбречна хипертония). Използването на АСЕ инхибитори при тези състояния води до бързо нормализиране на кръвното налягане.
В заключение трябва още веднъж да се подчертае, че ангиотензин-ренин-алдостероновата система е тясно свързана с функцията на каликреин-кининовата система, тъй като образуването на ангиотензин II и разрушаването на брадикинина се извършват под влиянието на същата. ензим - АСЕ.
Catad_theme Артериална хипертония- статии
Catad_tema Затлъстяване - статии
Затлъстяване и артериална хипертония
Публикувано в сп.:ПРОБЛЕМИ НА ЖЕНСКОТО ЗДРАВЕ № 4, том 3, 2008 г.
Е. И. Асташкин, М. Г. Глезер
Московска медицинска академия на име. И.М.Сеченова
РЕЗЮМЕ
В обзора се анализира ролята на затлъстяването за развитието на артериалната хипертония и сърдечно-съдови заболявания, патофизиологични механизми на тази връзка, доминиращата роля на системата ренин-ангиотензин-алдостерон (RAAS). Обсъждат се въпросите за фармакологичната корекция на високото кръвно налягане при пациенти със затлъстяване с помощта на фиксирана комбинация от лекарства, които блокират RAAS и верапамил. Представен е анализ на ефективността и безопасността на употребата на сибутрамин за отслабване при пациенти с високо кръвно налягане.
Ключови думи:затлъстяване, артериална хипертония, лечение.
РЕЗЮМЕ
Авторите анализират ролята на затлъстяването в развитието на артериалната хипертония и сърдечно-съдовите заболявания, патофизиологичните механизми на тази връзка и доминиращата роля на системата ренин-ангиотензин-алдостерон (RAAS). Доказано е, че фармакологичната корекция на високото кръвно налягане при пациенти със затлъстяване с фиксирана комбинация от блокери на RAAS и верапамил е ефективна. Представен е анализът на ефективността и безопасността на сибутрамин за отслабване при пациенти с високо кръвно налягане.
Ключови думи:затлъстяване, артериална хипертония, лечение.
Актуалността на разглежданата тема се дължи на факта, че през последните години в целия свят се наблюдава значително увеличение на броя на хората със затлъстяване. Понастоящем затлъстяването се счита за един от основните фактори, допринасящи за развитието на заболявания, които са основните причини за смъртността сред възрастните. Преди всичко ние говорим заза развитието на захарен диабет тип 2, както и сърдечно-съдови и онкологични заболявания. Увеличаването на теглото с 1 кг увеличава риска от сърдечно-съдови заболявания с 3,1% и диабет с 4,5-9%.
Известно е, че при затлъстяване рискът от развитие на артериална хипертония, фактор, който значително влияе и върху появата на сърдечно-съдови заболявания като инфаркти и инсулти, се утроява в сравнение с хората с нормално телесно тегло. Както е показано в проучването INTERSALT, за всеки 4,5 kg наддаване на тегло, систолното кръвно налягане (BP) се повишава с 4,5 mmHg. Изкуство. .
Затлъстяването като рисков фактор при жени с артериална хипертония, особено в напреднала възраст, се среща по-често, отколкото при мъжете. Една от причините за това е хипоестрогенизмът, който се проявява в периода след менопаузата. Отбелязват се някои особености на разпространението на затлъстяването при различни видове артериална хипертония. По този начин сред по-възрастните жени с изолирана систолна хипертония затлъстяването не е толкова често и няма данни за ефекта от загубата на тегло върху тази категория пациенти. При жени с абдоминално затлъстяване и систоло-диастолични форми на артериална хипертония загубата на тегло е важен моментв контрола на болестта.
При затлъстяването настъпват редица хемодинамични промени, по-специално увеличаване на обема на циркулиращата кръв, ударния обем и сърдечния дебит при относително нормално съдово съпротивление. Смята се, че високото кръвно налягане при пациенти със затлъстяване се дължи главно на повишен сърдечен дебит с "неадекватно нормално" периферно съпротивление.
Това хемодинамично състояние има стимулиращ ефект върху две антагонистични регулаторни системи, които контролират кръвния обем и периферно съпротивление- системата ренин-ангиотензин-алдостерон (RAAS) и системата на сърдечния натриуретичен пептид. Тяхната дисрегулация може до голяма степен да обясни високия сърдечен дебит при пациенти със затлъстяване и хипертония. Освен това, тези сърдечно-съдови регулаторни системи участват в метаболитните промени, свързани с наднорменото телесно тегло при сърдечно-съдови заболявания.
И така, при затлъстяването три основни механизма играят важна роля в патогенезата на артериалната хипертония:
Патогенезата на развитието на артериална хипертония и сърдечно-съдови заболявания при затлъстяване е схематично показана на фигура 1.
Фигура 1. Схема на патогенезата на артериалната хипертония и сърдечно-съдовите заболявания при затлъстяване
Системна и тъканна ренин-ангиотензин-алдостеронова система и нейните промени при затлъстяване
RAAS включва ангиотензиноген, ренин, ангиотензин I, ангиотензин-конвертиращ ензим (ACE) и ангиотензин II (AT II). AT II има разнообразен ефект върху различни клетки, които имат специфични рецептори.
Според класическите концепции ангиотензиногенът се образува в черния дроб и под въздействието на ренин, синтезиран в перигломерулните клетки на бъбреците (юкстагломерулни клетки), ангиотензиногенът се превръща в кръвта в ангиотензин I. ACE е отговорен за разцепването на AT I, което води до образуването на AT II.
Важно е да се отбележи, че при затлъстяването има нарушение на механизмите, регулиращи функционирането на RAAS. При физиологични условия повишената активност на RAAS води до повишена резистентност периферни съдовеи съответно до повишаване на кръвното налягане. Според принципа на обратната връзка повишаването на кръвното налягане трябва да доведе до намаляване на секрецията на ренин, спад на нивата на AT II и намаляване на нивата на алдостерон. Това от своя страна намалява задържането на течности и натрий и поддържа кръвното налягане на нормални нива.
Въпреки това, при пациенти с висцерално затлъстяване, регулирането на нивото на системните циркулиращи компоненти на RAAS е нарушено. Въпреки повишеното кръвно налягане, задържането на натрий и течности, както и увеличаването на обема на циркулиращата кръв, активността на плазмения ренин и алдостерон остава нормална или дори леко повишена. Такава дисрегулация на RAAS при затлъстяване може да бъде следствие от увеличаване на образуването на компоненти на RAAS и/или вторично повишаване на тяхната концентрация поради дефекти в натриуретичната пептидна система.
Установено е, че в допълнение към кръвния RAAS има тъкан, или т.нар. локален RAAS, който е идентифициран в редица тъкани и органи, включително мозъка, сърцето, кръвоносните съдове, бъбреците, тестисите, мастната тъкан и т.н.
Както е известно, два фактора играят ключова роля при образуването на AT II: ренинова активност и концентрация на ангиотензиноген. Синтез и секреция на ангиотензиноген в клетките различни видовене само определя повишаване на локалната концентрация на AT II, но също така повишава системната активност на RAAS. Хроничната инфузия на AT II в мишки беше придружена от значително повишаване на съдържанието на ангиотензиногенна иРНК в адипоцитите. Тези резултати показват наличието на положителна обратна връзка между AT II и ангиотензиногена, където повишаването на нивото на единия агент стимулира образуването на втория. При затлъстяване, особено от висцерален тип, активността на плазмения ренин остава, както вече беше посочено, нормална или леко повишено ниво, и нивата на ангиотензиноген и AT II са повишени.
Структура и физиологични свойства на мастната тъкан
Мастната тъкан съдържа различни видове клетки, включително адипоцити, макрофаги, фибробласти, васкуларни ендотелни клетки и преадипоцити (адипобласти). Последният тип клетки идва от плурипотентни мезодермални стволови клетки. Нови диференцирани („малки”) адипоцити се образуват от преадипоцитите в тялото на възрастния човек. Тези адипоцити се увеличават по размер ("големи" адипоцити) поради повишен хранителен прием мастни киселини. Дълговерижните мастни киселини навлизат в адипоцитите от кръвта и се отлагат под формата на неутрални триацилглицероли. Мастната тъкан е отговорна за съхранението и секрецията на дълговерижни мастни киселини, които действат като един от основните енергийни субстрати за много органи и тъкани, например сърдечните и скелетните мускули. „По-големите“ адипоцити отделят значително повече наситени мастни киселини. Хидролизата на триглицеридите и освобождаването на мастни киселини се извършват под въздействието на вътреклетъчната хормонално-чувствителна липаза, чиято активност се контролира от катехоламини (положителна регулация) и инсулин (отрицателна регулация).
Ендокринна активност на мастната тъкан
За разлика от подкожна мазнина, което обикновено представлява 75% от общата мастна тъкан на тялото и е основното място за съхранение на липиди, висцералната мазнина в момента се счита за активна тъкан, произвеждаща хормони.
Адипоцитите произвеждат широк обхватхормони и цитокини, участващи в метаболизма на глюкоза (адипонектин, резистин и др.), липиди (трансферен протеин на холестерол естер), възпаление (TNF-α, интерлевкин-6), коагулация (инхибитор на плазминогенния активатор-1), регулиране на кръвното налягане (ангиотензиноген, AT II), хранително поведение(лептин), както и повлияване на метаболизма и функционалната активност на различни органи и тъкани, включително мускули, черен дроб, мозък и кръвоносни съдове (виж таблицата).
Таблица. Ендокринна функцияадипоцити: адипоцитокини
| Адипоцитокини | Ефекти на адипоцитокините |
| Лептин | Усвояване на храната, мастна маса |
| Адипонектин | |
| Резистин | Инсулинова резистентност, възпаление |
| Висфатин | Инсулинова резистентност |
| Оментин | Инсулинова резистентност |
| Серпин, освободен от висцерална мастна тъкан (Vaspin) | Инсулинова резистентност |
| Апелин | Вазодилатация |
| Трансферен протеин на холестерил естер (CETP) | Липиден метаболизъм |
| Липопротеинова липаза (LPL) | Липиден метаболизъм |
| Хормонално чувствителна липаза (HSL) | Липиден метаболизъм |
| Протеин-4, свързващ адипоцитни мастни киселини (A-FABP-4 (aP2)) | Липиден метаболизъм |
| Перлипин | Липиден метаболизъм |
| Ренитол свързващ протеин (RBP) | Липиден метаболизъм |
| Протеин, стимулиращ ацилирането (ASP) | Липиден метаболизъм |
| Ангиотензин II (AT II) | Артериално налягане |
| Ангиотензин конвертиращ ензим (ACE) | Артериално налягане |
| Ангиотензиноген (AGT) | Артериално налягане |
| Фактор на туморна некроза алфа (TNF-a) | Възпаление |
| Интерлевкин, 6 (IL-6) | Възпаление |
| С-реактивен протеин (CRP) | Възпаление |
| Адипоцит-трипсин/комплемент фактор D (Адипсин) | Възпаление |
| Макрофаг хемоатрактант протеин-1 (MCP-1) | Атрактант за макрофаги |
| Междуклетъчна адхезионна молекула-1 (ICAM-1) | Активиране на макрофаги |
| Инхибитор на плазминогенния активатор-1 (PAI-1) | Фибринолиза |
Важно е да се подчертае, че дори и малко увеличение на обема висцерална мазнинаиграе важна роля при метаболитни нарушения, регулиране на водно-електролитния баланс и сърдечно-съдови заболявания.
С увеличаване на масата на мастната тъкан се увеличава съдържанието на почти всички адипокини в кръвта. Изключение прави адипонектинът, чието ниво пада при тези условия. Лептинът и адипонектинът са най-изследваните адипокини в момента.
Лептин.Производството на лептин се извършва главно в "големите" адипоцити. Лептинът често се разглежда като сигнална молекула, която медиира връзката между съдържанието на хранителни вещества, влизащи в тялото, състоянието на мастната тъкан и централната нервна система (хипоталамуса). Лептинът повишава липидното окисление в черния дроб, както и липолизата в адипоцитите и скелетни мускули. Инсулинът стимулира образуването на лептин. Нивата на лептин също се влияят от свободни мастни киселини, TNF-α, естрогени и растежен хормон.
Адипонектин.Производството на адипонектин се извършва изключително в адипоцитите. Адипонектинът има разнообразни биологични ефекти - има антиатерогенен ефект, повишава чувствителността на клетките към инсулин, потиска синтеза на глюкоза в черния дроб, засилва нейния транспорт до мускулите, повишава окисляването на мастните киселини. Нивата на адипонектин са намалени при затлъстяване, инсулинова резистентност и диабет тип 2.
Мастна тъкан и активност на RAAS
Оказа се, че мастната тъкан е на второ място след черния дроб по образуване на ангиотензиноген. Например количеството ангиотензиногенна иРНК в адипоцитите е около 70% от нивото в черния дроб. Връзката между нивата на ангиотензиноген, затлъстяването и артериалната хипертония е ясно демонстрирана в експерименти с трансгенни мишки, които експресират излишни количества ангиотензиноген в мастната тъкан. Тези мишки имат висцерално затлъстяване и хипертония. Преадипоцити и диференцирани мастни клеткиимат пълен набор от компоненти, необходими за локалния синтез на AT II, както и AT 1 рецептора за AT II, който осигурява вътреклетъчното предаване на сигнали за активиране, задействани от AT II. При затлъстяване обемът на висцералните диференцирани адипоцити се увеличава 20-30 пъти. Затлъстяването се характеризира с дисфункция на адипоцитите, което се разбира като повишено образуване и секреция на различни адипокини, цитокини, както и увеличаване на съдържанието на компоненти на RAAS, предимно във висцералната мазнина.
Обобщавайки данните от различни проучвания, можем да кажем, че при затлъстяване се наблюдава повишаване на активността на RAAS, което се отразява в следните факти:
Висока активност RAAS от своя страна води до увеличаване на масата на мастната тъкан. По-конкретно, трансгенни мишки, свръхекспресиращи ангиотензиноген само в мастните клетки, показват повишени нива на ангиотензиноген в кръвта, развитие на хипертония и увеличена маса на мастната тъкан. Тъкан AT II по същество функционира като растежен фактор за адипоцитите. AT II, в резултат на ефекта си върху AT 1 рецепторите, предизвиква повишаване на протеина циклин D 1, който участва в регулирането на растежа и деленето на мастните клетки. Доказано е, че AT II индуцира преминаването на G 1 фаза клетъчен цикълв човешки преадипоцити. Този ефект се свързва с ефект върху AT1 рецепторите и последващо активиране на циклин D1-зависима киназа.
Установено е, че AT II предизвиква диференциация на преадипоцитите, активира ключови ензими за образуване на липиди (липогенеза) и увеличава натрупването на триглицериди в адипоцитите.
Висцералното затлъстяване е придружено от повишаване на активността на 11-бета-хидроксистероид дехидрогеназа тип 1, което води до образуването на кортизол, ключов хормон в диференциацията на преадипоцитите в адипоцити.
Активността на тъканната RAS е тясно свързана с производството на адипокини от мастната тъкан. Например, доказано е, че AT II индуцира експресия на лептин в адипоцитите. Предполага се, че такава активност е характерна само за локално синтезиран AT II, за разлика от системния AT II.
Затлъстяване и активност на симпатиковата нервна система
При затлъстяване, особено при коремния му вариант, много често се наблюдава активиране на симпатиковата нервна система. NAS (Normotesive Aging Study) установи увеличение на норепинефрин в урината, пропорционално на индекса на телесна маса. Докато отслабвате, активността на симпатиковата нервна система намалява.
Повишената активност на симпатиковата нервна система при затлъстяване се улеснява от наличието на хиперинсулинемия и инсулинова резистентност. Инсулинът може сам да увеличи активността на симпатоадреналната система, но това може да се дължи отчасти на действието на лептина. Известно е, че с увеличаване на степента на затлъстяване се повишава нивото на лептин на гладно, който се секретира от адипоцитите. Лептинът повишава активността на симпатиковата нервна система, особено в бъбреците. Това води, от една страна, до висока производителност и повишена сърдечна честота, а от друга, до повишена реабсорбция на натрий и увеличаване на вътресъдовия кръвен обем.
Установена е връзка между RAAS и симпатиковата нервна система. Активирането на симпатиковата нервна система е свързано с повишена секреция на ренин в бъбреците и това се случва независимо от интрареналния сензорна системарегулиране на секрецията на ренин от бъбреците. Освен това, увеличаването на цикличния аденозин монофосфат под въздействието на катехоламините стимулира експресията на ангиотензиноген в човешките адипоцити. Увеличаването на нивата на AT II повишава активността на симпатиковата нервна система при хората. Установено е, че AT II активира локалната симпатикова нервна система, която участва в повишаването на телесната температура (термогенеза). Лечението със студ води до повишаване на съдържанието на AT II в адипоцитите без съпътстваща промяна в плазмените нива на AT II.
По този начин дисрегулацията на RAAS при затлъстяване може също да стимулира активността на симпатиковата нервна система.
Методи за фармакологична корекция на високо кръвно налягане при затлъстяване
Приносът на различни патогенетични механизми за поддържане на високо кръвно налягане при затлъстяване може да бъде различен. Следователно антихипертензивните лекарства с много различни механизми на действие могат да имат благоприятен ефект в тази ситуация.
В съответствие със съвременните препоръки за лечение на артериална хипертония, ключът към успеха на значително намаляване на кръвното налягане е използването на комбинирана терапия. При пациенти със затлъстяване, на първо място, основните компоненти на такава терапия трябва да съдържат комбинация от лекарства, които намаляват активността на RAAS (ACE инхибитори и сартани), с лекарства, които намаляват активността на симпатиковата нервна система (β-блокери и недихидропиридинови калциеви антагонисти) и диуретици. Висока ефективностИзползването на лекарства, които блокират RAAS при затлъстяване, е показано в много проучвания. Що се отнася до употребата на β-блокери, данните са много противоречиви, на първо място, като цяло поради съмнения относно тяхната полезност за лечение на пациенти с неусложнена артериална хипертония, и второ, поради факта, че β-блокерите най-малко класическите, могат да увеличат теглото на пациентите и да повишат инсулиновата резистентност. Следователно, ако изберем β-блокери за лечение на пациенти със затлъстяване или метаболитен синдром, тогава това трябва да бъдат лекарства със специални свойства, по-специално карведилол и небиволол.
В същото време беше установено, че недихидропиридиновият калциев антагонист верапамил може не само значително да намали кръвното налягане, но и да намали активността на симпатиковата нервна система.
По този начин, в случай на затлъстяване, комбинация от лекарства, които блокират RAAS и верапамил, може да се използва за лечение на артериална хипертония.
Трябва да се подчертае, че този тип комбинация лекарствасъществува под формата на готова комбинирана доза от- лекарството Tarka, което съдържа мастноразтворим ACEI - трандолаприл и верапамил с бавно освобождаване (verapamil SR). Този подход е много важен за ефективната терапия, тъй като използването на готови лекарствени форми подобрява придържането на пациента към лечението.
Има доказателства, че Tarka в по-голяма степен от всеки от неговите компоненти понижава кръвното налягане, има изразена способност да намалява левокамерната хипертрофия, спомага за нормализиране на ендотелната функция и е метаболитно неутрален дори при пациенти със захарен диабет.
Двойно действие- намаляване на активността на RAAS под влиянието на трандолаприл и симпатиковата нервна система поради удължено действие на верапамил - оказват важен ефект върху патогенетични механизмиразвитието на артериална хипертония при затлъстяване и механизмите, които провокират увреждането на таргетните органи при този тип хипертония.
Особено внимание, когато се обсъжда лечението на хипертония при затлъстяване, трябва да се обърне на факта, че терапията, базирана на комбинация от трандалаприл с дългодействащ верапамил, може да намали риска от развитие на захарен диабет в сравнение с използването на друга тактика на лечение - комбинация сартан с ниска доза тиазиден диуретик. Проучването STAR ясно показва, че когато Tarka се използва в продължение на една година, се развиват по-малко хора с метаболитен синдром, при които абдоминалното затлъстяване е преобладаващо състояние диабет(фиг. 2) .
Фигура 2. Развитие на нови случаи на захарен диабет (глюкоза на гладно > 126 mg/dL или 2-часов тест за глюкозен толеранс > 200 mg/dL) по вид антихипертензивна терапия при лица с метаболитен синдром в проучването STAR

Освен това, според проучването STAR-LET, дори когато захарният диабет се появява на фона лекарствена терапияпрехвърлянето на тези пациенти да приемат лекарството Tarka позволи да се нормализира при половината от пациентите въглехидратния метаболизъм.
Резултатите от тези проучвания ни принуждават да преразгледаме препоръките за лекарствена терапияартериална хипертония при хора с метаболитен синдром и да започне терапия с комбинация, съдържаща АСЕ инхибитор (или сартан) и калциев антагонист, или да прехвърли пациентите на подобна терапия.
Както многократно е споменавано, за лечението на артериалната хипертония важна роля играе намаляването на теглото на пациентите и степента на абдоминално затлъстяване. Разбира се, намаляването на телесното тегло по един или друг начин може да окаже значително влияние върху намаляването на честотата на сърдечно-съдовите заболявания. В момента има различни подходи за лекарствена терапия на затлъстяването. Първият е симптоматично лечение, а именно намаляване на броя на консумираните калории чрез намаляване на усвояването на мазнини от храната. Този подход може да се нарече компенсаторен. Всъщност при такава терапия заболяването не се елиминира (тъй като пациентът продължава да преяжда), а само временно се компенсира от лекарството. Друг подход за лечение на наднорменото тегло и затлъстяването е да се обърне внимание на корена на проблема, а именно хроничното преяждане. Ето как действа сибутрамин (Meridia). Води до бързо засищане и намалява количеството консумирана храна чрез потискане на обратното захващане на норепинефрин и серотонин в синапсите на невронните вериги. Днес Меридиа е единствената оригинално лекарство, премахване на причината за затлъстяването.
Основната разлика между сибутрамин е, че без да причинява намаляване на апетита, той насърчава по-ранното начало на чувство за ситост. Човек се отървава от патологичния навик на преяждане, което води до постепенно и устойчиво намаляване на телесното тегло. Под въздействието на сибутрамин консумацията на храна се намалява с приблизително 20%. В допълнение, сибутрамин косвено влияе върху нивото на биогенните амини в кръвта, които активират адренергичните рецептори в мастната тъкан и инициират липолизата в адипоцитите, което е придружено от промяна в съдържанието на енергийни субстрати в кръвта. Сибутрамин, благодарение на активирането на β2- и β3-адренергичните рецептори, подобрява процесите на термогенеза и увеличава потреблението на енергия в организма.
Клиничната ефикасност и безопасност на сибутрамин (Meridia) са доказани в големи количествамногоцентрови изследвания. По-специално, в проучването STORM (Sibutramine Trial on Obesity Reduction and Maintenance), включващо 605 пациенти със затлъстяване, беше показано, че двугодишната употреба на сибутрамин намалява теглото на пациентите 3 пъти, а обиколката на талията - 2 пъти по-изразено. отколкото плацебо.. Важно е, че 80% от пациентите поддържат загубата на тегло в продължение на две години, в сравнение с 16% от пациентите, получаващи плацебо (p< 0,001). Показательно, что при этом улучшался липидный спектр: уровень липопротеидов висока плътностсе увеличава с 21% с намаляване на нивата на липопротеините с ниска плътност и триглицеридите.
Благоприятният ефект от загубата на тегло при лечението на пациенти с артериална хипертония и други сърдечно-съдови заболявания може да се дължи и на факта, че намаляването на интраабдоминалната мазнина може да намали механичното притискане на бъбреците, което може да доведе до подобрено кръвоснабдяване на бъбреците и намаляване на активността на RAAS. Намаляването на мастната тъкан в и около бъбреците може да доведе до намалено интерстициално налягане, компресия на тънката част от примката на Henley, повишен кръвен поток във vasa recta и намалена тубулна реабсорбция на Na+ и вода. По този начин загубата на тегло поради нелекарствени или лекарствени методи за корекция може да намали кръвното налягане.
Доскоро обаче реално клинична практикасибутрамин се използва с повишено внимание, опасявайки се, че е възможно отрицателно влияниевърху кръвното налягане и сърдечната честота, което от своя страна може да доведе, макар и при малък брой пациенти, до неприятни субективни усещания. За изследване на ефекта на сибутрамин върху сърдечно-съдовата система и доказване на безопасността на лекарството при група пациенти с повишен риск от сърдечно-съдови заболявания, широкомащабно многоцентрово, двойно-сляпо, плацебо-контролирано международно проучване SCOUT (Sibutramine Cardiovascular OUTcomes), беше започнато, където бяха наблюдавани 10 742 пациенти, от които 97% имаха заболявания на сърдечно-съдовата система, 88 - артериална хипертония и 84% - захарен диабет тип 2. Въз основа на резултатите от първия завършен етап на изследването беше установено, че приложението на сибутрамин води до значително (p< 0,001) уменьшению веса (медиана изменения составила 2,2 кг), окружности талии (на 2 см в равной степени выраженному у мужчин и женщин) и снижению АД систолического на 3,0 мм рт. ст. и диастолического - на 1,0 мм рт. ст. Частота сердечных сокращений увеличивалась в среднем на 1,5 удара в минуту. Увеличение АД и увеличение частоты пульса наблюдалось соответственно у 4,7 и 3,5% пациентов. Таким образом, в данном исследовании было показано, что даже у пациентов, относящихся к группам высокого риска, применение сибутрамина (препарата Меридиа) было высокоэффективным и безопасным . Дальнейший анализ данных исследования SCOUT позволил установить, что у пациентов с артериальной гипертонией снижение АД при приеме сибутрамина было более выраженным и составило в среднем для систолического АД -6,5 (-27,0; 8,0) мм рт. ст., а для диастолического -2,0 (-15,0; 8,0) мм рт. ст. (p < 0,001). Среди пациентов, у которых снижение веса не было выраженным, снижение АД было достоверным, но менее выраженным, чем у лиц с успешным снижением веса, и составило в среднем для систолического -3,5 (-26,0; 10,0) мм рт. ст. и -1,5 (-16,0; 9,0) мм рт. ст. для диастолического АД (p < 0,001). У лиц с нормальным АД было достоверное, но не выраженное увеличение АД - 1,5 (-15,0; 19,5) мм рт. ст. систолического и на 1,0 (-10,5; 13,0) мм рт. ст. диастолического АД (p < 0,001). Степень повышения АД при приеме сибутрамина уменьшалась в соответствии со степенью потери веса .
Възниква естествен въпрос как този или онзи тип антихипертензивна терапия ще се свърже с лечението със сибутрамин. Проведени са няколко проучвания, за да се отговори на този въпрос. Например, беше показано, че употребата на комбинирана лекарствена форма, съдържаща верапамил 180 mg/трандолаприл 2 mg в комбинация със сибутрамин 10 mg, води до по-изразено понижение на кръвното налягане в продължение на 6 месеца, отколкото антихипертензивната терапия самостоятелно - систолното кръвно налягане се понижава, съответно с 21,9 ± 8,1 спрямо 15,9 ± 12,3 mm Hg. Изкуство. и диастолното - с 15,7 ± 8,1 срещу 9,1 ± 9,9 mm Hg. Изкуство. (р = 0,03). Комбинираната терапия също води до по-изразено подобрение на антропометричните параметри; надежден (стр<5) по сравнению с исходным уровнем снижение малых липопротеидов низкой плотности, С-реактивного белка и висфатина наблюдалось только в группе пациентов, получавших комбинированную терапию сибутрамином с антигипертензиным препаратом Тарка .
Проучването HOS (хипертония-затлъстяване-сибутрамин) е 16-седмично, проспективно, многоцентрово, плацебо-контролирано, двойно-сляпо проучване, сравняващо различни антихипертензивни режими (фелодипин 5 mg/рамиприл 5 mg (n = 57), верапамил 180 mg/ трандолаприл 2 mg (n = 55), метопролол сукцинат 95 mg/хидрохлоротиазид 12,5 mg n = 59), когато е предписан сибутрамин и плацебо. Това проучване потвърди, че сибутрамин може да повиши кръвното налягане. Следователно, разбира се, е необходима адекватна антихипертензивна терапия по време на употребата на сибутрамин при пациенти с артериална хипертония. Доказано е също, че при лечение с комбинация от β-блокер и хидрохлоротиазид, положителните ефекти на сибутрамин по отношение на загуба на тегло, обиколка на талията и ефект върху метаболитния профил са значително по-слабо изразени, отколкото когато се комбинира с комбинирана терапия с ACE инхибитори и калциеви антагонисти със сибутрамин. Това още веднъж потвърждава необходимостта от внимателен подбор на антихипертензивна терапия при пациенти със затлъстяване, особено при провеждане на програми, насочени към намаляване на теглото. И в заключение трябва да се отбележи, че от наша гледна точка един от съществените проблеми, които намаляват ефективността на борбата със затлъстяването, е, че нито лекарите, нито населението считат затлъстяването за значим рисков фактор. Освен това пациентите често не се оценяват като затлъстели. Например, в проучването POLONESE, според оценката на лекарите, базирана на изчисленията на ИТМ, затлъстяването при мъжете и жените е регистрирано три пъти по-често, отколкото според самооценката на пациентите. По този начин трябва да се засили и да се проведе разяснителна работа сред населението за необходимостта от предотвратяване на наддаване на тегло, коригиране на съществуващото затлъстяване и значението на постоянното лечение на артериалната хипертония. ЛИТЕРАТУРА
1. Флегал К.М., Карол М.Д., Огдън К.К., Джонсън К.Л. Разпространение и тенденции в затлъстяването сред възрастните в САЩ, 1999-2000 г. JAMA 2002; 288:1723-7.
2. Pi-Sunyer F.X. Епидемиологията на централното разпределение на мазнините във връзка с болестта. Nutr Rev 2004; 62 (7): 120-6.
3. Arbeeny C.M. Справяне с неудовлетворената медицинска нужда от безопасни и ефективни терапии за отслабване. Obes Res 2004; 12(8): 1191-6.
4. Stamler J., Rose G., Stamler R. и др. Резултати от проучването INTERSALT. Последици за общественото здраве и медицинските грижи. Хипертония 1989; 14(5): 570-7.
5. Jedrychowski W., Mroz E., Bojanczyk M., Jedrychowska I. Наднормено тегло и хипертония при възрастните хора - резултатите от проучването на общността. Arch Gerontol Geriatr 1991; 13 (1): 61-9.
6. Канай Х., Токунага К., Фуджиока С. и др. Намаляването на интраабдоминалната висцерална мазнина може да намали кръвното налягане при затлъстели жени с хипертония. Хипертония 1996; 27 (1): 125-9.
7. Poirier P., Giles T.D., Bray G.A., et al. Американска сърдечна асоциация; Комитет по затлъстяването към Съвета по хранене, физическа активност и метаболизъм. Затлъстяване и сърдечно-съдови заболявания: патофизиология, оценка и ефект от загуба на тегло: актуализация на научната декларация на Американската сърдечна асоциация от 1997 г. относно затлъстяването и сърдечните заболявания от Комитета по затлъстяването към Съвета по хранене, физическа активност и метаболизъм. Тираж 2006; 113:898-918.
8. Алперт М.А. Кардиомиопатия при затлъстяване; патофизиология и еволюция на клиничния синдром. Am J Med Sci 2001; 321: 225-36.
9. Aneja A., El-Atat F., McFarlane S.I., Sowers J.R. Хипертония и затлъстяване. Последни Progr Horm Res 2004; 59: 169-205.
10. Engeli S., Sharma A.M. Системата ренин-ангиотензин и натриуретичните пептиди при хипертония, свързана със затлъстяването. J Mol Med 2001; 79: 21-9.
11. Lafontan M., Moro C., Sengenes C. и др. Неподозирана метаболитна роля за предсърдните натриуретични пептиди: контрол на липолизата, мобилизацията на липидите и системните нива на неестерифицирани мастни киселини при хора. Arterioscler Thromb Vasc Biol 2005; 25: 2032-42.
12. Хол Й.Е. Бъбреци, хипертония и затлъстяване. Хипертония 2003; 41(3): 625-33.
13. Купър Р., Макфарлейн Андерсън Н., Бенет Ф. И. и др. ACE, ангиотензиноген и затлъстяване: потенциален път, водещ до хипертония. J Hum Hypertens 1997; 11: 107-11.
14. Lu N., Boustany-Kari C.M., Daugherty A., Cassis L.A. Ангиотензин II повишава експресията на адипозен ангиотензиноген. Am J Physiol Endocrinol Metab 2007; 292: 1280-7.
15. Енгели С., Негрел Р., Шарма А.М. Физиология и патофизиология на ренин-ангиотензиновата система на мастната тъкан. Хипертония 2000; 35(6): 1270-7.
16. Otto T.C., Lane M.D. Развитие на мастна тъкан: от стволова клетка до адипоцит. Crit Rev Biochem Mol Biol 2005; 40: 229-42.
17. Hajer G.R., van Haeften T.W., Visseren F.L.J. Дисфункция на мастната тъкан при затлъстяване, диабет и съдови заболявания. Eur Heart J 2008; 29: 2959-71.
18. Wannathee S.G., Lowe G.D., Rumley A., et al. Адипокини и риск от диабет тип 2 при възрастни мъже. Diabetes Core 2007; 30: 1200-5.
19. Chu N.F., Spiegelman D., Hotamisligil G.S., et al. Нивата на плазмен инсулин, лептин и разтворими TNF рецептори във връзка със свързаните със затлъстяването атерогенни и тромбогенни рискови фактори за сърдечно-съдови заболявания сред мъжете. Атеросклероза 2001; 157: 495-503.
20. Skurk T., Alberti-Huber C., Herder C., Hauner H. Връзка между размера на адипоцитите и експресията и секрецията на адипокин. J Clin Endocrinol Metab 2007; 6(92): 1023-33.
21. Ran J, Hirano T, Fukui T, et al. Инфузията на ангиотензин II намалява плазменото ниво на адипонектин чрез неговия рецептор тип 1 при плъхове: следствие за свързаната с хипертония инсулинова резистентност. Метаболизъм 2006; 55: 478-88.
22. Considine R.V., Sinha M.K., Heiman M.L., et al. Серумна концентрация на имунореактивен лептин при хора с нормално тегло и затлъстяване. N Engl J Med 1996; 334:292-5.
23. Schwartz M.W., Woods S.C., Porte D. Jr., et al. Централната нервна система контролира приема на храна. Nature 2000; 404 (6778): 661-71.
24. Cheung C.C., Clifton D.K., Steiner R.A. Проопиомеланокортиновите неврони са директни мишени за лептрин в хипоталамуса. Ендокринология 1997; 138; 4489-92.
25. Long Y.C., Zierath J.R. AMP-активирана протеин киназна сигнализация в метаболитната регулация. J Clin Invest 2006; 116: 1776-83.
26. Saladin R., De Vos P., Guerre-Millo M. и др. Преходно повишаване на генната експресия на затлъстяване след прием на храна или приложение на инсулин. Nature 1995; 377:527-9.
27. Zhang H.H., Kumar S., Barnet A.H., Eggo M.C. Факторът на туморна некроза-алфа упражнява двойни ефекти върху синтеза и освобождаването на човешки адипозен лептин. Mol Cell Endocrinol 2000; 159: 79-88.
28. Линдзи Р. С., Фунахаши Т., Хансън Р. Л. и др. Адипонектин и развитие на диабет тип 2 в индийското население на Пима. Lancet 2002; 360: 57-8.
29. Hajer G.R., van der Graaf Y., Olijhoek J.K., et al. Ниските плазмени нива на адипонектин са свързани с нисък риск от бъдещи сърдечно-съдови събития при пациенти с клинично очевидно съдово заболяване. Am Heart J 2007; 154 (750): 1-7.
30. Massiera F., Bloch-Faure M., Ceiler D., et al. Адипозният ангиотензиноген участва в растежа на мастната тъкан и регулирането на кръвното налягане. FASEB J 2001; 15: 2727-9.
31. Paul M., Mehr A.P., Kreutz R. Физиология на локалните системи ренин-ангиотензин. Physiol Rev 2006; 86: 747-803.
32. Karlsson C., Lindell K., Ottosson M., et al. Човешката мастна тъкан експресира ангиотензиноген и ензими, необходими за превръщането му в ангиотензин II. J Clin Endocrinol Metab 1998; 83: 3925-9.
33. Gorzelniak K., Engeli S., Janke J., et al. Хормонална регулация на ренин-ангиотензиновата система на човешката мастна тъкан: връзка със затлъстяването и хипертонията. J Hypertens 2002; 20: 965-73.
34. Engeli S., Gorzelniak K., Kreutz R., et al. Ко-експресия на гени на системата ренин-ангиотензин в човешка мастна тъкан. J Hypertens 1999; 17: 555-60.
35. Achard V., Boullu-Ciocca S., Desbrière R., et al. Експресия на ренинов рецептор в човешка мастна тъкан. Am J Physiol Regul Integr Comp Physiol 2007; 292: 274-82.
36. Sarzani R., Savi F., Dessi-Fulgheri P., Rappelli A. Ренин-ангиотензинова система, натриуретични пептиди, затлъстяване, метаболитен синдром и хипертония: интегриран изглед при човека. J Hypertens 2008; 26: 831-43.
37. Crandall D.L., Armellino D.C., Busler D.E., et al. Ангиотензин II рецептори в човешки преадипоцити: роля в регулирането на клетъчния цикъл. Ендокринология 1999; 140: 154-8.
38. Saint-Marc P., Kozak L.P., Ailhaud G., et al. Ангиотензин II като трофичен фактор на бялата мастна тъкан: стимулиране на образуването на мастни клетки. Ендокринология 2001; 142: 487-92.
39. Watanabe G., Lee R. J., Albanese C., et al. Ангиотензин II активиране на циклин D1-зависима киназна активност. J Biol Chem 1996; 271:22570-7.
40. Darimont C., Vassaux G., Ailhaud G., Negrel R. Диференциация на преадипозни клетки: паракринна роля на простациклин при стимулиране на мастни клетки от ангиотензин-II. Ендокринология 1994; 135:2030-6.
41. Jones B.H., Standridge M.K., Moustaid N. Ангиотензин II повишава липогенезата в 3T3-L1 и човешките мастни клетки. Ендокринология 1997; 138: 1512-9.
42. Wake D.J., Walker B.R. Инхибиране на 11бета-хидроксистероид дехидрогеназа тип 1 при затлъстяване. Ендокринна 2006; 29: 101-8.
43. Engeli S., Bohnke J., Feldpausch M., et al. Регулиране на 11beta-HSD гени в човешката мастна тъкан: влияние на централното затлъстяване и загуба на тегло. Obes Res 2004; 12:9-17.
44. Kim S., Whelan J., Claycombe K., et al. Ангиотензин II повишава секрецията на лептин от 3T3-L1 и човешките адипоцити чрез простагландин-независим механизъм. J Nutr 2002; 132: 1135-40.
45. Cassis L.A., English V.L., Bharadwaj K., Boustany C.M. Диференциални ефекти на локалния спрямо системния ангиотензин II при регулирането на освобождаването на лептин от адипоцитите. Ендокринология 2004; 145: 169-74.
46.Mancia G., Bousquet P., Elghozi J.L., et al. Симпатиковата нервна система и метаболитен синдром. J Hypertens 2007; 25: 909-20.
47. Tentolouris N., Liatis S., Katsilambros N. Активност на симпатиковата система при затлъстяване и метаболитен синдром. Ann N Y Acad Sci 2006; 1083: 129-52.
48. Landsberg L., Troisi R., Parker D. и др. Затлъстяване, кръвно налягане и симпатикова нервна система. Ann Epidemiol 1991; 1: 295-303.
49. Serazin V., Dos Santos E., Morot M., Giudicelli Y. Експресията и секрецията на човешки адипозен ангиотензиногенен ген се стимулират от цикличен AMP чрез повишена активност на свързване на елемент, отговарящ на ДНК цикличен AMP. Ендокринна 2004; 25: 97-104.
50. Касис Л.А. Роля на ангиотензин II в термогенезата на кафявата мастна тъкан по време на студена аклиматизация. Am J Physiol Endocrinol Metab 1993; 265:860-5.
51. Cassis L.A., Dwoskin L.P. Пресинаптична модулация на освобождаване на невротрансмитери от ендогенен ангиотензин II в кафява мастна тъкан. J Neural Transm 1991; 34: 129-37.
52. Reisin E., Weir M., Falkner B., et al. Лизиноприл срещу хидрохлоротиазид при пациенти с хипертония със затлъстяване: многоцентрово плацебо-контролирано проучване. Проучвателна група за лечение на пациенти със затлъстяване и хипертония (TROPHY). Хипертония 1997; 30(1): 2140-5.
53. Neutel J.M., Saunders E., Bakris G.L., et al. Ефикасността и безопасността на фиксирани комбинации с ниски и високи дози ирбесартан/хидрохлоротиазид при пациенти с неконтролирано систолично кръвно налягане при монотерапия: проучването INCLUSIVE. J Clin Hypertens (Гринуич) 2005; 7(10): 578-86.
54. Беленков Ю.Н., Чазова И.Е., Мичка В.Б. от името на изследователската група за IVF. Многоцентрово, рандомизирано, отворено проучване, изследващо ефективността на промените в начина на живот и терапията с АСЕ инхибитори (квинаприл) при пациенти със затлъстяване и артериална хипертония (IVF). Артериална хипертония 2003; 9(6): 3-6.
55. Джейкъб С., Рет К., Хенриксен Е. Дж. Антихипертензивна терапия и инсулинова чувствителност: трябва ли да предефинираме ролята на бета-блокерите? Am J Hypertens 1998; 11(10): 1258-65.
56. Kaaja R, Kujala S, Manhem K, et al. Ефекти от симпатиколитичната терапия върху индексите на инсулиновата чувствителност при жени с хипертония след менопауза. Int J Clin Pharmacol Ther 2007; 45 (7): 394-401.
57. Kuperstein R., Sasson Z. Ефекти от антихипертензивната терапия върху метаболизма на глюкозата и инсулина и върху масата на лявата камера: рандомизирано, двойно-сляпо, контролирано проучване на 21 хипертоници със затлъстяване. Тираж 2000 г.; 102 (15): 1802-6.
58. Халперин A.K., Cubeddu L.X. Ролята на блокерите на калциевите канали при лечението на хипертония. Am Heart J 1986; 111 (2): 363-82.
59. Макалистър Р.Г. мл. Клинична фармакология на агенти, блокиращи бавни канали. Prog Cardiovasc Dis 1982; 25 (2): 83-102.
60. Binggeli C., Corti R., Sudano I., et al. Ефекти от хроничната блокада на калциевия канал върху активността на симпатиковия нерв при хипертония. Хипертония 2002; 39(4): 892-6.
61. Lefrandt J.D., Heitmann J., Sevre K., et al. Ефектите на класовете дихидропиридин и фенилалкиламин калциев антагонист върху автономната функция при хипертония: проучването VAMPHYRE. Am J Hypertens 2001; 14(11): 1083-9.
62. Wanovich R., Kerrish P., Gerbino P.P., Shoheiber O. Модели на съответствие на пациенти, лекувани с 2 отделни антихипертензивни средства спрямо комбинирана терапия с фиксирана доза Am J Hypertens 2004; 175:223.
63. Дезии Ц.М. Ретроспективно проучване на постоянството при комбинирана терапия с едно хапче срещу. едновременна терапия с две таблетки при пациенти с хипертония. Управлявайте грижата. 2000 г.; 9(9): 2-6.
64. Gerbino P.P., Shoheiber O. Модели на придържане сред пациенти, лекувани с комбинация с фиксирана доза спрямо отделни антихипертензивни средства. Am J Health Syst Pharm 2007; 64(12): 1279-83.
65. Jackson K. Устойчивост на фиксирана срещу свободна комбинация с валсартан и HCTZ при пациенти с хипертония. Value Health Suppl 2006; 9:363.
66. Aepfelbacher F.C., Messerli F.H., Nunez E., Michalewicz L. Сърдечно-съдови ефекти на комбинация трандолаприл/верапамил при пациенти с лека до умерена есенциална хипертония. Am J Cardiol 1997; 79(6): 826-8.
67. Reynolds N.A., Wagstaff A.J., Keam S.J. Trandolapril/verapamil с продължително освобождаване: преглед на употребата му при лечението на есенциална хипертония. Наркотици 2005; 65 (13): 1893-914.
68. Sharma S.K., Ruggenenti P., Remuzzi G. Управление на хипертонията при пациенти с диабет - фокус върху комбинацията trandolapril/verapamil. Vasc Health Risk Manag 2007; 3(4): 453-65.
69. Bakris G., Molitch M., Hewkin A., et al. Разлики в глюкозния толеранс между комбинации от антихипертензивни лекарства с фиксирани дози при хора с метаболитен синдром. Грижа за диабета 2006; 29(12): 2592-7.
70. Bakris G., Molitch M., Zhou Q., et al. Възстановяване на свързания с диуретици нарушен глюкозен толеранс и нововъзникнал диабет: резултати от проучването STAR-LET. J Cardiometab Syndrome 2008; 3 (1): 18-25.
71. Bailey C.J., Ден C. Нови фармакологични подходи към затлъстяването. Практика при затлъстяване 2005; 1:2-5.
72. Яновски С.З., Яновски Я.А.Й. затлъстяване. N Engl J Med 2002; 346 (8): 591-602.
73. Ден C., Бейли C.J. Сибутрамин актуализация. Br J Diabet Vasc Dis 2002; 2: 392-7.
74. James W.P., Astrup A., Finer N., et al. Ефект на сибутрамин върху поддържането на тегло след загуба на тегло: рандомизирано проучване. Проучвателна група STORM. Изпитване със сибутрамин за намаляване и поддържане на затлъстяването. Lancet 2000; 356:2119-25.
75. Torp-Pedersen C., Caterson I., Coutinho W., et al. Сърдечно-съдови реакции към управление на теглото и сибутрамин при високорискови субекти: анализ от проучването SCOUT. Eur Heart J 2007; 28(23): 2915-23.
76. Sharma A.M., Caterson I.D., Coutinho W., et al. Промени в кръвното налягане, свързани със сибутрамин и управление на теглото - анализ от 6-седмичния начален период на проучването за сърдечно-съдови резултати със сибутрамин (SCOUT). Diabetes Obes Metab 2008. doi 10.1111/J.1463-1326.2008.00930.
77. Nakou E., Filippatos T.D., Liberopoulos E.N., et al. Ефекти на комбинацията сибутрамин плюс верапамил със забавено освобождаване/трандолаприл върху кръвното налягане и метаболитните променливи при пациенти с хипертония със затлъстяване. Expert Opin Pharmacother 2008; 9(10): 1629-39.
78. Scholze J., Grimm E., Herrmann D., et al. Оптимално лечение на хипертония, свързана със затлъстяването: проучването Hypertension-Obesity-Sibutramine (HOS). Тираж 2007; 115 (15): 1991-8.
79. Глезер М.Г. Резултати от руското проучване POLONESE (Ефикасност и безопасност на енаренала при пациенти с артериална хипертония). Терапевтичен архив 2006; 4: 44-50.
За оферта:Леонова М.В. Нови и обещаващи лекарства, които блокират системата ренин-ангиотензин-алдостерон // Рак на гърдата. Медицински преглед. 2013. № 17. С. 886
Ролята на системата ренин-ангиотензин-алдостерон (РААС) в развитието на артериалната хипертония (АХ) и други сърдечно-съдови заболявания понастоящем се счита за доминираща. В сърдечно-съдовия континуум хипертонията е сред рисковите фактори, а основният патофизиологичен механизъм на увреждане на сърдечно-съдовата система е ангиотензин II (ATII). ATII е ключов компонент на RAAS - ефектор, който осъществява вазоконстрикция, задържане на натрий, активиране на симпатиковата нервна система, клетъчна пролиферация и хипертрофия, развитие на оксидативен стрес и възпаление на съдовата стена.
В момента два класа лекарства, които блокират RAAS, вече са разработени и широко използвани клинично - ACE инхибитори и ATII рецепторни блокери. Фармакологичните и клиничните ефекти на тези класове се различават. ACE е пептидаза от групата на цинковите металопротеинази, която метаболизира ATI, AT1-7, брадикинин, субстанция Р и много други пептиди. Механизмът на действие на АСЕ инхибиторите е свързан главно с предотвратяването на образуването на ATII, което насърчава вазодилатацията, натриурезата и елиминира провъзпалителните, пролиферативните и други ефекти на ATII. Освен това АСЕ инхибиторите предотвратяват разграждането на брадикинина и повишават нивата му. Брадикининът е мощен вазодилататор, потенцира натриурезата и най-важното е, че има кардиопротективен ефект (предотвратява хипертрофия, намалява исхемичното увреждане на миокарда, подобрява коронарното кръвоснабдяване) и вазопротективен ефект, подобрявайки ендотелната функция. В същото време високото ниво на брадикинин е причина за развитието на ангиоедем, което е един от сериозните недостатъци на АСЕ инхибиторите, които значително повишават нивото на кинините.
АСЕ инхибиторите не винаги са в състояние напълно да блокират образуването на ATII в тъканите. Сега е установено, че други ензими, които не са свързани с АСЕ, също могат да участват в неговата трансформация в тъканите, предимно ендопептидази, които не се повлияват от АСЕ инхибиторите. В резултат на това АСЕ инхибиторите не могат напълно да премахнат ефектите на ATII, което може да е причината за тяхната липса на ефективност.
Решението на този проблем беше улеснено от откриването на ATII рецептори и първия клас лекарства, които селективно блокират AT1 рецепторите. Чрез AT1 рецепторите се реализират неблагоприятните ефекти на ATII: вазоконстрикция, секреция на алдостерон, вазопресин, норепинефрин, задържане на течности, пролиферация на гладкомускулни клетки и кардиомиоцити, активиране на SAS, както и механизъм за отрицателна обратна връзка - образуването на ренин . AT2 рецепторите изпълняват "полезни" функции, като вазодилатация, процеси на възстановяване и регенерация, антипролиферативни ефекти, диференциация и развитие на ембрионални тъкани. Клиничните ефекти на ATII рецепторните блокери се медиират чрез елиминиране на "вредните" ефекти на ATII на ниво AT1 рецептори, което осигурява по-пълно блокиране на неблагоприятните ефекти на ATII и увеличаване на влиянието на ATII върху AT2 рецепторите , което допълва съдоразширяващия и антипролиферативния ефект. ATII рецепторните блокери имат специфичен ефект върху RAAS, без да се намесват в кининовата система. Липсата на влияние върху активността на кининовата система, от една страна, намалява тежестта на нежеланите реакции (кашлица, ангиоедем), но, от друга страна, лишава ATII рецепторните блокери от важен антиисхемичен и вазопротективен ефект, което ги отличава от АСЕ инхибиторите. Поради тази причина показанията за употреба на ATII рецепторни блокери в голяма степен повтарят показанията за употреба на АСЕ инхибитори, което ги прави алтернативни лекарства.
Въпреки въвеждането на блокерите на RAAS в широко разпространената практика при лечението на хипертония, проблемите за подобряване на резултатите и прогнозата остават. Те включват: възможността за подобряване на контрола на кръвното налягане в популацията, ефективността на лечението на резистентна хипертония и възможността за допълнително намаляване на риска от сърдечно-съдови заболявания.
Търсенето на нови начини за въздействие върху RAAS продължава активно; Проучват се други тясно взаимодействащи системи и се създават лекарства с множество механизми на действие, като инхибитори на АСЕ и неутрална ендопептидаза (NEP), ендотелин-конвертиращ ензим (ACE) и инхибитори на NEP, инхибитори на ACE/NEP/EGT.
Вазопептидазни инхибитори
В допълнение към добре познатия АСЕ, вазопептидазите включват още две цинкови металопротеинази - неприлизин (неутрална ендопептидаза, NEP) и ендотелин-конвертиращ ензим, които също могат да бъдат мишени за фармакологично действие.
Неприлизин е ензим, произвеждан от съдовия ендотел и участващ в разграждането на натриуретичния пептид, както и на брадикинина.
Натриуретичната пептидна система е представена от три различни изоформи: предсърден натриуретичен пептид (А-тип), мозъчен натриуретичен пептид (В-тип), които се синтезират в атриума и миокарда, и ендотелен С-пептид, които по своите биологични функции са ендогенни инхибитори на RAAS и ендотелин-1 (Таблица 1). Сърдечно-съдовите и бъбречните ефекти на натриуретичния пептид включват понижаване на кръвното налягане чрез ефекта му върху съдовия тонус и водно-електролитния баланс, както и антипролиферативни и антифиброзни ефекти върху целевите органи. Най-новите доказателства сочат, че натриуретичната пептидна система участва в метаболитната регулация: окисляване на липидите, образуване и диференциация на адипоцити, активиране на адипонектин, инсулинова секреция и въглехидратен толеранс, което може да осигури защита срещу развитието на метаболитен синдром.
Сега стана известно, че развитието на сърдечно-съдови заболявания е свързано с дисрегулация на натриуретичната пептидна система. По този начин при хипертония има дефицит на натриуретичен пептид, водещ до чувствителност към сол и нарушена натриуреза; при хронична сърдечна недостатъчност (CHF), на фона на дефицит, се наблюдава ненормално функциониране на хормоните на натриуретичната пептидна система.
Следователно, за потенциране на натриуретичната пептидна система, за да се постигнат допълнителни хипотензивни и защитни кардиоренални ефекти, е възможно да се използват NEP инхибитори. Инхибирането на неприлизин води до потенциране на натриуретичния, диуретичния и вазодилататорния ефект на ендогенния натриуретичен пептид и в резултат на това до понижаване на кръвното налягане. Въпреки това, NEP също участва в разграждането на други вазоактивни пептиди, по-специално ATI, ATII и ендотелин-1. Следователно, балансът на ефектите на инхибиторите на NEP върху съдовия тонус е променлив и зависи от преобладаването на констрикторните и дилататорните ефекти. При продължителна употреба антихипертензивният ефект на инхибиторите на неприлизин е слаб поради компенсаторно активиране на образуването на ATII и ендотелин-1.
В тази връзка, комбинацията от ефектите на АСЕ инхибиторите и NEP инхибиторите може значително да потенцира хемодинамичните и антипролиферативните ефекти в резултат на комплементарния механизъм на действие, което доведе до създаването на лекарства с двоен механизъм на действие, наричани общо вазопептидаза инхибитори (Таблица 2, Фиг. 1).
Известните вазопептидазни инхибитори се характеризират с различна степен на селективност за NEP/ACE: омапатрилат - 8.9:0.5; фасидоприлат - 5.1:9.8; Сампатрилат - 8,0:1,2. В резултат на това вазопептидазните инхибитори са придобили много по-голям потенциал за постигане на хипотензивен ефект, независимо от активността на RAAS и нивото на задържане на натрий, както и в органната защита (регресия на хипертрофия, албуминурия, съдова скованост). Най-изследван в клиничните проучвания е омапатрилат, който показва по-висока антихипертензивна ефикасност в сравнение с АСЕ инхибиторите и при пациенти със ЗСН води до увеличаване на фракцията на изтласкване и подобрени клинични резултати (IMPRESS, OVERTURE проучвания), но без предимства пред АСЕ инхибиторите.
Въпреки това, в големи клинични проучвания, използващи омапатрилат, е установена по-висока честота на ангиоедем в сравнение с АСЕ инхибиторите. Известно е, че честотата на ангиоедем при използване на АСЕ инхибитори варира от 0,1 до 0,5% в популацията, от които 20% от случаите са животозастрашаващи, което е свързано с многократно повишаване на концентрациите на брадикинин и неговите метаболити. Резултатите от голямото многоцентрово проучване OCTAVE (n = 25 302), което е специално предназначено за изследване на честотата на ангиоедем, показаха, че честотата на този страничен ефект по време на лечение с омапатрилат надвишава тази в групата на еналаприл - 2,17% срещу 0,68% ( относителен риск 3.4) . Това се обяснява с повишения ефект върху нивата на кинин със синергично инхибиране на ACE и NEP, свързано с инхибиране на аминопептидаза Р, която участва в разграждането на брадикинин.
Нов двоен вазопептидазен инхибитор, който блокира ACE/NEP, е илепатрил, който има по-висок афинитет към ACE в сравнение с NEP. При изследване на фармакодинамичните ефекти на илепатрил върху активността на RAAS и натриуретичния пептид при здрави доброволци беше установено, че лекарството зависи от дозата (в дози от 5 и 25 mg) и значително (повече от 88%) потиска ACE в кръвна плазма за повече от 48 часа, независимо от чувствителността към сол. В същото време лекарството значително повишава активността на плазмения ренин в рамките на 48 часа и намалява нивата на алдостерон. Тези резултати показват изразено и по-дълготрайно потискане на RAAS за разлика от АСЕ инхибитора рамиприл в доза от 10 mg, което се обяснява с по-значимия тъканен ефект на илепатрил върху АСЕ и по-големия афинитет към АСЕ и сравнима степен на блокадата на RAAS в сравнение с комбинацията от 150 mg ирбесартан + 10 mg рамиприл. За разлика от ефекта върху RAAS, ефектът на илепатрил върху натриуретичния пептид се проявява чрез краткотрайно повишаване на нивото на неговата екскреция в периода 4-8 часа след приема на доза от 25 mg, което показва по-ниска и по-слаб афинитет към NEP и го отличава от omapatrilat. Освен това, по отношение на нивото на екскреция на електролити, лекарството няма допълнителен натриуретичен ефект в сравнение с рамиприл или ирбесартан, както и други вазопептидазни инхибитори. Максималният хипотензивен ефект се развива 6-12 часа след приема на лекарството, а понижението на средното кръвно налягане е 5±5 и 10±4 mmHg. съответно при ниска и висока чувствителност към сол. Според фармакокинетичните характеристики илепатрил е пролекарство с активен метаболит, който се образува бързо, достигайки максимална концентрация след 1-1,5 часа и бавно се елиминира. В момента се провеждат клинични изпитвания фаза III.
Алтернативен път за двойно потискане на RAAS и NEP е представен от комбинация от ATII и NEP рецепторна блокада (фиг. 2). ATII рецепторните блокери не повлияват метаболизма на кинините, за разлика от АСЕ инхибиторите, и следователно потенциално имат по-нисък риск от развитие на усложнения на ангиоедем. В момента първото лекарство, ATII рецепторен блокер с ефект на инхибиране на NEP в съотношение 1:1, LCZ696, преминава фаза III на клинични изпитвания. Комбинираната лекарствена молекула съдържа валсартан и NEP инхибитор (AHU377) под формата на пролекарство. В голямо проучване при пациенти с хипертония (n=1328), LCZ696 в дози от 200-400 mg показва предимство в хипотензивния ефект спрямо валсартан в дози от 160-320 mg под формата на допълнително понижение на кръвното налягане с 5 /3 и 6/3 mmHg. . Хипотензивният ефект на LCZ696 е придружен от по-изразено понижение на пулсовото кръвно налягане: с 2,25 и 3,32 mmHg. съответно в дози от 200 и 400 mg, което понастоящем се счита за положителен прогностичен фактор за ефекта върху сковаността на съдовата стена и сърдечно-съдовите резултати. В същото време, изследване на неврохуморални биомаркери по време на лечение с LCZ696 показа повишаване на нивото на натриуретичния пептид със сравнима степен на повишаване на нивото на ренин и алдостерон в сравнение с валсартан. Поносимостта при пациенти с хипертония е добра и не са отбелязани случаи на ангиоедем. Проучването PARAMOUMT вече е завършено при 685 пациенти със ЗСН и неувредена EF. Резултатите от проучването показват, че LCZ696 по-бързо и по-значително намалява нивото на NT-proBNP (първичната крайна точка е маркер за повишена активност на натриуретичен пептид и лоша прогноза при ХСН) в сравнение с валсартан и също така намалява размера на левия атриум, което показва регресия на неговото ремоделиране. В момента е в ход проучване при пациенти със ЗСН и намалена ФИ (проучване PARADIGM-HF).
Инхибитори на ендотелиновата система
Ендотелиновата система играе важна роля в регулацията на съдовия тонус и регионалния кръвен поток. Сред трите известни изоформи ендотелин-1 е най-активният. В допълнение към известните вазоконстрикторни ефекти, ендотелинът стимулира пролиферацията и синтеза на междуклетъчния матрикс, а също така, поради директния си ефект върху тонуса на бъбречните съдове, участва в регулирането на водно-електролитната хомеостаза. Ефектите на ендотелина се реализират чрез взаимодействие със специфични рецептори от тип А и В, чиито функции са взаимно противоположни: вазоконстрикцията се осъществява чрез рецептори от тип А, а вазодилатацията се осъществява чрез рецептори от тип В. През последните години беше установено, че В-тип рецепторите играят важна роля в клирънса на ендотелин-1, т.е. когато тези рецептори са блокирани, рецептор-зависимият клирънс на ендотелин-1 се нарушава и концентрацията му се повишава. В допълнение, B-тип рецепторите участват в регулирането на бъбречните ефекти на ендотелин-1 и поддържането на хомеостазата на течности и електролити, което е важно.
В момента е доказана ролята на ендотелина в развитието на редица заболявания, вкл. хипертония, CHF, белодробна хипертония, хронично бъбречно заболяване; доказана е тясна връзка между нивата на ендотелина и метаболитния синдром, ендотелната дисфункция и атерогенезата. От 1990 г в ход е търсене на антагонисти на ендотелиновия рецептор, подходящи за клинична употреба; Вече са известни 10 лекарства („сентани”) с различна степен на селективност към A/B-тип рецептори. Първият неселективен ендотелинов рецепторен антагонист, бозентан, в клинично проучване при пациенти с хипертония показва антихипертензивна ефикасност, сравнима с тази на АСЕ инхибитора еналаприл. По-нататъшни проучвания на ефективността на употребата на ендотелинови антагонисти при хипертония показаха тяхното клинично значение при лечението на резистентна хипертония и висок сърдечно-съдов риск. Тези данни са получени от две големи клинични проучвания, DORADO (n=379) и DORADO-AC (n=849), в които дарусентан е добавен към тройна комбинирана терапия при пациенти с резистентна хипертония. В проучването DORADO при пациенти с резистентна хипертония, съчетана с хронично бъбречно заболяване и протеинурия, в резултат на добавянето на дарузентан се наблюдава не само значително понижение на кръвното налягане, но и намаляване на екскрецията на протеини. Антипротеинуричният ефект на антагонистите на ендотелиновия рецептор впоследствие е потвърден в проучване при пациенти с диабетна нефропатия, използващи авосентан. Въпреки това, в проучването DORADO-AS не са открити предимства в допълнителното намаляване на кръвното налягане пред сравнителните лекарства и плацебо, което е причината за спиране на по-нататъшните проучвания. В допълнение, 4 големи проучвания на ендотелинови антагонисти (бозентан, дарусентан, енразентан) при пациенти със ЗСН показват противоречиви резултати, което се обяснява с повишаване на концентрациите на ендотелин-1. По-нататъшното изследване на антагонистите на ендотелиновия рецептор беше спряно поради нежелани ефекти, свързани със задържане на течности (периферен оток, обемно претоварване). Развитието на тези ефекти се свързва с ефекта на ендотелиновите антагонисти върху В-тип рецептори, което промени търсенето на лекарства, които засягат ендотелиновата система по други пътища; и ендотелиновите рецепторни антагонисти в момента имат само едно показание - лечението на белодробна хипертония.
Като се има предвид голямото значение на ендотелиновата система в регулацията на съдовия тонус, се търси друг механизъм на действие чрез вазопептидаза - EPF, която участва в образуването на активен ендотелин-1 (фиг. 3). Блокирането на ACE и комбинирането му с инхибиране на NEP може ефективно да потисне образуването на ендотелин-1 и да потенцира ефектите на натриуретичния пептид. Предимствата на двойния механизъм на действие са, от една страна, предотвратяване на недостатъците на NEP инхибиторите, свързани с възможна вазоконстрикция, медиирана от активиране на ендотелин, от друга страна, натриуретичната активност на NEP инхибиторите позволява да се компенсира задържането на течности, свързано с неселективна блокада на ендотелиновите рецептори. Daglutril е двоен NEP и ACE инхибитор, който е във фаза II на клинични изпитвания. Проучванията показват изразени кардиопротективни ефекти на лекарството поради намаляване на сърдечното и съдовото ремоделиране, регресия на хипертрофия и фиброза.
Директни ренинови инхибитори
Известно е, че АСЕ инхибиторите и ATII рецепторните блокери повишават активността на ренина чрез механизъм на обратна връзка, което е причината ефективността на блокерите на РААС да се изплъзва. Ренинът представлява първата стъпка от каскадата на RAAS; той се произвежда от юкстагломерулните клетки на бъбреците. Ренинът чрез ангиотензиноген насърчава образуването на ATII, вазоконстрикцията и секрецията на алдостерон, а също така регулира механизмите за обратна връзка. Следователно инхибирането на ренина ни позволява да постигнем по-пълна блокада на системата RAAS. Търсенето на инхибитори на ренина продължава от 1970 г.; Дълго време не беше възможно да се получи перорална форма на ренинови инхибитори поради ниската им бионаличност в стомашно-чревния тракт (по-малко от 2%). Първият директен ренинов инхибитор, подходящ за перорално приложение, алискирен, е регистриран през 2007 г. Алискирен има ниска бионаличност (2,6%), дълъг полуживот (24-40 часа) и екстраренален път на елиминиране. Фармакодинамиката на алискирен е свързана с 80% понижение на нивата на ATII. В клинични проучвания при пациенти с хипертония алискирен в дози от 150-300 mg/ден води до понижение на САН с 8,7-13 и 14,1-15,8 mmHg. съответно и ДАН - със 7,8-10,3 и 10,3-12,3 mm Hg. . Хипотензивният ефект на алискирен се наблюдава при различни подгрупи пациенти, включително пациенти с метаболитен синдром, затлъстяване; по тежест той е сравним с ефекта на АСЕ инхибиторите, блокерите на ATII рецепторите, а адитивен ефект е отбелязан и в комбинация с валсартан, хидрохлоротиазид и амлодипин. Редица клинични проучвания показват органопротективните ефекти на лекарството: антипротеинуричен ефект при пациенти с диабетна нефропатия (проучване AVOID, n=599), регресия на левокамерната хипертрофия при пациенти с хипертония (проучване ALLAY, n=465). Така, в проучването AVOID, след 3 месеца лечение с лосартан в доза от 100 mg/ден и постигане на таргетното ниво на кръвното налягане (<130/80 мм рт.ст.) при компенсированном уровне гликемии (гликированный гемоглобин 8%) больных рандомизировали к приему алискирена в дозах 150-300 мг/сут или плацебо. Отмечено достоверное снижение индекса альбумин/креатинин в моче (первичная конечная точка) на 11% через 3 мес. и на 20% - через 6 мес. в сравнении с группой плацебо. В ночное время экскреция альбумина на фоне приема алискирена снизилась на 18%, а доля пациентов со снижением экскреции альбумина на 50% и более была вдвое большей (24,7% пациентов в группе алискирена против 12,5% в группе плацебо) . Причем нефропротективный эффект алискирена не был связан со снижением АД. Одним из объяснений выявленного нефропротективного эффекта у алискирена авторы считают полученные ранее в экспериментальных исследованиях на моделях диабета данные о способности препарата снижать количество рениновых и прорениновых рецепторов в почках, а также уменьшать профибротические процессы и апоптоз подоцитов, что обеспечивает более выраженный эффект в сравнении с эффектом ингибиторов АПФ . В исследовании ALLAY у пациентов с АГ и увеличением толщины миокарда ЛЖ (более 1,3 см по данным ЭхоКГ) применение алискирена ассоциировалось с одинаковой степенью регресса ИММЛЖ в сравнении с лозартаном и комбинацией алискирена с лозартаном: −5,7±10,6 , −5,4±10,8, −7,9±9,6 г/м2 соответственно. У части пациентов (n=136) проводилось изучение динамики нейрогормонов РААС, и было выявлено достоверное и значительное снижение уровня альдостерона и активности ренина плазмы на фоне применения алискирена или комбинации алискирена с лозартаном, тогда как на фоне применения монотерапии лозартаном эффект влияния на альдостерон отсутствовал, а на активность ренина - был противоположным, что объясняет значимость подавления альдостерона в достижении регресса ГЛЖ.
Освен това се провеждат серия от клинични проучвания на алискирен при лечението на други сърдечно-съдови заболявания, за да се оцени ефектът върху прогнозата на пациентите: ALOFT (n=320), ASTRONAUT (n=1639), ATMOSPHERE (n=7000). ) проучвания при пациенти със ЗСН, проучването ALTITUDE при пациенти със захарен диабет и висок сърдечно-съдов риск, проучването ASPIRE при пациенти с постинфарктно ремоделиране.
Заключение
За решаване на проблемите с профилактиката на сърдечно-съдовите заболявания продължава създаването на нови лекарства със сложен множествен механизъм на действие, позволяващ по-пълна блокада на RAAS чрез каскада от хемодинамични и неврохуморални механизми за регулиране. Потенциалните ефекти на такива лекарства позволяват не само да се осигури допълнителен хипотензивен ефект, но и да се постигне контрол на кръвното налягане при пациенти с висок риск, включително резистентна хипертония. Лекарствата с множество механизми на действие демонстрират предимства в по-изразен органопротективен ефект, който ще предотврати по-нататъшно увреждане на сърдечно-съдовата система. Проучването на ползите от нови лекарства, които блокират RAAS, изисква по-нататъшни изследвания и оценка на тяхното въздействие върху прогнозата на пациенти с хипертония и други сърдечно-съдови заболявания.


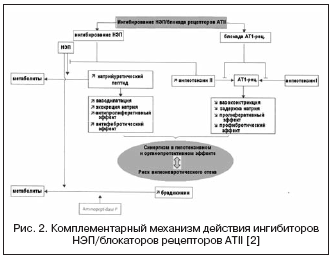
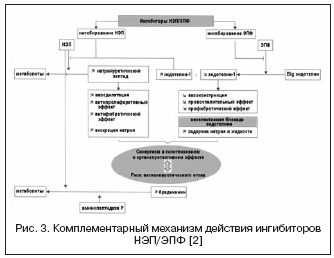
Литература
1. Кембъл Д. Дж. Вазопептидазното инхибиране: нож с две остриета? // Хипертония. 2003. том. 41. С. 383-389.
2. Laurent S., Schlaich M., Esler M. Нови лекарства, процедури и устройства за хипертония // Lancet. 2012. том. 380. С. 591-600.
3. Corti R., Burnett J.C., Rouleau J.L. и др. Вазопептидазни инхибитори: нова терапевтична концепция при сърдечно-съдови заболявания? // Тираж. 2001. том. 104. С. 1856-1862.
4. Mangiafico S., Costello-Boerrigter L.C., Andersen I.A. и др. Инхибиране на неутралната ендопептидаза и натриуретичната пептидна система: развиваща се стратегия в сърдечно-съдовата терапия // Eur. Heart J. 2012, doi:10.1093/eurheartj/ehs262.
5. Rouleau J.L., Pfeffer M.A., Stewart D.J. и др. Сравнение на вазопептидазен инхибитор, омапатрилат и лизиноприл върху толерантността към упражнения и заболеваемостта при пациенти със сърдечна недостатъчност: рандомизирано проучване IMPRESS // Lancet. 2000. Vol. 356. С. 615-620.
6. Packer M., Califf R.M., Konstam M.A. и др. Сравнение на omapatrilat и enalapril при пациенти с хронична сърдечна недостатъчност: The Omapatrilat Versus Enalapril Randomized Trial of Utility in Reducing Events (OVERTURE) // Circulation. 2002. том. 106. С. 920-926.
7. Warner K.K., Visconti JA, Tschampel M.M. Ангиотензин II рецепторни блокери при пациенти с индуциран от АСЕ инхибитор ангиоедем // Ann. Pharmacother. 2000. Vol. 34. С. 526-528.
8. Kostis J.B., Packer M., Black H.R. и др. Омапатрилат и еналаприл при пациенти с хипертония: проучването Omapatrilat за сърдечно-съдово лечение срещу еналаприл (OCTAVE) // Am. J. Hypertens. 2004. том. 17. С. 103-111.
9. Azizi M., Bissery A., Peyrard S. et al. Фармакокинетика и фармакодинамика на вазопептидазния инхибитор AVE7688 при хора // Clin. Pharmacol. Там. 2006. том. 79. С. 49-61.
10. Gu J., Noe A., Chandra P. et al. Фармакокинетика и фармакодинамика на LCZ696, нов инхибитор на неприлизин с двойно действие на ангиотензин рецептор (ARNi) // J. Clin. Pharmacol. 2010. том. 50. С. 401-414.
11. Ruilope L.M., Dukat A., Buhm M. et al. Намаляване на кръвното налягане с LCZ696, нов инхибитор с двойно действие на рецептора на ангиотензин II и неприлизин: рандомизирано, двойно-сляпо, плацебо-контролирано, активно сравнително проучване // Lancet. 2010. том. 375. С. 1255-1266.
12. Solomon S.D., Zile M., Pieske B. et al. Инхибиторът на ангиотензин рецептор неприлизин LCZ696 при сърдечна недостатъчност със запазена фракция на изтласкване: фаза 2 двойно-сляпо рандомизирано контролирано проучване // Lancet. 2012. том. 380 (9851). P. 1387-1395.
13. Левин Е.Р. Ендотелини // N. Engl. J. Med. 1995. Vol. 333. С. 356-363.
14. Dhaun N., Goddard J., Kohan D.E. и др. Роля на ендотелин-1 при клинична хипертония: 20 години по-късно // Хипертония. 2008. том. 52. С. 452-459.
15. Burnier M., Forni V. Ендотелинови рецепторни антагонисти: място в лечението на есенциална хипертония? // Нефрол. Набиране. Трансплантация. 2011. 0: 1-4. doi: 10.1093/ndt/gfr704.
16. Krum H., Viskoper R. J., Lacourciere Y. et al. Ефектът на ендотелин-рецепторен антагонист, бозентан, върху кръвното налягане при пациенти с есенциална хипертония. Bosentan Hypertension Investigators // N. Engl. J. Med. 1998. Том. 338. С. 784-790.
17. Weber M.A., Black H., Bakris G. et al. Селективен ендотелин-рецепторен антагонист за намаляване на кръвното налягане при пациенти с резистентна на лечение хипертония: рандомизирано, двойно-сляпо, плацебо-контролирано проучване // Lancet. 2009. том. 374. С. 1423-1431.
18. Бакрис Г.Л., Линдхолм Л.Х., Блек Х.Р. и др. Различни резултати при използване на клинични и амбулаторни кръвни налягания: доклад за резистентно към дарузентан проучване за хипертония // Хипертония. 2010. том. 56. С. 824-830.
19. Mann J.F., Green D., Jamerson K. et al. Авосентан за явна диабетна нефропатия // J. Am. Soc. Нефрол. 2010. том. 21. С. 527-535.
20. Калк П., Шарковска Ю., Кашина Е. и др. Ендотелинконвертиращият ензим/неутрален ендопептидазен инхибитор SLV338 предотвратява хипертонично сърдечно ремоделиране по начин, независим от кръвното налягане // Хипертония. 2011. том. 57. С. 755-763.
21. Nussberger J., Wuerzner G., Jensen C. et al. Потискане на ангиотензин II при хора чрез теоретично активен инхибитор на ренин Aliskiren (SPP100): сравнение с еналаприл // Хипертония. 2002. том. 39(1). P. E1-8.
22. Alreja G., Джоузеф Дж. Ренин и сърдечно-съдови заболявания: Изтощен път или нова посока? // World J. Cardiol. 2011. том. 3(3). С. 72-83.
23. Ingelfinger J.R. Алискирен и двойна терапия при захарен диабет тип 2 // N. Engl. J. Med. 2008. том. 358 (23). P. 2503-2505.
24. Pouleur A.S., Uno H., Prescott M.F., Desai A. (за изследователите на ALLAY). Потискането на алдостерона медиира регресията на хипертрофия на лявата камера при пациенти с хипертония // J. Renin-Angiotensin-Aldosterone System. 2011. том. 12. С. 483-490.
25. Kelly D.J., Zhang Y., Moe G. et al. Алискирен, нов инхибитор на ренин, е ренопротективен в модел на напреднала диабетна нефропатия при плъхове // Diabetol. 2007. том. 50. С. 2398-2404.


