Lipidi 200401
KEMIJA IN METABOLIZEM LIPIDOV.
LIPIDI - organske snovi, značilne za žive organizme, netopne v vodi, vendar topne v organskih topilih in drug v drugem.
Skupine lipidov se razlikujejo po stopnji hidrofobnosti. Fosfolipidi in glikolipidi so polarni lipidi.
Holesterol zavzema vmesni položaj med polarnimi in absolutno hidrofobnimi lipidi.
Absolutno hidrofobni so trigliceridi in estri holesterola.
Večina lipidov (razen sterolov in nekaterih manjših lipidov) vsebuje višje maščobne kisline (HFA).
Membrane vsebujejo samo FOSFOLIPIDE (PL), GLIKOLIPIDE (GL) in HOLESTEROL (CS).
MAŠČOBNE KISLINE, ZNAČILNE ZA ČLOVEŠKO TELO
Kislina se imenuje maščobna kislina, če je število ogljikovih atomov v njeni molekuli večje od štirih. Prevladujejo dolgoverižne maščobne kisline (število ogljikovih atomov je 16 ali več).Število ogljikovih atomov in dvojnih vezi je označeno z dvojnim indeksom. Na primer: C18:1 (9-10). V tem primeru je 18 število ogljikovih atomov, 1 pa število dvojnih vezi. Položaji dvojnih vezi so navedeni v oklepajih (glede na število ogljikovih atomov).
Učenci morajo poznati število ogljikovih atomov in dvojnih vezi v molekulah naslednjih maščobnih kislin:
С16:0 - palmitinska,
С18:0 - stearinska,
C18:1 - oleinska (9:10),
С18:2 - linolna (9-10,12-13),
С18:3 - linolen (9-10, 12-13, 15-16),
C20:4 - arahidonska (5-6, 8-9, 12-13, 15-16).
Maščobne kisline z dvojno vezjo na položaju 3 imajo zelo izrazit antiaterosklerotični učinek (linolenska kislina). Še posebej veliko maščobnih kislin, ki vsebujejo 3, je v ribjem olju in drugih morskih sadežih. Te maščobne kisline se v človeškem telesu ne sintetizirajo.
Maščobne kisline, ki so del človeškega telesa, imajo skupne značilnosti zgradbe:
Sodo število ogljikovih atomov.
Linearna (nerazvejana) ogljikova veriga.
Polinenasičene maščobne kisline imajo SAMO IZOLIRANE dvojne vezi (vsaj dve enojni vezi med sosednjima dvojnima vezma).
Dvojne vezi imajo samo cis konfiguracijo.
Glede na število dvojnih vezi delimo maščobne kisline na NASIČENE (brez dvojnih vezi), MONONENASIČENE (obstaja ena dvojna vez) in POLINENASIČENE (dve ali več dvojnih vezi).
Proste maščobne kisline najdemo v zelo majhnih količinah. Najdemo jih predvsem v drugih lipidih. Hkrati so z drugimi sestavinami lipidov povezani z estrsko vezjo (esterificirani).
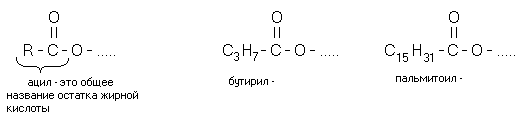
OBLIKE OBSTOJA LIPIDOV V ČLOVEŠKEM TELESU
Maščobni vključki, ki jih je največ v adipocitih. To je oblika obstoja trigliceridov.
Biomembrane. Ne vsebujejo trigliceridov, vsebujejo pa fosfolipide, glikolipide in holesterol.
Lipoproteini. Lahko vključuje lipide vseh razredov.
Lipoproteini
Lipoproteini so sferični delci, v katerih lahko ločimo hidrofobno jedro, sestavljeno iz trigliceridov (TRG) in estrov holesterola (ECS) ter amfifilno lupino, ki vključuje fosfolipide, glikolipide in proteine.
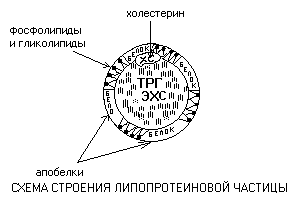
Beljakovine lupine imenujemo apoproteini. Holesterol (CS) običajno zaseda vmesni položaj med lupino in jedrom. Komponente delca so povezane s šibkimi vrstami vezi in so v stanju nenehne difuzije - lahko se gibljejo relativno druga glede na drugo.
Glavna vloga lipoproteinov je transport lipidov, zato jih najdemo v bioloških tekočinah.
Pri preučevanju lipidov krvne plazme se je izkazalo, da jih lahko razdelimo v skupine, saj se med seboj razlikujejo po razmerju komponent. Različni lipoproteini imajo različno razmerje lipidov in beljakovin v sestavi delca, zato je tudi gostota različna.
Lipoproteini se ločijo po gostoti z ultracentrifugiranjem, pri čemer se ne usedejo, ampak lebdijo (lebdijo). Mera plovca je konstanta flotacije, označen s S f (swedbergova flotacija). V skladu s tem indikatorjem ločimo naslednje skupine lipoproteinov:

Lipoproteine lahko ločimo tudi z elektroforezo. Pri klasični alkalni elektroforezi se različni lipoproteini obnašajo različno. Ko lipoproteine postavimo v električno polje, hilomikroni ostanejo na začetku. VLDL in LPP lahko najdemo v pre-globulinski frakciji, LDL v -globulinski frakciji in HDL v -globulinski frakciji:
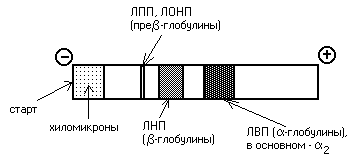
Določanje lipoproteinskega spektra krvne plazme se v medicini uporablja za diagnozo ateroskleroze.
Vsi ti lipoproteini se razlikujejo po svoji funkciji.
1. Hilomikroni (HM)- nastajajo v celicah črevesja, njihova funkcija je prenos eksogene maščobe iz črevesja v tkiva (predvsem v maščobno tkivo) ter transport eksogenega holesterola iz črevesja v jetra.
2. Lipoproteini zelo nizke gostote (VLONP)- nastajajo v jetrih, njihova vloga je transport endogene maščobe, sintetizirane v jetrih iz ogljikovih hidratov, v maščobno tkivo.
3. lipoproteini nizke gostote (LNP)- nastajajo v krvnem obtoku iz VLDL skozi stopnjo nastajanja lipoproteinov srednje gostote (ILP). Njihova vloga: transport endogenega holesterola v tkiva.
4. lipoproteini visoke gostote (HDL)- nastanejo v jetrih, glavna vloga je transport holesterola iz tkiv v jetra, to je odstranitev holesterola iz tkiv, nato pa se holesterol izloči z žolčem.
Pri določanju vsebnosti lipoproteinov različnih gostot v krvi jih običajno ločimo z elektroforezo. Pri tem ostanejo CM na začetku, VLDL se nahajajo v pre-globulinski frakciji, LDL in LPP v -globulinski frakciji, HDL - 2 -globulini. Če je v krvi povečana vsebnost -globulinov (LDL), to pomeni, da se holesterol odlaga v tkivih (razvije se ateroskleroza).
VLOGA APOPROTEINOV V SESTAVI LIPOPROTEINOV
Posebej pomembne so beljakovinske sestavine lipoproteinov. Imenujejo se " apolipoproteini" in so označeni z latiničnimi črkami (apoA, apoB, apoC in tako naprej do apoG).
FUNKCIJE APOBELKS.
1. Apoproteini delujejo kot emulgatorji, ker so amfifilne snovi.
2. Nekateri apolipoproteini so regulatorji aktivnosti encimov presnove lipidov.
3. Lahko imajo lastno encimsko aktivnost.
Lahko delujejo kot ligandi za celične receptorje za lipoproteine.
Veliko apoproteinov prenaša lipide iz enega lipoproteina v drugega.
METABOLIZEM MAŠČOB (TRIACILGLICEROL)
Kemijsko ime za maščobe je acilgliceroli, torej maščobe. To so estri glicerola in višjih maščobnih kislin. "Acil-" pomeni "ostanek maščobne kisline" (ne sme se zamenjevati z "acetil-" - ostankom ocetne kisline). Maščobe glede na število acilnih ostankov delimo na mono-, di- in trigliceride. Če sta v molekuli 2 ostanka maščobne kisline, se maščoba imenuje DIACILGLICERIN. Če molekula vsebuje 1 radikal maščobne kisline, se maščoba imenuje MONOACILGLICEROL.
Pri ljudeh in živalih prevladujejo triacilgliceroli (vsebujejo tri radikale maščobnih kislin).
Lastnosti maščobe določa sestava maščobnih kislin.
Funkcije maščobe:
1. ENERGIJA.
Za razliko od ogljikovih hidratov maščobe predstavljajo energijsko rezervo telesa. Prednost maščobe kot rezerve energije je v tem, da so maščobe bolj reducirane snovi v primerjavi z ogljikovimi hidrati (molekule ogljikovih hidratov imajo kisik na vsakem atomu ogljika - skupine "–CHOH-"; maščoba ima dolge ogljikovodikove radikale, v katerih skupine " -CH 2 -" - nimajo kisika). Iz maščobe se lahko odstrani več vodika, ki nato preide skozi mitohondrijsko oksidacijsko verigo in tvori ATP.
Vsebnost kalorij v ogljikovih hidratih in beljakovinah: ~ 4 kcal / gram.
Vsebnost kalorij v maščobi: ~ 9 kcal / gram.
Prednost maščobe kot energijske rezerve je za razliko od ogljikovih hidratov hidrofobnost – ni povezana z vodo. To zagotavlja kompaktnost maščobnih rezerv - shranjene so v brezvodni obliki in zavzemajo majhen volumen.
V povprečju ima oseba zalogo čistih triacilglicerolov približno 13 kg. Te rezerve bi lahko zadostovale za 40 dni posta v pogojih zmerne vadbe. Za primerjavo: skupne zaloge glikogena v telesu so približno 400 g; med stradanjem ta količina ne zadostuje niti za en dan.
2. ZAŠČITNI.
Maščobno tkivo:
a) ščiti organe pred mehanskimi poškodbami.
b) sodeluje pri termoregulaciji.
Nastajanje maščobnih zalog v telesu človeka in nekaterih živali velja za prilagoditev na neredno prehrano in življenje v hladnem okolju. Posebno velika zaloga maščobe je pri živalih, ki zapadejo v dolgo hibernacijo (medvedi, svizci) in so prilagojene na življenje v hladnih razmerah (mroži, tjulnji). Plod praktično nima maščobe in se pojavi šele pred rojstvom.
VIRI MAŠČOB V TELESU:
1. Prehranske maščobe ( exo genetski)
2. Endo genska maščoba, sintetizirana v jetrih iz ogljikovih hidratov.
Lipidi so netopni v vodi, zato se po krvi prenašajo v kombinaciji z beljakovinami. Maščobne kisline v krvi so povezane z albuminom, drugi lipidi se prenašajo kot del lipoproteinov (LP).
Eden od dejavnikov, ki prispevajo k razvoju aterosklerotičnega procesa, je kršitev metabolizma LP. To dejstvo je v zadnjih 25 letih povzročilo obsežne študije strukture LP, njihove sinteze, presnovnih transformacij in internalizacije delcev LP v celicah. Številna dela predstavljajo podatke o lastnostih in sestavi delcev LP različnih razredov, pa tudi o značilnostih biosinteze in katabolizma lipidnih in beljakovinskih komponent.
Na sl. 1.5 prikazuje strukturne formule glavnih lipidov v plazmi.
Proste ali neesterificirane maščobne kisline so glavni vir energije v telesu. Človeška kri vsebuje tudi nasičene, enkrat nenasičene in večkrat nenasičene maščobne kisline (tabela 1.7).
Tabela 1.7. Maščobne kisline v plazmi Maščobne kisline Ime Dolžina
verige Vir Myristic C 14:0 Kokosovo olje Nasičeno Palmitinsko C 16:0 Živalska maščoba Stearinsko C 18:0 Živalska maščoba Mononenasičeno Palmitoleinsko C 16:1 co 7 Maščoba Oleinsko C 18:1 co9 Maslo Polinenasičeno Linolensko C 18:2 soc Rastlinsko
olje (polien) arahidonska C 20:4 co8 Rastlinska
Eikozapentaenojsko olje C 20:5 co3 Ribja maščoba Opomba. Skrajšana formula prikazuje število ogljikovih atomov in število dvojnih vezi. Dvojna vez, ki je najbližja metilnemu koncu, je označena s simbolom co.
TG so estri glicerola in maščobnih kislin; tako kot maščobne kisline služijo kot pomemben vir energije.
Fosfolipidi so estri glicerola ali sfingozina z maščobnimi kislinami in fosforno kislino. Sestava fosfolipidov vključuje tudi spojine, ki vsebujejo dušik (holin, etanolamin, serin) ali druge hidrofilne skupine, povezane z estrsko vezjo s fosfatom. Fosfolipidi so sestavine vseh celične membrane in LP.
CH3(CH2)„COSH Maščobne kisline (n> 14)
Trigliceridi®
O CH2 - O - C - (CH,) "-CH3II I
CH, - (CH2) „ - s - O-CH o
II
sn, - o - s - k.
Fosfolipidi O
CH, - O - C - (CH,) "-CH,
jaz
CH, ~ (CH2) „ - s - o-sn o
CH2 - O - P - O -1
jaz
O
riž. 1.5. Strukturne formule lipidi.
Holesterol je steroid, na osnovi katerega nastajajo steroidni hormoni in žolčne kisline. Približno 2/3 holesterola v krvi je v obliki holesterolnih estrov in maščobnih kislin, približno 1/3 je v obliki prostega holesterola. Prosti holesterol je del vseh celičnih membran; LP vsebuje prosti in esterificirani holesterol.
V klinični praksi se za odkrivanje motenj presnove lipidov določi raven holesterola in TG v krvnem serumu.
LIPOPROTEINI
Delci LP so makromolekularni kompleksi, katerih notranji del vsebuje nevtralne lipide (TG in estre holesterola), površinsko plast pa sestavljajo fosfolipidi, neesterificirani holesterol in specifični lipidni transportni proteini, imenovani apolipoproteini (apoLP).
LP so razvrščeni glede na njihovo mobilnost v električnem polju (med EF) ali hidrirano gostoto v pogojih povečane gravitacije med preparativnim ultracentrifugiranjem (flotacija ali sedimentacija). Pri izvajanju EP se LP razdeli na frakcije, od katerih ena ostane na začetku (hilomikroni), drugi migrirajo v globulinske cone - R-LP, pre-r-LP, a-LP. Glede na vrednost hidrirane gostote LP običajno delimo v 5 razredov: hilomikroni (XM), LP zelo nizke gostote (VLDL), LP srednje gostote (LDL), LP nizke gostote (LDL), LP. visoka gostota(HDL). Glede na elektroforetično mobilnost VLDL ustrezajo pre-r-LP, LDL - R-LP, HDL - a-LP in HM ostanejo na začetku (slika 1.6).
ApoLP spodbujajo tvorbo micel LP v endoplazmatskem retikulumu hepatocitov, služijo kot ligandi za specifične receptorje na površini plazemske membrane celic in kofaktorji (aktivatorji in zaviralci) procesov lipolize in metabolizma LP v vaskularni postelji (tabela 1.8) .
Glede na vlogo apoLP v organizaciji primarnih delcev LP in njihovih poznejših transformacijah, apoproteini
lahko pa jih razdelimo v dva razreda. Ena od njih bi morala vključevati apoLP, ki tvorijo micelarno strukturo kompleksov LP in služijo kot jedro delcev LP. Značilnost takih apoproteinov je, da proteini ne zapustijo delca LP, pri tvorbi katerega sodelujejo. Ta skupina apoLP vključuje apoB (apoB-100 in apoB-48) in apoA (A-1 in A-H), odgovorna za izvajanje aferentnega in eferentnega transporta lipidov. ApoB je glavni strukturni protein s trigliceridi bogatih delcev LP; ne pušča micelarne
Tabela 1.8. Lastnosti in funkcije apolipoproteinov DpoLP Included in Place
sinteza Mol.
utež,
cD Funkcije C* in
plazma, mg/l A-1 HDL,
hmm tanek
črevesje,
jetra 28.3 Aktivacija LCAT, transport lipidov, ligand za HDL receptor 100-1600 A-H HDL Thin
črevesje,
jetra 17 Strukturni protein, ligand za HDL receptor 300-500 A-1U xm,
lvp,
lponp V redu
črevo 46 Aktivacija LCAT, liganda za HDL receptor 150 V-100 lpp,
lppp,
lpnp Jetra 549 Prenos lipidov iz jeter, vezava na B-, E-receptor 500-900 B-48 xm Thin
črevo 265 Prenos lipidov iz tankega črevesa VLDL,
HDL jetra 6,5 LCHAT aktivator LDL,
HDL Liver 8.8 Activator LPL 30-80 C-W xm,
lponp.
HDLp jetra 8,9 Inhibitor aktivnosti LPL 8-150 B HDL3 20 LCAT aktivator ~100 E
Hm,
HDL Jetra 36,5 Vezava na B- in E-receptorje 30-50 (a) LP(a) Jetra 270-1000 Kompleks v procesu zaporednih presnovnih transformacij VLDL v LDLP in naprej v LDL, katerega kopičenje v vaskularnem zid služi patogenetska povezava aterosklerotični proces. Apoproteina A-1 in A-H sta glavna proteina HDL. Osnova za domnevo, da apoB in apoA tvorita razrede LP, ki se razlikujejo po sestavi in funkciji, je bilo dejstvo, da apoB in apoA nista prisotna skupaj v dolgotrajno krožečih delcih LP. Genetske motnje v sintezi teh apoproteinov so vzrok za motnje v aferentnem in eferentnem transportu lipidov.
ApoLP lahko pripišemo drugemu razredu, njihova glavna vloga je regulacija metabolizma LP v žilni postelji in proces njihove internalizacije v celicah. Ti apoproteini so v LP vsebovani v veliko manjših količinah in se v procesu medsebojne transformacije delcev LP v krvnem obtoku premikajo med LP različnih razredov v obliki proteinsko-lipidnih kompleksov. Presnovno aktivni apoLP-ji ostanejo v žilni postelji dlje kot delci LP, v katere so bili vključeni v času sinteze. Glavna predstavnika skupine presnovno aktivnih apoLP sta apoE (z izoformami E2, E3, E4) in apoC (C-1, C-H, C-Sh).
ApoLP imajo velik pomen za presnovo LP, ki igrajo vlogo ligandov delcev LP, ki medsebojno delujejo s celičnimi receptorji za specifične LP. ApoB-100 in apoE interagirata z receptorjem LDL, pri čemer se začne absorpcijska endocitoza, ki jo spremlja katabolizem LDL. ApoE sodeluje z receptorjem za preostale komponente HM, ki ima pomembno vlogo pri odstranjevanju teh komponent v jetrih. Domneva se, da apoA-1 sodeluje z receptorjem HDL in olajša odstranitev holesterola iz perifernih celic za povratni transport v jetra.
Plazma vsebuje 4 glavne razrede zdravil: XM, VLDL, LDL in HDL ter več drugih zdravil, predstavljenih v relativno nizkih koncentracijah: LDL in Lp (a). V tabeli. 1.9 predstavlja nekatere lastnosti LP.
CM se sintetizirajo v črevesju in služijo za transport eksogenih lipidov. Glavni protein nastajajoče (primarne) HM je apoB-48. Kmalu po izločanju HM iz enterocitov se v njihovo sestavo v žilni postelji vključita 2 dodatna apoproteina, ki ju vsebuje HDL, apoC-H in apoE. ApoS-N aktivira od heparina odvisno lipoproteinsko lipazo, encim, ki je fiksiran.
P P a Mesto nastanka Tanko črevo Jetra Katabolizem
VLDL Katabolizem VLDL prek DILD Jetra, tanko črevo, katabolizem CM in VLDL Glavna funkcija Prenos eksogenih TG Prenos endogenih TG prekurzorja LDL Prenos
Holesterol Reverse
transport
holesterol Sestava: TG 90% 65% 20% 5% 5% holesterol 5% 15% 25% 50% 20% fosfolipidi 4% 10% 35% 25% 25% beljakovine 1% 10% 20% 20% 50% apoproteini A, B-48, C, E B-100, C, E B-100, E B-100 A, C, E Tabela 1.9. Značilnosti lipoproteinov
1.5. Lipidi in lipoproteini -f- 143
na endoteliju kapilar. Lipoproteinska lipaza hidrolizira hilomikronske trigliceride, da nastanejo proste maščobne kisline. Pri hidrolizi LP delci izgubijo približno 96 % svoje mase, predvsem zaradi TG, pa tudi apoLP A in C. Posledično se delec LP pretvori v manjši, s holesterolom obogaten ostanek CM, v katerem apoB in apoE služita kot glavni apoLP. Nastale rezidualne komponente HM imajo hidrirano gostoto VLDL in LDL, običajno pa jih hepatociti izločajo iz krvnega seruma preko specifičnih receptorjev (apoE receptorjev). Zato imajo pri zdravih osebah vmesne oblike LP kratko življenjsko dobo in se v fizioloških pogojih nahajajo v krvnem serumu v nizkih koncentracijah. Vendar pa pri nekaterih oblikah HLP pride do kopičenja LPPP v krvnem serumu. Zaradi teh presnovnih transformacij se prehodni HLP, ki se pojavi v nekaj urah po obroku, izloči, nato pa se eksogeni lipidi uporabijo v jetrih. Lipidi, dostavljeni v jetra, po sestavi maščobnih kislin ustrezajo eksogenim lipidom. Delci LP, ki jih jetra izločajo v krvni obtok, imajo maščobnokislinsko sestavo, značilno za človeško telo.
VLDL nastajajo v jetrih, izločajo jih hepatociti v krvni obtok in prenašajo endogene trigliceride. Nastajajoči VLDL vsebujejo le apoB-100. V krvnem obtoku VLDL vključuje tudi apoLP iz HDL - apoC-P in apoE. Študije metabolizma so pokazale, da se radioaktivnost, ki je bila prvotno prisotna v frakciji VLDL, hitro prenese na delce LDL s hidrirano gostoto LDL. Pri zdravih ljudeh skoraj ves LDL nastane v žilnem koritu iz VLDL. Med presnovo s TH bogatih LP, ki vsebujejo apoB, zaradi hidrolize s TH bogatih LP manjše gostote in velike velikosti pretvori v gostejši in manjši LDL in nato v LDL. Nekatere preostale komponente VLDL in VLDL zapustijo žilno ležišče prek interakcije s specifičnimi receptorji apoB/E na površini endotelijskih celic. V procesu presnovne pretvorbe LPPP v LDL poleg heparin-odvisne lipoproteinske lipaze sodeluje še en lipolitični encim, jetrna trigliceridna lipaza. Ta encim lahko deluje ne le kot TG hidrolaza, ampak tudi kot fosfolipaza.
LDL pri ljudeh vsebuje večina holesterola v obtoku in ga prenašajo v periferna tkiva za tvorbo membran in procese steroidogeneze. LDL sodeluje z receptorji na plazemski membrani celic v jetrih, nadledvičnih žlezah in perifernih tkivih, vključno s SMC in fibroblasti. Po interakciji z receptorjem je LDL podvržen endocitozi in komponente LDL se katabolizirajo v lizosomih. Kot rezultat teh procesov nastanejo ločeni razredi lipidov; apoproteini se razgradijo v aminokisline.
Lp(a) - podobno kot LDL, obogaten s holesterolom in beljakovinami, vsebuje poleg 1 molekule apoB še 2 molekuli apo(a). Povečana raven Lp(a) je povezana z zgodnjim razvojem koronarne srčne bolezni: 50 % bolnikov s koronarno arterijsko boleznijo je imelo raven Lp(a) nad 40 mg/l v primerjavi s 17 % v kontrolni skupini. Zvišanje koncentracije Lp(a) v krvi velja za neodvisen dejavnik tveganja za aterosklerozo.
HDL nastaja na več načinov, vključno s sintezo in izločanjem nastajajočega HDL v jetrih in črevesju, v procesu lipolize lipoproteinov, bogatih s TG, ali kot posledica interakcije novonastalih apoproteinov s celičnimi membranami. Nastajajoči HDL so dvoslojni diski, sestavljeni iz apoLP in fosfolipidov. Prosti holesterol difundira v HDL iz endotelijskih celic, eritrocitov in drugih celic. Poleg tega se med lipolizo VLDL ali HM površinski lipidi (fosfolipidi in holesterol) in proteini (apoA-1, apoA-P, apoproteini skupine C) prenesejo v frakcijo HDL. Te komponente lahko tvorijo nastajajoče diskoidne delce HDL ali pa se vključijo v že obstoječe delce HDL. Diskoidni nastajajoči HDL v krvni plazmi medsebojno deluje z encimom LCAT, kar ima za posledico tvorbo estrov holesterola, ki se hitro premaknejo v jedro delca; nastanejo sferični (zreli) delci HDL - HDL3.
Pri ljudeh se večina estrov holesterola, ki nastanejo v HDL, prenese na večje lipoproteine, bogate s TG. Beljakovine,
prenašanje estrov holesterola, spodbuja izmenjavo estrov holesterola iz HDL v TG iz LP, ki vsebuje apoB, kar vodi do zmanjšanja vsebnosti estrov holesterola in povečanja vsebnosti TG v HDL. Skupni učinek lipolize in transporta lipidov vodi do obogatitve delcev HDL z dodatnimi lipidi in apoproteini, kar ima za posledico povečanje velikosti in zmanjšanje gostote delcev HDL, ki ga spremlja pretvorba delcev HDL3 v HDLg. so nato izpostavljeni jetrni trigliceridni lipazi, encimu, ki ga najdemo predvsem v endotelijskih celicah.sinusoidi jeter. Jetrna trigliceridna lipaza ima aktivnost triglicerid hidrolaze in fosfolipaze, kar vodi do zmanjšanja vsebnosti TG in fosfolipidov v HDL ter zmanjšanja velikosti delcev.
Tako LP krvne plazme, tradicionalno razdeljeni v razrede s fizikalnimi, kemičnimi in imunokemičnimi metodami, presnovno tvorijo en sam sistem.
Vsebnost razredov LP v krvnem serumu je mogoče kvantitativno izmeriti. Tovrstne meritve se izvajajo z metodo analitičnega ultracentrifugiranja, ki zahteva sofisticirano analitično opremo. Prav tako je možno izračunati koncentracijo LP na podlagi analize posamezne komponente. Ta pristop zahteva kvantitativno izolacijo in čiščenje vsakega razreda zdravil s preparativnim ultracentrifugiranjem. Raven lipoproteinov v krvni plazmi v klinični biokemiji se običajno ocenjuje z vsebnostjo holesterola v njih. Vsebnost TG v posameznih skupinah zdravil praviloma ni raziskana, saj je podvržena večjim nihanjem kot raven holesterola. Poudariti je treba, da večina epidemioloških podatkov o povezavi med LP in razvojem KVB temelji na meritvah vsebnosti holesterola v posameznih razredih LP.
Razmerje skupni holesterol krvne plazme in holesterola glavnih razredov LP lahko izrazimo z naslednjo formulo:
holesterol v krvi = holesterol VLDL +
+ LDL holesterol (- HDL holesterol.
Za merjenje holesterolskih razredov LP se določi skupni holesterol in TG krvnega seruma ter koncentracija holesterola HDL v supernatantu po obarjanju LP, ki vsebuje apoB (VLDL in LDL). koncentracija LDL holesterol izračunano po Friedwaldovi formuli:
LDL holesterol = skupni holesterol -
- HDL holesterol - VLDL holesterol.
Za približno oceno koncentracije VLDL holesterola se uporablja vrednost TG / 5, če sta koncentraciji holesterola in TG izraženi v mg / dl, oziroma TG / 2,2, če sta koncentraciji holesterola in TG izraženi v mmol / l. . Uporaba te formule nad 400 mg/dl TG povzroči precenjevanje holesterola VLDL in podcenjevanje holesterola LDL. Za oceno porazdelitve LP pri bolnikih z zelo visoko ravnjo trigliceridov in prisotnostjo znatne količine CM je potrebno predhodno ultracentrifugiranje za ločitev CM in VLDL. Po ločitvi frakcije VLDL in obarjanju LDL v supernatantu lahko določimo koncentracijo holesterola HDL.
Zanesljiva metoda za oceno vsebnosti posameznih razredov LP v krvnem serumu je metoda EF na enem od nosilnih gojišč: agarozni gel, poliakrilamidni gel, celulozni acetat, papir. Te metode vam omogočajo, da dobite samo odstotek posameznih razredov zdravil, vključno z XM, | 3-, pre-f - in a-LP. EF je osnova za fenotipizacijo HLP v skladu s klasifikacijo, ki jo je predlagal Fredrickson (tabela 1.10). Končno odločitev o fenotipu HLP opravimo glede na podatke LP EF, pri čemer upoštevamo koncentracijo holesterola in trigliceridov v krvi ter LDL holesterola.
Klinični pomen določanja lipoproteinov v krvi
Številne klinične in epidemiološke raziskave so pokazale, da je zvišanje ravni holesterola v krvi eden glavnih dejavnikov tveganja za aterosklerozo. enkrat-
Tabela 1.10. Razvrstitev WHO hiperlipoproteinemije Tip HM LDL LDL Holesterol TG Karakter
kršitve I t N N N TT T hm Pa - N TT TT N t lpnp Pi - t t t T lpnp in vpnp III - Plavajoči r-LP t t t OKH in LPPP IV - t N N (T) t T lponp V t 1 N N (T) tt T xm in lponp Opomba. | - porast; OKH - preostale komponente HM.
razvoj HLP je lahko posledica genetskih nepravilnosti in okoljskih dejavnikov (primarni HLP), pa tudi bolezni, kot so diabetes mellitus, patologija jeter, ledvic, hormonske motnje(sekundarni SDP). Pri nastanku primarne HLP ima glavno vlogo dedna nagnjenost. Pri beli ameriški populaciji je 63 % variabilnosti ravni holesterola posledica genetskih variacij. Glede na raziskavo eno- in dvojajčnih dvojčkov v Rusiji je variabilnost celotnega holesterola 82% zaradi genetskih dejavnikov.
Trenutno je raziskanih veliko dednih anomalij metabolizma LP, vendar so le za nekatere znane natančne biokemične napake, ki omogočajo diagnosticiranje bolezni. Te oblike HLP vključujejo družinsko disbetalipoproteinemijo (HLP tipa III) in družinsko hiperhilomikronemijo (HLP tipa I).
DRUŽINSKA HIPERHOLESTEROLEMIJA
Med bolniki s primarno hiperholesterolemijo so najbolj raziskane motnje presnove lipidov pri družinski hiperholesterolemiji. To je dedna monogena bolezen, pri kateri visoka stopnja serumski in LDL holesterol ter zgodnji razvoj ateroskleroza in ishemična bolezen srca.
Kolk dedovanja pri družinski hiperholesterolemiji je avtosomno dominanten. Pri homozigotih je bolezen hujša kot pri heterozigotih. Pri 60 % homozigotov se IHD razvije pred 10. letom starosti. Raven holesterola v serumu pri heterozigotih se giblje od 250 do 550 mg/dl, pri homozigotih so opazili povečanje do 800 mg/dl. Tetivni ksantomi veljajo za patognomonične pri bolnikih z družinsko hiperholesterolemijo. Prevalenca družinske hiperholesterolemije med populacijami Evrope in Amerike je 1: 1.000.000 za homozigote in 1: 500 za heterozigote, čeprav obstajajo populacije z večjo incidenco bolezni - 1: 100 (kanadski Francozi, Finci, belci v Južni Afriki). ).
Molekularno napako, ki določa razvoj družinske hiperholesterolemije, sta opisala Brown in Goldstein. Vzrok za hiperholesterolemijo je okvara receptorja LDL, ki povzroči močno zmanjšanje absorpcije LDL, kar povzroči kopičenje delcev LDL in posledično povečanje njihove koncentracije v krvi. Stopnja zmanjšanja aktivnosti receptorjev LDL pri bolnikih z družinsko hiperholesterolemijo je povezana z ravnijo holesterola LDL, ne pa s kliničnimi manifestacijami bolezni ( zgodnje manifestacije ishemična srčna bolezen, prisotnost ksantomov kit). Ugotovljene so bile štiri vrste genetskih okvar receptorja LDL:
popolna odsotnost receptorskega proteina;
oslabljen transport receptorskega proteina na celično površino;
okvara receptorja, ki preprečuje vezavo LDL;
napaka v receptorju, ki preprečuje njegovo internalizacijo po vezavi na LDL. Doslej so odkrili več kot 150 mutacij tega proteina.
Kljub ugotovitvi genetske okvare, ki določa razvoj družinske hiperholesterolemije, je značilnost klinične manifestacije bolezni in motenj metabolizma lipidov, merila za diagnosticiranje družinske hiperholesterolemije niso dokončno določena. Na žalost določanje aktivnosti receptorja LDL za diagnozo družinske hiperholesterolemije ni našlo široke razširjenosti. Menijo, da je uporaba analize DNK za diagnozo družinske hiperholesterolemije nepraktična zaradi veliko število mutacije. Zvišanje holesterola - mehko diagnostični kriterij družinsko hiperholesterolemijo, saj je opisano, da imajo bolniki zmanjšano aktivnost receptorja apoB in normalno raven holesterola.
Zmanjšanje vezave delcev LDL na receptor je lahko posledica ne samo genetskih okvar, ki povzročajo odsotnost receptorja LDL ali njegove funkcionalne okvare, ampak tudi dednih sprememb liganda, apoB-100. Analiza DNK bolnikov s hiperholesterolemijo je pokazala mutacijo v genu, ki kodira sintezo apoB-100, zaradi česar je bil arginin na mestu 3500 zamenjan z glutaminom. Ta patologija se imenuje "dedna okvara apoB-100". Prevalenca te okvare v populaciji je primerljiva s prevalenco družinske hiperholesterolemije (1: 500), po drugih podatkih pa precej nižja (1: 1300).
DRUŽINSKA KOMBINIRANA HIPERLIPIDEMIJA Izraz "družinska kombinirana hiperlipidemija" (FCH) so prvi predlagali Goldstein et al. leta 1973 za karakterizacijo dedne motnje presnove lipidov, pri kateri imajo proband in njegovi sorodniki 1. stopnje sorodstva. različni tipi HLP (Na, Hn, IV). Motnje presnove lipidov se običajno pojavijo po 20. letu starosti, lahko pa se odkrijejo tudi v starejših letih. zgodnja starost. Pogostnost SHF v populaciji je po različnih raziskovalcih od 0,5 do 2%, pri bolnikih z miokardnim infarktom - 5%, pri bolnikih, mlajših od 60 let, z angiografsko dokumentirano boleznijo koronarnih arterij - 15-20%. Študija rodovnikov je pokazala, da je SKGL - dedna bolezen z avtosomno dominantnim dedovanjem. Kljub številnim študijam biokemični marker SKHF ni bil identificiran; natančna molekularna napaka, ki vodi do nastanka SGL, še ni znana.
POLIGENSKA HIPERHOLESTEROLEMIJA Med dednimi motnjami presnove lipidov je najpogostejša poligenska hiperholesterolemija. Pri tej bolezni je porazdelitev ravni holesterola med pripadniki takšnih
družine preusmerjene k več visoke vrednosti kot povprečje prebivalstva. Poleg tega je porazdelitev unimodalna, kar kaže na odsotnost monogenega dedovanja. Domneva se, da je prisotnost poligenske hiperholesterolemije posledica skupnega vpliva več genov, medtem ko manifestacijo poligenske hiperholesterolemije v veliki meri izzovejo okoljski dejavniki, zlasti narava prehrane. Izraz "poligenska hiperholesterolemija" se uporablja za označevanje bolnikov z dedno hiperholesterolemijo z neidentificirano genetsko okvaro in v odsotnosti znakov monogenskega dedovanja.
Glede na poligensko naravo dedovanja hiperholesterolemije nista znana genetska napaka, ki določa bolezen, in njen biokemični marker (ali markerji). Razširjenost poligenske hiperholesterolemije v populaciji in pri bolnikih s koronarno srčno boleznijo je odvisna od normalne ravni holesterola: z znižanjem norme se delež bolnikov s poligensko hiperholesterolemijo naravno poveča.
DRUŽINSKA HIPERTRIGLICERIDEMIJA
Družinska hipertrigliceridemija je dedna motnja presnove lipidov, pri kateri se pri probandu in njegovih sorodnikih pri normalni koncentraciji holesterola LDL - HLP tipa IV ali V odkrije zmerno ali znatno povečanje ravni TG. Bolezen se običajno pojavi po 30 letih. Pri teh bolnikih se pogosto, vendar ne vedno, zniža raven holesterola HDL. Vrsta dedovanja je avtosomno dominantna. Družinska hipertrigliceridemija se pojavlja v populaciji s pogostnostjo 1 %, pri bolnikih s koronarno arterijsko boleznijo, mlajših od 60 let, pa s pogostnostjo 5-8 %. Genetska okvara, ki povzroča razvoj družinske hipertrigliceridemije, in biokemični marker te bolezni trenutno nista znana.
Diagnostična merila za hiperlipoproteinemije
Za določitev GLP so potrebna jasna biokemična merila. Trenutno obstajata dva pristopa k temu vprašanju. Dolga leta so bile na podlagi rezultatov epidemioloških študij ugotovljene normalne vrednosti holesterola in TG v krvnem serumu ter holesterola LDL in HDL. Za vsako populacijo so bila določena lastna merila za normo metabolizma lipidov glede na 5-10% najmanjših in največjih vrednosti z Gaussovo porazdelitvijo. Za hiperlipidemijo smo v tem primeru šteli takšno koncentracijo holesterola in TG, ki je presegla 90 ali 95 % ravni na Gaussovi ploskvi (glede na spol in starost). Prav ta merila za vrednosti norme so osnova za klasifikacijo SDP, ki so jo predlagali Fredrickson et al. in po nekaterih dodatkih, ki jih je sprejela WHO. V nadaljevanju glede na nakopičene podatke o razmerju napredni nivo holesterol in tveganje za srčno-žilne bolezni, strokovne skupine Nacionalnega izobraževalni program o holesterolu v ZDA in Evropskem združenju za preučevanje ateroskleroze je bila predlagana drugačna klasifikacija HLP. Glede na tveganje za koronarno arterijsko bolezen je predlagano, da se želena raven holesterola v krvi določi pri 6,2 oziroma > 6,5 mmol/l za moške in ženske, starejše od 20 let. Na podlagi teh meril je predlagano razlikovanje med zmerno hiperholesterolemijo (6,2–7,5 ali 6,5–7,8 mmol/l) in hudo hiperholesterolemijo (> 7,5 ali > 7,8 mmol/l).
Skladno s tem so bili spremenjeni tudi kriteriji za holesterol LDL, normalna raven za holesterol TG in HDL pa je ostala enaka. Čeprav zmerna hiperholesterolemija ustreza 75-95% Gaussovi porazdelitvi v ameriški populaciji, se ta merila uporabljajo za tipizacijo HLP v ZDA in Rusiji. Izbira nižjih vrednosti norme je nedvomno upravičena z vidika primarne in sekundarne preventive bolezni koronarnih arterij. Poleg tega uporaba enotnih meril za diagnozo omogoča primerjavo razširjenosti HLP v populacijah z različnimi povprečnimi ravnmi holesterola. Po drugi strani pa ima 95 % oseb s HLP, ugotovljeno po epidemioloških merilih, dedno HLP. V skladu s tem kot zmanjšanje normalne vrednosti povečal se bo delež ljudi, katerih SDP povzročajo le okoljski dejavniki. V zvezi s tem pri iskanju bolnikov s hudimi dednimi oblikami hiperholesterolemije
še vedno velja epidemiološko ugotovljena 90-95% raven holesterola glede na spol in starost
bolnik.
Hipolipoproteinemija
Hipolipoproteinemije nastanejo kot posledica nekaterih okvar, ki uravnavajo lipidno presnovo encimov ali mutacij v genu apoB.
Abetalipoproteinemija in hipobetalipoproteinemija sta dedni bolezni, ki ju povzročajo mutacije v genu apoLP B, glavnem apoLP XM in VLDL. Specifična terapija za te motnje ni bila razvita.
Abetalipoproteinemija: v krvi ni p-lipoproteinov, HM, LP z gostoto pod 1,063 (LDL in VLDL), eritrociti imajo več koničastih izrastkov (akantociti), razvije se pomanjkanje vitaminov E in A (posledica pomanjkanje LDL, ki prenaša v maščobi topne vitamine). Pogoste so črevesna malabsorpcija, motnje koordinacije (zaradi demielinizacije aksonov), ataksija, nistagmus, pigmentoza retinitisa in duševna zaostalost. Steatoreja nastane zaradi pomanjkanja apoB, ki določa nastanek HM v črevesnih celicah. Biopsija tankega črevesa razkrije maščobne vključke v epitelijskih celicah.
Hipobetalipoproteinemijo spremlja zmanjšanje vsebnosti p-lipoproteinov in je pogosto asimptomatsko. Vsebnost HDL je normalna ali povečana, trigliceridi 70-120 mg%, LDL 20-70 mg%. Absorpcija maščob običajno ni motena.
trigliceridi
Trigliceridi (TG; triacilgliceroli) so estri trihidričnega alkohola glicerola in dolgoverižnih maščobnih kislin, med katerimi v človeškem telesu prevladujejo stearinska, palmitinska, palmitooleinska, oleinska in linolna kislina, redkeje pa polinenasičene linolenska in arahidonska kislina. Celice človeških tkiv ne sintetizirajo linolne kisline, zato jo imenujemo esencialne kisline. Porazdelitev maščobnih kislin v molekuli TG je odvisna od dolžine verige in stopnje nenasičenosti. Kislina z najdaljšo verigo je običajno v srednjem položaju. največje število dvojne vezi, skrajne položaje običajno zasedajo nasičene kisline.
Maščobne kisline v telo vstopajo s hrano v obliki triacilglicerolov, ki v Tanko črevo hidroliziran z lipazo. Nastali glicerol in proste maščobne kisline absorbirajo epitelne celice, kjer pride do resinteze TG. Tvorba TG se pojavi v jetrih; maščobne kisline pridejo v jetra iz maščobnega tkiva ali pa se sintetizirajo v hepatocitih. Maščobnokislinska sestava trigliceridov v telesu je v večji meri kot fosfolipidov odvisna od sestave prehranskih maščob. Dolgoverižne maščobne kisline, ki so del TH, so optimalen vir makroergičnih spojin, ki nastanejo med p-oksidacijo maščobnih kislin v mitohondrijih. Večina organov izvaja ravno TG za pokrivanje energetskih potreb. Izjema so možgani; njegova oskrba z energijo nastane zaradi presnove glukoze (aerobna glikoliza).
V krvni plazmi se trigliceridi, tako kot drugi lipidi (holesterol in njegovi estri, fosfolipidi), prenašajo kot del makromolekularnih micelarnih kompleksov - LP. TG so prisotni v vseh razredih lipoproteinov, v VLDL in HM predstavljajo večino lipidov. Z nekaj izkušnjami videz plazma vam omogoča približno določitev vsebnosti TG v njej. Če je krvna plazma prozorna, raven TG v njej ne presega 180-200 mg%; izrazita opalescenca krvne plazme je značilna za hipertrigliceridemijo reda 300-500 mg%, pri čemer raven TG presega 600 mg%, plazma in krvni serum sta neprozorna. Prisotnost HM v krvi je mogoče zaznati s "stojnim testom" - pojavom "smetane" na površini plazme med njenim 16-urnim shranjevanjem pri temperaturi 4 °C. Čist krvni serum in prisotnost HM kažeta na HLP tipa I, odsotnost HM z močno opalescenco ali mlečno obarvanost seruma kaže na HLP tipa IV; prisotnost HM na površini vzorca seruma z izrazito opalescenco ali mlečno obarvanostjo nakazuje, da ima bolnik tip III ali V HLP.
Klinični pomen določanja koncentracije TG
Ne smemo pozabiti, da je HM lahko prisoten v krvnem serumu zdrave osebe, ki je zaužila hrano manj kot 12 ur pred odvzemom krvi. Zaradi pomembnega vpliva indukcije substrata na raven TG se lahko raven TG v krvi čez dan močno spreminja. Hipertrigliceridemijo lahko označimo kot fiziološko ali patološko. Fiziološka hipertrigliceridemija se pojavi po obroku in lahko traja 12-14 ur; stopnja njegove manifestacije je odvisna od narave in količine zaužite hrane. hipertrigl iceridemijo med N-Sh trimesečje nosečnost je tudi fiziološka. Patološko hipertrigliceridemijo glede na patogenetske značilnosti ločimo na primarno in sekundarno. Primarno hipertrigliceridemijo povzročajo genetske motnje metabolizma LP ali povečana indukcija substrata (prenajedanje). Motnje metabolizma TG, ki se pojavijo kot zaplet osnovnega patološkega procesa, imenujemo sekundarne hipertrigliceridemije.
Obstaja več primarnih oblik hipertrigliceridemij, ki jih povzročajo dedne motnje v presnovi LP: družinska hipertrigliceridemijo, družinsko kombinirano hiperlipidemijo, družinsko disbetalipoproteinemijo (tip III HLP), družinsko hiperhilomikronemijo (tip I HLP). K primarnim oblikam presnovnih motenj TG lahko pripišemo tudi hipotrigliceridemijo, ki jo povzročajo genetske spremembe v sintezi ali izločanju apoB. Pri teh boleznih (dedna abetalipoproteinemija ali homozigotna hipobetalipoproteinemija) se lahko vsebnost trigliceridov zmanjša na 19-20 mg%.
Razvoj sekundarne hipertrigliceridemije so opazili pri sladkorni bolezni, hipotiroidizmu, nefrotskem sindromu, peroralnih kontraceptivih in zdravljenju z glukokortikoidi. običajno, patogenetsko zdravljenje usmerjen na glavno patološki proces spremlja zmanjšanje ravni TG.
Korekcija ravni glikemije z insulinom ali peroralnimi hipoglikemičnimi zdravili pomaga normalizirati vsebnost trigliceridov v krvi. Z olajšanjem nefrotskega sindroma se raven TG v krvi zmanjša, vendar včasih ostane povišana dolgo časa. Ukinitev hormonskih kontraceptivov, glukokortikoidov in številnih drugih zdravil (β-blokatorji) prav tako prispeva k normalizaciji ravni TG.
Pri maščobni infiltraciji jeter opazimo hipertrigliceridemijo. Patogeneza te bolezni temelji na povečani oskrbi jeter s prostimi maščobnimi kislinami (povečana lipoliza) ali njihovi povečani sintezi (resinteza) na eni strani in kršitvi izločanja VLDL v jetrih na drugi strani. . Številne strupene spojine, alkohol, farmakološki pripravki prispevajo k motnjam sinteze apoLP, zlasti apoB, v odsotnosti ali pomanjkanju katerega ne pride do tvorbe VLDL. Pod temi pogoji TG, ki prihajajo iz krvi ali na novo sintetizirani, končajo v jetrih in tvorijo strukturo "svinjskih jeter", kar povzroči njihovo maščobno infiltracijo in cirozo.
Hipertrigliceridemijo pogosto opazimo pri bolnikih z akutni pankreatitis. Vendar pa zvišanje ravni trigliceridov ni značilno za akutne lezije trebušne slinavke, nasprotno, huda hipertrigliceridemijo (> 1000 mg%), primarna in sekundarna, prispeva k razvoju bolezni trebušne slinavke in je pogosto zapleten pankreatitis. Pankreatitis velja za eno od kliničnih manifestacij družinske oblike hipertrigliceridemije. Razvoj pankreatitisa je pogosto opažen pri bolnikih s sladkorno boleznijo, z alkoholizmom, pri ženskah, ki jemljejo hormonske kontraceptive.
Podatki o razmerju med hipertrigliceridemijo in CHD so protislovni, čeprav so epidemiološke študije v številnih populacijah pokazale neodvisnost TG kot dejavnika tveganja za CHD. Ocena neodvisnosti TG kot dejavnika tveganja za CHD je izjemno težka zaradi prisotnosti negativne povezave med ravnijo TG in HDL holesterola, neodvisnega negativnega dejavnika tveganja za CHD. Kljub temu, če povečanje koncentracije trigliceridov ni neodvisen dejavnik tveganja za koronarno srčno bolezen, tesna povezava med presnovo trigliceridov in HDL ne daje razlogov za zanikanje pomena hipertrigliceridemije pri nastanku bolezni koronarnih arterij. Biokemična osnova to je lahko kopičenje v krvi LPPP, ki ima izrazito aterogenost.
Pomen hipertrigliceridemije pri nastanku patologije perifernih in možganskih žil je v nasprotju s koronarno arterijsko boleznijo bolj jasen. Študije japonskih strokovnjakov so pokazale, da je pri tej populaciji z nizko ravnjo holesterola v krvi in pojavnostjo miokardnega infarkta hipertrigliceridemijo dejavnik tveganja za periferno arterijsko patologijo. Podobni podatki so bili pridobljeni tudi za druge populacije.
Študija vsebnosti TG v krvnem serumu ima veliko skupnega z določanjem holesterola. Tako holesterol kot TG sta strukturni komponenti LP, ki ju je treba razgraditi, da so lipidi na voljo za kemične ali encimske reakcije. Obe spojini sta hidrofobni, slabo topni v vodne raztopine. Vendar pa obstajajo pomembne razlike pri določanju vsebnosti TG v krvnem serumu: za oceno vsebnosti TG se določi glicerol, ki se sprosti po hidrolizi TG.
Metode za določanje vsebnosti TG v krvi
Obstajata dva načina za določanje vsebnosti TG v krvnem serumu - kemični in encimski; vsak od njih vključuje številne metodološke tehnike. Trenutno je določanje TG mogoče tudi z metodo "suhe kemije".
Kemične metode. Za določanje TG so neposredne kemijske metode (brez predhodne ekstrakcije z organskim topilom) nesprejemljive, saj je v krvnem serumu veliko spojin, ki se med kemično hidrolizo (umiljenje maščobnih kislin) lahko pretvorijo tudi v glicerol, npr. , fosfolipidi in glukoza. V zvezi s tem v kemične metode določanje TG prva faza je ekstrakcija TG in odstranitev motečih spojin. Za ekstrakcijo se uporabljajo organska topila: metanol, etanol, izopropanol in kloroform. Topila denaturirajo LP in spodbujajo disociacijo TG. Moteče spojine odstranimo z ekstrakcijo z organskimi topili (heksan, nonan) ali z adsorbenti (zeolit, silicijeva kislina, florizil).
Druga stopnja kemijskega določanja TG - hidroliza TG s tvorbo glicerola in prostih maščobnih kislin - običajno poteka z reakcijo z etanolno raztopino kalijevega hidroksida pri povišani temperaturi (umiljenje).
Po oksidaciji glicerola v formaldehid se določi z eno od naslednjih reakcij:
reakcija formaldehida z mešanico kromotropne in žveplove kisline (meritev pri 570 nm);
reakcija z mešanico fenilhidrazina, železovega cianida in klorovodikove kisline (meritev pri 540 nm);
reakcija z mešanico 3-metil-2-benzotiazolina in železovega klorida (meritev pri 620 nm);
reakcija z amonijevim acetatom in acetilacetonom.
Reakcijski produkt je mogoče kolorimetrično izmeriti pri
412 nm ali fluorometrično. Pogostejša je fluorometrična metoda, ki je prilagojena polavtomatskim analizatorjem.
encimske metode. Z encimskimi metodami za določanje TG poteka uničenje LP-kompleksov, hidroliza TG v prisotnosti detergentov, lipaze in proteaze. V pogojih encimske hidrolize TG se glicerol ne sprosti iz fosfolipidov in glukoze, zato se specifičnost določanja poveča.
Za določanje glicerola, ki nastane med hidrolizo TH, se uporabljajo številne metode, ki v vsakem primeru uporabljajo številne sklopljene encimske reakcije. Encimske metode omogočajo določanje TG z zmanjšanjem ali povečanjem koncentracije NADH pri valovni dolžini 340 nm. Predlagane so tudi kolorimetrične metode: redukcija soli tetrazolijevega nitrozina z NADH in merjenje nastalega formazana (valovna dolžina 505 nm) ali oksidacija 4-aminofenazona v prisotnosti peroksidaze s tvorbo kromogena (valovna dolžina 510 nm).
Z uporabo encimske metode se je mogoče izogniti uporabi organskih topil, čiščenju ekstraktov za odstranitev motečih spojin, uporabi koncentriranega kalijevega hidroksida in hidrolizi pri visoka temperatura. V primerjavi s kemičnimi metodami ima encimsko določanje TG večjo specifičnost in natančnost, kar je primerno za avtomatizacijo.
Glavne težave pri encimskem določanju TG so možnost nepopolnega uničenja kompleksa LP in nepopolne hidrolize s sproščanjem prostega glicerola. Iz eksperimentalnega dela je znano, da se TG, ki jih tvorijo nasičene in nenasičene maščobne kisline, hidrolizirajo z različnimi stopnjami pod delovanjem lipaze; za hitrost hidrolize je pomembno tudi razmerje med kratko- in dolgoverižnimi maščobnimi kislinami.
Ker določanje vsebnosti TG v krvnem serumu, tako s kemičnimi kot encimskimi metodami, temelji na sproščanju glicerola, je treba upoštevati vsebnost prostega glicerola v krvnem serumu. Pri večini svežih vzorcev seruma pri koncentracijah TG pod 700 mg % sprememba prostega glicerola ne vpliva bistveno na dobljene rezultate. Kopičenje prostega glicerola v krvnem serumu se pojavi pri diabetes mellitusu, nekaterih vrstah jetrne patologije, v pogojih hemodialize, pri akutnem in kroničnem. odpoved ledvic, jemanje nitroglicerina, zdravljenje s heparinom. Akutne okužbe, kratkotrajna stresna stanja, sprejem zdravila, ki imajo lipolitično lastnost, znatno povečajo vsebnost prostega glicerola v krvi. Spontana hidroliza TG se pojavi tudi v krvnem serumu, zlasti če so vzorci shranjeni pri sobni temperaturi.
Za natančno določitev ravni TG je treba izmeriti raven prostega glicerola in rezultat odšteti od splošni pomen. Pri določanju ravni prostega glicerola s kolorimetričnimi in fluorometričnimi metodami je ta lahko v istem vzorcu krvne plazme različen. Fluorometrija Daje bolj stabilne rezultate, vendar manj specifične: v pogojih odpovedi ledvic in aktivirane proteolize lahko fluorescentni peptidi občutno precenijo rezultate.
Za pridobitev natančnih podatkov pri določanju TG je treba uporabiti primarni standard - raztopino triacilglicerolov v organskih topilih. Kot standard se običajno uporablja triolein, čeprav je mešanica trioleina in tripalmitina (2:1 po masi) glede nenasičenosti maščobnih kislin bolj podobna človeškim TG. Standardno se raztopina trioleina v izopropanolu lahko uporablja samo za kemijske raziskovalne metode, saj izopropanol nespecifično aktivira encime, ki se uporabljajo za določanje TG. V zvezi s tem se pri določanju TG z encimskimi metodami uporabljajo sekundarni standardi (kalibratorji) - človeški krvni serum, v katerem se vsebnost TG določi z referenčnimi metodami z uporabo primarnih standardov.
Vzorčenje krvi za določitev TG je treba opraviti 12-14 ur po obroku. Vrednosti TG v krvni plazmi so za 2-4% nižje od tistih v serumu. To je posledica redčenja zaradi tekočine, ki jo eritrociti izgubijo pod delovanjem antikoagulanta. Nekateri antikoagulanti (fluorid, citrat in oksalat) povzročijo večjo izgubo tekočine z rdečimi krvnimi celicami, kar se odraža v večjem znižanju vrednosti TG (do 10%). Kot antikoagulant pri določanju TG je bolje uporabiti EDTA (1 mg/ml polne krvi). Za zmanjšanje učinka redčenja je treba vzorce krvi centrifugirati in dobljeno plazmo ločiti v 2 urah po odvzemu krvi.
HOLESTEROL
Holesterol, 3-p-hidroksiholest-5-en, je enkrat nenasičen sterol s sestavo C27H40(0H)b; Avtor: kemijska struktura je enoatomski sekundarni alkohol (holesterol). Molekula holesterola temelji na strukturi ciklopentanperhidrofenantrena, na tretjem mestu je hidroksilna skupina, med 5. in 6. atomom ogljika je dvojna vez in alifatska stranska veriga z 8 atomi ogljika. Izraz "holesterol" opredeljuje vir, iz katerega je bil prvič izoliran (iz grškega holesterola - žolč). Molekulska masa holesterol 387 D, c čista oblika to je prašek bele barve. holesterol
dobro se topi v organskih topilih (še posebej dobro v alkoholih s 6-7 ogljikovimi atomi). Topnost holesterola v vodi je izjemno nizka in znaša 4,7 µmol/l pri 25°C.
Kemična struktura holesterola omejuje število biokemičnih reakcij, v katere vstopi. Glavna biokemična transformacija holesterola (kot alkohola) je tvorba estrske vezi s kislinami, zlasti s prostimi maščobnimi kislinami, s tvorbo estrov holesterola. 80 % holesterola v telesu je prosti holesterol, skoraj ves je del bioloških membran. Hkrati je 2/3 holesterola v krvnem serumu v obliki estrov z maščobnimi kislinami.
Holesterol je del vseh živih celic. V bioloških membranah ima holesterol strukturno vlogo. Njena struktura je neločljivo povezana z njeno funkcijo, ki določa prepustnost membrane in ustvarjanje mikrookolja za encime, vgrajene v membrano. pomembna funkcija holesterol - njegova vloga kot predhodnik za sintezo steroidnih hormonov.
Vse telesne celice sintetizirajo holesterol iz acetata, ki zaporedno prehaja skozi faze acetoacetata, metilglutaril-CoA in končno mevalonske kisline. Pretvorba metil-glutaril-CoA v mevalonsko kislino pod delovanjem hidroksi-metilglutaril-CoA-(HMG-CoA) reduktaze - ključni trenutek sinteza holesterola. Nastala mevalonska kislina se lahko uporabi le pri sintezi holesterola, zato aktivacija reduktaze HMG-CoA vedno vodi do hiperholesterolemije.
Večina holesterola se sintetizira v jetrih in prihaja iz hrane; Telo sintetizira 1 g holesterola na dan. Del holesterola se oksidira v žolčne kisline, del se odstrani z blatom. Obstaja vzajemno razmerje med holesterolom v prehrani in sintetiziranim v telesu. Holesterol se, tako kot drugi lipidi, prenaša v krvnem serumu kot del LP.
Glavnina serumskega holesterola vsebuje LDL; njihov glavni apoLP je apoB-100. LDL je glavna oblika transporta holesterola in polienskih maščobnih kislin iz
Klinična biokemija jeter do perifernih tkiv. LDL pri interakciji z apoB receptorji plazemske membrane so internalizirani; v liposomih pride do uničenja delca LP s sproščanjem prostega holesterola. Celica uporablja holesterol za izgradnjo membran, del se ga zaestri. Molekule holesterola plazemske membrane Ko so enkrat v krvnem serumu, začnejo aferentno pot do jeter kot del HDL. Holesterol, ki vstopi v jetra kot del HDL, je podvržen mikrosomski hidroksilaciji, se spremeni v žolčne kisline in se tudi izloči v žolču v obliki prostega holesterola ali njegovih estrov.
Na raven holesterola vplivata narava hrane in uživanja alkohola, intenzivno fizično usposabljanje, farmakološki pripravki, vključno s hormonskimi kontraceptivi, steroidi, zdravili za zniževanje lipidov. Sezonska in dnevna nihanja nimajo pomembnega vpliva na ravni holesterola v serumu. Posamezna nihanja vrednosti holesterola so po različnih avtorjih od 3 do 14%. Dnevna nihanja ravni holesterola pri moških in ženskah (0,7-4,3 %) so bistveno nižja od nihanj med
mesecev (2,0–12,2 %) in 1 leto (3,9–10,9 %).
Klinični pomen hiperholesterolemije
Hiperholesterolemija je najbolj dokumentiran dejavnik tveganja za koronarno aterosklerozo. To so potrdile številne epidemiološke in klinične raziskave ki je ugotovil povezavo hiperholesterolemije s koronarno aterosklerozo, pogostost kliničnih manifestacij bolezni koronarnih arterij (angina pektoris in miokardni infarkt). pri sekundarna preventiva koronarne ateroskleroze med terapijo za zniževanje lipidov je bila dokazana regresija klinična slika IHD in kardioskleroza z normalizacijo ravni holesterola v serumu. Za podrobnejšo karakterizacijo dejavnikov tveganja za koronarno aterosklerozo preučujemo vsebnost holesterola v posameznih razredih LP; Najbolj razširjena je študija LDL in HDL holesterola, ki sta pomembna dejavnika tveganja in dejavnika proti tveganju za koronarno aterosklerozo.
Študija holesterola ne nosi diagnostičnih informacij o določeni bolezni, ampak označuje patologijo presnove lipidov in lipidov. Ugotavljanje ravni holesterola je družbenega pomena, saj povečana populacijska raven holesterola zahteva izvajanje organizacijskih ukrepov za primarna preventiva koronarna ateroskleroza. Največ hiperholesterolemije opazimo pri genetskih motnjah metabolizma LP: družinska homo- in heterozigotna hiperholesterolemija, družinska kombinirana hiperlipidemija, poligenska hiperholesterolemija.
S številko patološka stanja razvije se sekundarna hiperholesterolemija. Ti procesi vključujejo hipotiroidizem, nefrotski sindrom, diabetes mellitus itd. Hipoholesterolemija se pojavi pri hipertiroidizmu, v hudih kliničnih situacijah, ki spremljajo različne nosološke oblike bolezni, v akutni fazi vnetnega procesa, pa tudi onkološke bolezni.
Metode določanja holesterola v serumu
Metode za določanje serumskega holesterola so številne; ločimo kemične in encimske metode. Med kemičnimi metodami pa ločimo neposredne in posredne (ekstrakcijske) metode.
KEMIJSKE METODE ZA DOLOČANJE KONCENTRACIJE HOLESTEROLA
neposredne metode. Osnova neposrednih metod za določanje holesterola je Liebermann-Burchardova reakcija, pri kateri holesterol medsebojno deluje z mešanico žveplove in ocetne kisline ter anhidrida ocetne kisline. Reakcija poteka v močno kislem brezvodnem mediju. Med reakcijo se molekula holesterola zaporedno oksidira in nastane obarvana spojina holestaheksaen-žveplova kislina z absorpcijskimi maksimumi pri 410 in 610 nm. Barva v razvoju je nestabilna, zato je treba čas fotometrije natančno vzdrževati. V literaturi lahko najdete drugačno razmerje sestavin v Liebermann-Burchardovem reagentu; večja kot je vsebnost anhidrida ocetne kisline, hitreje poteka reakcija. Reak
tsiya holesterola z mešanico Lieberman-Burchard je nespecifična, V reakciji neposredna opredelitev barva holesterola reakcijske zmesi s standardno raztopino ima smaragdno barvo; vzorci seruma lahko dajejo zeleno, modro, rjavo barvo. To je posledica dejstva, da številne sestavine krvnega seruma vstopijo v reakcijo. Poleg tega pri Liebermann-Burchardovi reakciji prosti holesterol in njegovi estri tvorijo obarvane komplekse z različnimi molarnimi absorpcijskimi koeficienti: v primeru holesterolskih estrov je optična gostota večja. To na začetku povzroči napako v študiji, saj razmerje prosti holesterol/estri holesterola v vsakem od vzorcev ni znano.
Druga pogosta metoda za določanje holesterola je Killiany-Zackova reakcija (reakcija holesterola z železovimi solmi, ocetno in žveplovo kislino). Ta kemična reakcija poteka v prisotnosti ionov železovega železa z zaporedno tvorbo 2, 3 in 4 dvojno konjugiranih vezi v molekuli holesterola, medtem ko absorpcijski maksimum nastalih spojin variira od 420 do 563 nm. Pri Killiany-Zackovi reakciji prosti holesterol in njegovi estri tvorijo podobno obarvane komplekse.
posredne metode. Med indirektne metode sodijo metode, ko lipide iz krvnega seruma najprej ekstrahiramo z organskimi topili, po uparjenju pa izvedemo Liebermann-Burchardovo reakcijo. Ta metoda je bolj ponovljiva in natančna, saj je mogoče odstraniti moteče snovi, ki ostanejo v vodni fazi. Za ekstrakcijo se uporabljajo sistemi etanol-dietileter, etanol-aceton, metanol-kloroform; najpogosteje uporabljena sta heksan in izopropilni alkohol. Vključitev koraka ekstrakcije poveča specifičnost metode; rezultati določanja holesterola so za 7 % nižji kot pri direktni metodi.
Referenčne metode za določanje holesterola potekajo skozi 3 stopnje; ti vključujejo ekstrakcijo lipidov v nepolarno topilo, umiljenje estrov holesterola in ponovno ekstrakcijo holesterola iz umiljene zmesi. Kot referenčna metoda je najbolj zaželena Abell-Kendallova metoda, predlagana leta 1952: ekstrakt lipidov se umili z alkoholno raztopino kalijevega hidroksida in ekstrahira s petroletrom. Liebermann-Burchardova reakcija se izvede po izhlapevanju petroletra.
Težave pri pripravi standardnih raztopin holesterola so povezane z njegovo hidrofobnostjo. dolgo časa kot standardno raztopino smo uporabili raztopino holesterola v ledocetni kislini. Nadalje je bila kot standard predlagana raztopina holesterola v izopropanolu, vendar se je izkazalo, da je tak standard neprimeren za encimske metode za določanje holesterola, saj izopropanol aktivira encimske sisteme in precenjuje optično gostoto. Za določanje holesterola pri delu z biokemičnim analizatorjem je običajno uporabiti sekundarne standarde (kalibratorje) - krvni serum, v katerem je raven holesterola določena z referenčnimi metodami.
Kljub relativni enostavnosti izvedbe in nizki ceni postopka so kemične metode strupene, njihova uporaba na sodobnih analizatorjih pa je povezana s korozijo sistema.
ENZIMSKE METODE ZA DOLOČANJE KONCENTRACIJE
HOLESTEROL
Prednosti encimskega določanja: izvedba reakcije v vodni fazi; udobje avtomatizacije; visoka občutljivost in specifičnost.
Tudi encimsko določanje holesterola vključuje več stopenj: encimsko hidrolizo estrov holesterola pod delovanjem holesterol esteraze s tvorbo prostega holesterola in prostih maščobnih kislin; oksidacija holesterola s kisikom, raztopljenim v reakcijskem mediju pod delovanjem holesterol oksidaze s tvorbo holesta-4-en-3-ola in H2O2. Pri najbolj razširjenih metodah nastali vodikov peroksid oksidira nekatere spojine, da nastanejo kromogeni, ki jih je mogoče izmeriti fotometrično. Ti kromogeni lahko vključujejo 4-aminofenazon (maksimalna absorpcija 500-525 nm), pa tudi tvorbo heterocikla Henach v reakciji z metanolom (maksimalna absorpcija 405 nm). Možno je registrirati nastali vodikov peroksid v reakciji z NAD-odvisnimi dehidrogenazami in izmeriti optično gostoto pri valovni dolžini 340 nm.
Tako kot pri kemičnih metodah lahko nekatere sestavine serumskega holesterola vplivajo na rezultate določanja. Bilirubin zavira reakcijo peroksidaze s 4-aminoantipirinom in fenolom. Na rezultate reakcije vplivajo tudi reducenti sulfhidrilnih skupin (glutation, cistein, ditiotreitol). Metode, ki temeljijo na različnih encimskih reakcijah, lahko dajo različne rezultate.
Metodološke težave pri encimskem določanju holesterola so povezane s heterogenostjo porazdelitve holesterola med LP, pa tudi z njegovo esterifikacijo v krvi. Popolnost hidrolize estrov holesterola je odvisna od vira izolacije encima. Mikrobna holesterol esteraza bolj aktivno hidrolizira estre holesterola, ki jih tvorijo nasičene maščobne kisline, medtem ko trebušna slinavka - polinenasičene maščobne kisline.
Odvzem krvi za določitev vseh lipidov se običajno opravi po 12-16 urah tešča. Koncentracija holesterola v krvi se ne spremeni pred in po obroku, vendar pa lahko izrazita opalescenca krvnega seruma zaradi prisotnosti HM in VLDL moti določanje. Zaželeno je, da bolnik vsaj 2 tedna pred odvzemom krvi ne spremeni svoje običajne prehrane. Za določanje ravni holesterola lahko uporabimo serum ali plazmo. Kot antikoagulant za proizvodnjo plazme se običajno uporablja suha EDTA (1 mg/ml krvi), ki ima tudi antioksidativne lastnosti. Koncentracija holesterola v krvnem serumu je 2-4% nižja kot v krvni plazmi.
Lipidi- maščobam podobne snovi, ki so del vseh živih celic. To je široka skupina organske spojine, vključno z maščobnimi kislinami, pa tudi njihovimi derivati - tako na radikalu kot na karboksilni skupini. Lipidi igrajo zelo pomembno vlogo v življenjskih procesih.
Lipidi opravljajo različne funkcije. So del celičnih membran, služijo kot predhodniki steroidnih hormonov, žolčnih kislin, prostaglandinov in fosfoinozitidov.
Kri vsebuje posamezne sestavine lipidov - nasičene maščobne kisline (SFA), mononenasičene maščobne kisline (MUFA) in večkrat nenasičene maščobne kisline (PUFA), trigliceride, holesterol, estri holesterola in fosfolipidi.
Lipidi so glavne sestavine bioloških membran, ki vplivajo na prepustnost celic in aktivnost številnih encimov, sodelujejo pri prenosu živčni impulz, pri krčenju mišic, ustvarjanju medceličnih stikov, pri imunokemičnih procesih.
Za lipide je značilna topnost v organskih topilih in so na splošno netopni v vodi; so del vseh živih celic. Lipidi tvorijo energijsko rezervo in ustvarjajo zaščitne vodoodbojne in toplotnoizolacijske ovoje v živalih in rastlinah ter ščitijo različne organe pred mehanskimi vplivi. (Na podlagi materialov TSB, Wikipedia, SMT).
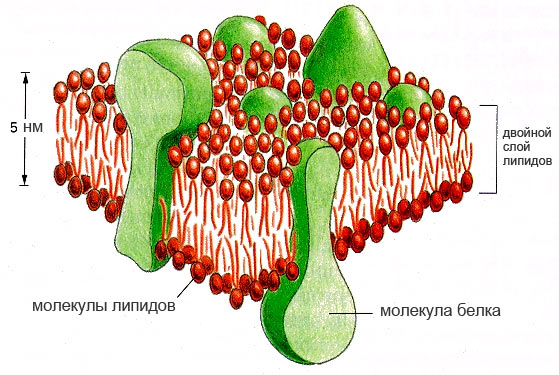
celična membrana
Lipidi se po krvnem obtoku prenašajo v različne organe in tkiva kot del kompleksnih makromolekularnih spojin - lipoproteini , ki so spojine različnih beljakovin (apoproteinov) in lipidov.
Lipoproteini razdeljen na:
Lipoproteini se razlikujejo po velikosti, sestavi in vlogi pri aterogenezi.
V klinični praksi imata LDL in HDL največjo vlogo pri razvoju vaskularne patologije.
LDL v glavnem sestavljen iz estrov holesterola. Njihov funkcionalni apoprotein je protein apoB-100.
Da LDL postanejo aterogeni, morajo biti podvrženi modifikaciji, ki je največkrat posledica procesa njihove peroksidacije. Oksidirani LDL spremenijo svoje lastnosti. Najprej je motena njihova interakcija z jetrnimi receptorji, nato pa postanejo aktivni dražljaji za monocite. Aktivirani krvni monociti prodrejo v subendotelijski prostor žile, se spremenijo v makrofage, ki fagocitirajo spremenjeni LDL in se spremenijo v penaste celice, tj. celice, napolnjene z estri holesterola. Prav holesterol LDL je zaradi njegove pomembne vloge pri nastanku aterosklerotičnih plakov glavna tarča terapije za zniževanje lipidov.
HDL izvajajo obratni transport holesterola iz žilne stene in makrofagov v jetra, od koder se izločijo iz telesa kot del žolčnih kislin. Obstajata dva podrazreda HDL: HDL-2 in HDL-3. HDL-3 je tisti, ki zajame holesterol iz perifernih celic in makrofagov in se spremeni v HDL-2, ki je sestavljen iz estrov holesterola in fosfolipidov. HDL se preko apoproteinov (apoA-1 in apoA-2) veže na jetrne receptorje in celice žilne stene.
lipoproteini nizke gostote- to so spojine beljakovin s holesterolom, ki slednjega prenašajo iz jeter v tkiva. LDL prenašajo potrebni holesterol v tkiva, vendar se s povečanjem njihove koncentracije povečuje tveganje za razvoj ateroskleroze.
Spodaj aterogena razumeti je treba lipoproteine, katerih visoka koncentracija v krvni plazmi je pomembno povezana z razvojem ateroskleroze.
Makrofagi- velike celice, tvorjene iz monocitov, sposobne fagocitoze - proces aktivnega zajemanja in absorpcije živih in neživih delcev s strani enoceličnih organizmov ali posebnih celic (fagocitov) večceličnih živalskih organizmov.
Literatura
Diagnoza in korekcija presnovnih motenj lipidov za preprečevanje in zdravljenje ateroskleroze. Ruska priporočila. Razvil Strokovni odbor VNOK. M., 2004.
Diagnoza in korekcija presnovnih motenj lipidov za preprečevanje in zdravljenje ateroskleroze // Kratka ruska priporočila. Razvila skupina strokovnjakov VNOK. M., 2005.
Orlov R.S., Nozdračev A.D. normalna fiziologija: Učbenik. – M.: GEOTAR-Media, 2009.
Pogozheva A.V. Osnove racionalne dietne terapije za bolezni srca in ožilja // Klinična dietologija. 2004. Zv.1. št. 2.
Pogozheva A.V. Moderni pogledi o dietni terapiji arterijske hipertenzije // Medicina. Kakovost življenja. 2005. št. 3.
Dieta, prehrana in preventiva kronične bolezni. WHO. Ženeva, 1993.
Rehabilitacija za bolezni srčno-žilnega sistema/ Ed. I.N. Makarova. M., 2010.


