טרשת צדדית אמיוטרופית (ALS), הידועה גם כמחלת לו גריג ומחלת שארקוט, מחלה ספציפיתמוביל למוות של תאים. בבריטניה משתמשים במונח מחלת נוירונים מוטוריים (MND), בעוד שבמדינות אחרות המונח מיושם על 5 סוגי מחלות, מהן ALS הנפוצה ביותר. הוא מאופיין בנייוון שרירים, התכווצויות שרירים וחולשה גוברת בהדרגה עקב אובדן של רקמת שריר. זה מוביל לקושי בדיבור, בבליעה ובמקרים מסוימים בנשימה. הסיבה אינה ידועה ב-90-95% מהמקרים. כ-5-10% מהמקרים הם תורשתיים. כמחצית מהמקרים נובעים מגן ספציפי אחד או שניים. זה מוביל למוות של נוירונים השולטים בהתכווצות שרירים מרצון. האבחנה מבוססת על סימנים ותסמינים לאחר בדיקה כדי לשלול מצבים פוטנציאליים אחרים. אין תרופה ל-ALS. תרופה בשם riluzole מאטה את התקדמות ה-ALS ומגדילה את תוחלת החיים ב-2-3 חודשים. אוורור לא פולשני יכול לשפר את מצב המטופל ואת תוחלת החיים. המחלה מתפתחת לרוב מגיל 60, במקרה של מחלה תורשתית– מ-50. תוחלת החיים הממוצעת מתחילת המחלה היא 3-4 שנים. כ-10% מהחולים חיים יותר מ-10 שנים. רובם מתים מדום נשימה. ברוב המדינות, השכיחות של ALS אינה ידועה. באירופה ובארה"ב, המחלה מופיעה אצל 2 מתוך 100,000 אנשים בשנה. המחלה תוארה לראשונה על ידי צ'ארלס בל ב-1824. הקשר בין סימפטומים ובעיות נוירולוגיות בסיסיות תואר על ידי ז'אן מרטין שארקו ב-1869, וב-1874 הוא החל להשתמש במונח "טרשת צדדית אמיוטרופית" בעצמו. בארה"ב נודעה המחלה לאחר שפגעה בשחקן הבייסבול המפורסם לו גריג, וסטיבן הוקינג התפרסם בזכות הישגיו המדעיים. בשנת 2014 הושק קמפיין מקוון להעלאת המודעות ל-ALS. במסגרת הקמפיין הזה, שנקרא אתגר דלי הקרח (תרתי משמע - מבחן עם דלי מי קרח), אנשים כיבקו על עצמם דלי מים ותרמו.
סימנים וסימפטומים
המחלה גורמת לחולשה ובזבוז של שרירים בכל הגוף עקב ניוון של הנוירונים המוטוריים העליונים והתחתונים. אנשים שנפגעו עלולים בסופו של דבר לאבד את היכולת לשלוט בתנועות רצוניות, אך שלפוחית השתן, המעיים ושרירי תנועת העיניים פועלים עד לשלבים המתקדמים של המחלה. התפקוד הקוגניטיבי נשמר גם אצל רוב האנשים, אם כי חלקם (כ-5%) מפתחים דמנציה פרונטומפורלית. רבים (30-50%) חווים גם שינויים קוגניטיביים קלים שעשויים להיעלם מעיניהם אך נראים בבדיקות נוירופסיכולוגיות מפורטות. לעתים רחוקות, ALS נראה אצל אנשים עם מחלת שרירים ועצמות ניוונית (חלק מתסמונת הפרוטונופתיה הרב-מערכתית). המחלה אינה פוגעת בעצבים התחושתיים ובמערכת העצבים האוטונומית, מה שאומר שרוב האנשים שומרים על השמיעה, הראייה, הרגישות, הריח והטעם.
תסמינים ראשוניים
התסמינים המוקדמים של המחלה הם כלליים למדי (חולשה ו/או ניוון שרירים) ולכן האבחנה קשה. תסמינים אחרים כוללים קושי בבליעה, עוויתות או נוקשות של השרירים הפגועים, חולשת שרירים (המשפיעה על הידיים או הרגליים), ו/או דיבור עגום ומעברי האף. בשלבים הראשונים של המחלה, אותו חלק בגוף נפגע, תלוי באילו נוירונים מוטוריים נפגעים ראשונים. כ-75% מהאנשים עם המחלה חשים לראשונה חולשה או ניוון של הידיים או הרגליים. ישנה סרבול בהליכה או בריצה, אדם עלול למעוד או למעוד, או לגרור את הרגל מעט מאחוריו (תסמונת כף הרגל). אם היד מושפעת, אז יש קושי בתנועות הדורשות מיומנות ידנית (למשל, כפתור חולצה, כתיבה, סיבוב מפתח במנעול). התסמינים עשויים להימשך באיבר אחד בלבד למשך תקופה ארוכה או לאורך כל המחלה; הסימפטום ידוע בשם אמיוטרופיה של איבר אחד. כ-25% מכלל המחלות מתחילות כתסמונת בולברית פרוגרסיבית. התסמינים העיקריים במקרה זה מתבטאים בקושי בדיבור או בבליעה. הדיבור הופך מבולבל, שקט יותר ואף. קושי בבליעה מלווה באובדן ניידות של הלשון. במספר קטן של אנשים, השרירים הבין צלעיים, התורמים לתהליך הנשימה, הם הראשונים להיפגע. לאחוז קטן מהאנשים יש דמנציה פרונטו-טמפורלית, אך ככל שהמחלה מתקדמת, מופיעים תסמיני ALS אופייניים יותר. עם הזמן, אנשים חווים קושי בתנועה, בבליעה (דיספגיה), בדיבור ויצירת מילים (דיסארטריה). תפקוד לקוי של נוירון מוטורי עליון מתבטא בקשיות שרירים (ספסטיות) ועלייה פעילות רפלקס(היפרפלקסיה), כמו גם רפלקס גאג היפראקטיבי. רפלקס הבאבינסקי מצביע גם על פגיעה בנוירון המוטורי העליון. תסמינים של פגיעה בנוירון המוטורי התחתון הם חולשת שרירים וניוון, התכווצויות שרירים שניתן לראות מתחת לעור, אך התכווצויות קטנות אינן סימפטום שניתן לאבחן, הן נצפות מאוחר יותר או מלוות חולשה וניוון. כ-15-45% מהאנשים חווים רגישות רגשית, הפרעה נוירולוגית המכונה אי יציבות רגשית, המורכבת מהתקפי צחוק בלתי נשלטים, בכי, חיוך מתמיד, הקשורים לניוון של הנוירונים המוטוריים העליונים הבולבריים, המתבטאים בהבעה מופרזת של רגשות . כדי להיות מאובחן עם ALS, אדם חייב להיות בעל תסמינים של נזק לנוירונים העליונים והתחתונים שאינם טבועים במחלות אחרות.
התפתחות המחלה
למרות שהסדר והמהירות של התפתחות התסמינים משתנים בין אנשים, רוב האנשים אינם מסוגלים ללכת או להשתמש בידיהם. הם גם מאבדים את היכולת לדבר ולבלוע מזון, ולכן בדרך כלל נעשה שימוש ב-BiPAP אוורור לא פולשני (BiPAP). קצב התקדמות המחלה מוערך באמצעות סולם ALSFRS-R, שהוא שאלון או ראיון קליני בסולם מ-48 (תפקוד תקין) עד 0 (צורה חמורה). למרות שמידת השונות גבוהה, ומספר קטן של אנשים סובלים מדרגת מחלה נמוכה, בממוצע, החולים מאבדים 0.9 נקודות בחודש. מחקר המבוסס על בדיקות קליניות הראה שינוי של 20% ב-ALSFRS-R כמשמעותי מבחינה קלינית. ללא קשר לאיזה חלק בגוף נפגע ראשון, המחלה בהתפתחותה מתפשטת לחלקים אחרים בגוף. תסמיני הגפיים בדרך כלל מתפשטים לגפיים מנוגדות ולא לחלק חדש בגוף, בעוד שהתפרצות המחלה פוגעת תחילה בזרועות ולאחר מכן ברגליים. קצב התקדמות המחלה נמוך יותר בחולים מתחת לגיל 40 בהופעתה, בחולים עם רמות נמוכות של השמנת יתר, אצל אנשים עם מחלה בגפה אחת, ובאלה עם תסמינים ראשוניים של מחלת נוירונים מוטוריים עליונים. לעומת זאת, קצב התקדמות המחלה גבוה יותר והפרוגנוזה גרועה יותר אצל אנשים עם דמנציה בולברית, נשימתית ופרונטומפורלית. לגרסה האללית CX3CR1 יש השפעה על התקדמות המחלה ועל תוחלת החיים.
שלבים מאוחרים
למרות שאוורור מסייע עשוי להקל על בעיות נשימה ולהגדיל את תוחלת החיים, הוא אינו מאט את התקדמות ALS. רוב האנשים עם ALS מתים מדום נשימה תוך 3-5 שנים מתחילת התסמינים. תוחלת החיים הממוצעת מתחילת המחלה ועד המוות היא 39 חודשים, ורק 4% מהאנשים חיים יותר מ-10 שנים. הגיטריסט ג'ייסון בקר חי עם המחלה מאז 1989, והפיזיקאי סטיבן הוקינג חי עם המחלה למעלה מ-50 שנה, אך המקרים הללו הם כולם ייחודיים. קושי בלעיסה ובליעה מקשה על האכילה ומגביר את הסיכון לחנק ולבליעת מזון לריאות. בשלבים המאוחרים של המחלה עלולה להתפתח דלקת ריאות אספירציה, ושמירה על המשקל עלולה להפוך לבעיה רצינית, שעלולה לדרוש צינור האכלה. עם היחלשות של הסרעפת והשרירים הבין צלעיים חזה, התומכים בנשימה, בתפקוד הריאות, או ליתר דיוק יכולת חיונית ולחץ השראה, יורדים. בצורת הנשימה של המחלה, זה יכול להתרחש גם לפני היחלשות של שרירי הגפיים. רוב חולי ALS מתים מדום נשימה או דלקת ריאות. עַל שלבים אחרוניםהמחלה עלולה להיות מושפעת עצב אוקולומוטורי, השולט בתנועה, כמו שרירי גלגל העין. תנועת עיניים נשמרת עד לשלבים האחרונים עקב הבדלים בשרירים גַלגַל הָעַיִןעם שרירי השלד, שהם הראשונים להיפגע מהמחלה. בשלבים המאוחרים של המחלה, מצבו של החולה עשוי להידמות לתסמונת נעולה.
תנועות עיניים
אנשים עם ALS עשויים להתקשות בביצוע תנועות עיניים רצוניות מהירות. מהירות תנועת העיניים מואטת. יש גם עווית של התכנסות העיניים. בדיקת הרפלקס הוסטיבולו-עיני יכולה לסייע בזיהוי בעיות אלו. אלקטרוקולוגרפיה (EOG) מודדת את פוטנציאל המנוחה של הרשתית. באנשים עם ALS, EOG מדגים שינויים המשפיעים על התקדמות המחלה וכן מספק נתונים להערכה הקלינית של התקדמות המחלה המשפיעה על פעילות oculomotor. בנוסף, EOG מאפשר לזהות בעיות עיניים בשלב מוקדם. השרירים האוקולומוטוריים שונים משאר שרירי השלד. השריר האוקולומוטורי ייחודי בכך שהוא משתנה כל הזמן לאורך החיים ושומר על מספר תאי הלוויין במהלך ההזדקנות. ישנם הרבה יותר תאי אבות מיוגניים בשרירי האוקולומוטוריים מאשר בשרירי השלד של הגפיים.
גורם ל
גנטיקה
ב-5-10% מהמקרים המחלה עוברת בירושה ישירה מההורים. כ-20% מהמקרים המשפחתיים (או 2% מכלל המקרים) קשורים למוטציה בכרומוזום 21, המקודד לסופראוקסיד דיסמוטאז. יש יותר ממאה צורות של מוטציה. IN צפון אמריקההגן המוטנטי הנפוץ ביותר הוא הגן המוטנטי SOD1; הוא מאופיין בקצב התקדמות גבוה להפליא מזמן המחלה ועד למוות. המוטנט הנפוץ ביותר במדינות סקנדינביה הוא D90A-SOD1, עם קצב התקדמות איטי יותר מאשר ALS טיפוסי, ואנשים עם צורה זו של המחלה חיים בממוצע 11 שנים. בשנת 2011 התגלתה אנומליה גנטית הידועה כחזרה של hexanucleotide ב-C9orf72, אנומליה זו קשורה ל-ALS ולדמנציה פרונטו-טמפורלית ומהווה עד 6% מכלל מקרי ה-ALS בקרב אירופאים לבנים. גן זה קיים גם אצל אנשים ממוצא פיליפיני. הגן UBQLN2 אחראי על ייצור החלבון Ubiquilin 2 בתא, שהוא חבר במשפחת Ubiquilin ושולט על פירוק חלבונים Ubiquitinated. מוטציות ב-UBQLN2 מונעות פירוק חלבון, המובילה לניוון עצבי וגורמת (בעיקר תורשתית) ל-X-linked ALS ו-ALS/דמנציה.
SOD1
בשנת 1993 גילו מדענים שמוטציה בגן (SOD1), המייצרת את האנזים Cu-Zn superoxide dismutase (SOD1), קשורה ל-20% מהמקרים של ALS תורשתי. אנזים זה הוא נוגד חמצון חזק למדי המגן על הגוף מפני נזק הנגרם על ידי סופראוקסיד, רדיקל חופשי רעיל שנוצר במיטוכונדריה. רדיקלים חופשיים הם מולקולות תגובתיות מאוד המיוצרות על ידי תאים במהלך חילוף החומרים. רדיקלים חופשיים יכולים להצטבר ולגרום נזק ל-DNA ולחלבונים בתוך התא. נכון להיום, למעלה מ-110 מוטציות שונות ב-SOD1 קשורות ל-ALS, שלחלקן (כגון H46R) יש היסטוריה קלינית ארוכה מאוד, בעוד שאחרות, כמו A4V, הן אגרסיביות במיוחד. כאשר ההגנה מפני עקה חמצונית נחלשת, מוות תאי (אפופטוזיס) מופעל. פגם ב-SOD1 עלול לגרום לאובדן או רווח של פונקציונליות. אובדן תפקוד SOD1 יכול להוביל להצטברות של רדיקלים חופשיים. רכישת פונקציות SOD1 יכולה להיות רעילה. כתוצאה ממחקרים שכללו עכברים מהונדסים, הוצעו מספר תיאוריות לגבי תפקידו של SOD1 ב-ALS תורשתי. עכברים חסרי הגן SOD1 אינם מפתחים ALS, למרות שהם חווים ניוון שרירים מואץ (סרקופניה) הקשור לגיל ותוחלת חיים מופחתת. משמעות הדבר היא שהתכונות הרעילות של המוטציה SOD1 הן תוצאה של עלייה בתפקוד, לא של אובדן. בנוסף, הצטברות חלבון נמצאה כמאפיין פתולוגי של ALS תורשתית וספורדית (פרוטאינופתיה). באופן מוזר, בעכברים עם מוטציה של SOD1 (בדרך כלל מוטציית G93A), הצטברות (חלבון מקופל שגוי) של SOD1 שעבר מוטציה נמצאה רק ברקמות מושפעות, כאשר הצטברות גדולה יותר נצפתה במהלך ניוון עצבי מוטורי. מדענים מאמינים שהצטברות של SOD1 שעבר מוטציה ממלאת תפקיד חשוב בשיבוש תפקודי התא, דרך פגיעה במיטוכונדריה, בפרוטאזום, בצ'פרונים ובחלבונים אחרים. אם תאושר, כל אחת מהחריגות הללו יכולה לשמש ראיה לכך שהצטברויות כאלה מובילות לרעילות של המוטציה SOD1. המבקרים מציינים כי בבני אדם, מוטציות SOD1 גורמות רק ל-2% מכל מקרי המחלה, ומנגנונים סיבתיים עשויים להיות שונים מאלה האחראים לצורה הספורדית של המחלה. נכון לעכשיו, עכברי ALS-SOD1 נותרו המודל הטוב ביותר של המחלה במחקרים פרה-קליניים, אך יש לקוות שמודל חדש יפותח. קיים מאגר מידע מקוון המהווה קהילה ופלטפורמה מדעית עם מידע ALS עדכני לקהל הרחב. האתר נקרא ALSOD, הוא נוצר במקור עבור פרסומים על הגן SOD1 בשנת 1999, כרגע ישנם יותר מ-40 גנים הקשורים ל-ALS שנמצאים באתר.
גורמים אחרים
במקרה שהמחלה אינה תורשתית, כלומר ב-90% מהמקרים, הגורמים למחלה אינם ידועים. סיבות אפשריותלמרות שאינם אמינים, הם טראומת ראש, שירות צבאי, שימוש תכוף בסמים והשתתפות בספורט מגע. המחקר מתמקד גם בתפקיד של גלוטמט בניוון נוירון מוטורי. גלוטמט הוא אחד מהנוירוטרנסמיטורים במוח. מדענים מצאו שלאנשים עם ALS, בהשוואה לאנשים בריאים, יש יותר רמה גבוההגלוטמט בדם ובנוזל השדרה. רילוזול היא כיום התרופה היחידה המאושרת בארצות הברית לטיפול ב-ALS והשפעות על מעבירי גלוטמט. לתרופה השפעה נמוכה על הגדלת תוחלת החיים, מה שמצביע על כך שעודף גלוטמט אינו הגורם היחיד למחלה. חלק מהמחקרים מצביעים על קשר בין ALS ספורדי (במיוחד אצל ספורטאים) לבין תזונה עשירה בחומצות אמינו מסועפות (תוסף פופולרי בקרב ספורטאים), הגורמות לעוררות תאית דומה לזו של אנשים עם ALS. עוררות תאית מובילה לספיגה מוגברת של סידן על ידי התא, מה שמוביל למוות של תאים עצביים. כמה ראיות מצביעות על כך שהפרעה מתמשכת של היווצרות מבנה חלבון סופראוקסיד דיסמוטאז 1 (SOD1) מתרחשת באותו אופן כמו בפריון. ההשערה היא גם שהשילוב של β-methylamino-l-alanine (BMAA) יוביל להתפשטות דמוית פריון נוספת של היווצרות מבנה חלבון מופרע. גורם שכיח נוסף הקשור ל-ALS הוא נגע מערכת מוטוריתבאזורים כמו האונות הפרונטומפורליות. תבוסה באזור זה היא סימן הפרות מוקדמות, שבו ניתן להשתמש כדי לחזות את ההפסד תפקוד מוטורי. מנגנוני ALS מופיעים הרבה לפני הופעת הסימנים והתסמינים הראשונים. לפני שמתגלה ניוון שרירים, כשליש מהנוירונים המוטוריים צריכים למות. גורמי סיכון פוטנציאליים רבים אחרים נחקרו - חשיפה לכימיקלים, שדות אלקטרומגנטיים, פגיעה פיזית והתחשמלות - אך לא הוסקו מסקנות עקביות.
פתופיזיולוגיה
מאפיין ייחודי של ALS הוא מוות של נוירונים מוטוריים עליונים ותחתונים באזור ההקרנה של קליפת המוח, גזע המוח וחוט השדרה. לפני מותם, נוירונים מוטוריים מפתחים תכלילים עשירים בחלבון בגוף התא ובאקסונים. בחלקו, ייתכן שהסיבה לכך היא פירוק חלבון. תכלילים אלה מכילים לרוב יוביקוויטין ולעיתים קרובות כוללים את אחד מחלבוני ALS: SOD1, חלבון קושר TAR DNA (TDP-43 או TARDBP), או חלבון קושר FUS RNA.
יחידות מוטוריות שלד
שרירים חיצוניים של גלגל העין ו שרירי שלדלהראות מאפיינים שונים. להלן מאפיינים המבדילים בין שרירי גלגל העין לבין שרירי השלד.
סיב עצבי אחד מתחבר לסיב שריר אחד בלבד
ללא רפלקס מתיחה, למרות מספר גדול שלצירי שרירים
אין עיכוב מחזורי
חוסר בשרירי עווית מהירים/איטיים
כל הנוירונים המוטוריים של העין מעורבים בכל סוגי תנועת העיניים.
הבדלים נצפים גם בין שרירים בריאים ומושפעים של גלגל העין. שרירי גלגל העין של תורמים שנפטרו שומרים על הציטוארכיטקטוניקה שלהם, בהשוואה לשרירי הגפיים. שרירי גלגל העין הבריאים מורכבים משכבה מרכזית (GL) בקדמת גלגל העין ושכבה מסלולית דקה (OL) בקדמת המסלול. השרירים האוקולומוטוריים המושפעים מ-ALS שומרים על המיקום של GL ו-OL. השרירים האוקולומוטוריים שומרים על גורם נוירוטרופי שמקורו במוח (BDNF) וגורם נוירוטרופי גליאלי, אשר נשמרים גם בשרירים מושפעי ALS. למינין הוא חלבון מבני הממוקם בצומת העצב-שרירי (NMJ). Lnα4 הוא איזופורם של למינין, כלומר סימן היכרצומת neuromuscular של השרירים oculomotor. אנשים עם ALS שומרים על ביטוי Lnα4 בצומת oculomotor neuromuscular, אך ביטוי זה נעדר בשרירי הגפיים של אותם אנשים. שמירה על ביטוי למינין עשויה למלא תפקיד חשוב בשמירה על שלמות השרירים האוקולומוטוריים אצל אנשים עם ALS. לאנשים עם ALS ספורדי (sALS) יש רמה מוגבהתסידן תוך תאי, הגורם לשחרור מוגבר של נוירוטרנסמיטורים. הובלה פסיבית של סרום מאנשים עם sALS מגבירה את השחרור הספונטני של מתווכים בנוזל השדרה. השרירים האוקולומוטוריים עמידים לשינויים במצב הפיזיולוגי. עם זאת, יש סוגים שוניםהשפעת המחלה. לשרירי האוקולומוטוריים המושפעים מ-ALS יש שונות גדולה יותר בגודל הסיבים מאשר שרירי שליטה בריאים. נמצאו סיבים אטרופיים והיפרטרופיים מקובצים ומפוזרים בשרירי האוקולומוטוריים, אך הנזק לשרירים אלו נמוך במידה ניכרת מאשר בשרירי הגפיים של אותם תורמים. ישנה גם עלייה ברקמת החיבור ועלייה ברקמת השומן בשרירי האוקולומוטוריים כדי לפצות על אובדן סיבים וניוון. לחולים עם ALS יש גם אופטלמופלגיה, אובדן של נוירונים סביב ובתוך הגרעינים של השרירים המוטוריים של גלגל העין. בנוסף, תכולת השרשרת הכבדה של המיוזין בסיבים של השרירים האוקולומוטוריים משתנה, הביטוי התקין של השרשרת הכבדה של המיוזין האיטית ב-GL מופרע, ושרשרת המיוזין הכבדה העוברית נעדרת ב-OL. שינויים בשרשרת הכבדה האיטית של המיוזין ובשרשרת המיוזין הכבדה העוברית הם השינויים היחידים בשרירי האוקולומוטוריים. מכיוון ששריר ה-oculomotor הוא מאוד עצבני, כל דנרבציה מפוצה על ידי אסקונים שכנים, שנשארים מתפקדים.
לקטט וקינמט
חומצה לקטית - מוצר סופיגליקוליזה, הגורמת לעייפות שרירים. האנזים הלקטאט דהידרוגנאז פועל בצורה דו-כיוונית ויכול לחמצן לקטאט לפירובט, כך שניתן להשתמש בו במחזור קרבס. בשרירי האוקולומוטוריים, לקטט תומך בהתכווצות השרירים במהלך פעילות מוגברת. הוא האמין כי השרירים oculomotor פעילות גבוההדהידרוגנאז לקטט עמיד ל-ALS. Cinnamate הוא חוסם הובלת לקטט. Cinnamate מסוגל לגרום לעייפות של השרירים הגלו-מוטוריים, להפחית את סיבולת השרירים ומאמץ שיורי. עם זאת, ל-cinnamate אין השפעה על שרירי הבוהן הפושטות. החלפת הגלוקוז בלקטאט אקסוגני מגבירה את העייפות של שרירי ה-extensor digitorum longus, אך אין לה השפעה על השריר הגלומוטורי. עייפות של שרירי ה-oculomotor נצפתה רק כאשר השילוב של לקטט אקסוגני ו-cinnamate מחליף גלוקוז.
אבחון
שום ניתוח לא יכול לאבחן במדויק ALS, אם כי נוכחותם של סימנים המעידים על מותם של הנוירונים המוטוריים העליונים והתחתונים היא סימן חיוני. אבחון ALS מתרחש בעיקר על סמך תצפיות רופא וסדרת בדיקות השוללות מחלות אחרות. הרופא לוקח היסטוריה רפואית מלאה של המטופל ומבצע באופן קבוע בדיקות נוירולוגיות כדי להעריך את התקדמות התסמינים כגון חולשה, ניוון שרירים, היפר-רפלקסיה וספסטיות בשרירים. בדיקות נוספות עשויות להיעשות כדי לשלול אפשרות של מצבים אחרים, שכן רבים מהתסמינים של ALS יכולים להופיע גם עם מצבים אחרים שניתן לטפל בהם. בדיקה אחת כזו היא אלקטרומיוגרפיה (EMG), המזהה פעילות חשמלית בשרירים. חלק מממצאי EMG עשויים לתמוך באבחון של ALS. בדיקה נפוצה נוספת היא בדיקת מהירות הולכה עצבית (NVR). סטייה מסוימת שזוהתה כתוצאה מהבדיקה עשויה להצביע על כך שלמטופל יש סוג של נוירופתיה היקפית (נזק ל עצבים היקפיים) או מיופתיה (מחלת שרירים), לא ALS. הדמיית תהודה מגנטית יכולה לזהות חריגות הגורמות לתסמיני ALS, כגון נפיחות עמוד שדרה, טרשת נפוצה, פריצת דיסק צווארי, סירינגומיליה או ספונדילוזיס צוואר הרחם. בהתבסס על תסמינים ותוצאות בדיקות, הרופא שלך עשוי להזמין בדיקות דם ושתן או בדיקות מעבדה אחרות כדי לשלול מחלות אפשריות. במקרים מסוימים, אם הרופא חושד שלמטופל יש מיופתיה ולא ALS, הם עשויים להזמין ביופסיית שריר. מחלות ויראליות כגון וירוס הכשל החיסוני האנושי (HIV), וירוס לוקמיה של תאי Tאנושי (HTLS), מחלת ליים, עגבת ו דלקת מוח קרציותיכול לגרום לתסמינים דומים לאלו של ALS. מחלות נוירולוגיותכמו טרשת נפוצה, תסמונת פוסט-פוליו, נוירופתיה מוטורית מולטיפוקל, תסמונת Guillain-Barré וניוון שרירי עמוד השדרה עשויים להיות גם תסמינים דמויי ALS. חשוב לאבחן נכון את המחלה, שכן ניתן לבלבל בקלות בין התסמינים של ALS לבין תסמינים של מספר מחלות אחרות. לכן, יש צורך בהערכה על ידי נוירולוג מוסמך כדי לשלול מחלות אחרות. ברוב המקרים, ALS מאובחן בקלות, כאשר אבחון שגוי מהווה פחות מ-10% מהמקרים. נערך מחקר עם פרוטוקול מחקר ובדיקות סדירות, בו לקחו חלק 190 מטופלים שעמדו בקריטריונים ל-MND/ALS. האבחנה של 30 חולים (16%) השתנתה באופן דרמטי במהלך תקופת המעקב הקליני. באותו מחקר, לשלושה חולים הייתה אבחנה שלילית שגויה, מיאסטניה גרביס (TM, מחלה אוטואימונית). ל-TM יש את אותם תסמינים כמו ALS ועוד כמה מומים נוירולוגיים אחרים, וכתוצאה מכך עיכוב באבחון ובטיפול. TM ניתן לטיפול, אבל ALS לא. תסמונת מיאסטנית, אחרת תסמונת למברט-איטון, יכולה לחקות ALS ו תסמינים מוקדמיםדומה לתסמינים של TM.
יַחַס
טיפול נדרש לחולים עם ALS כדי להקל על הסימפטומים ולהגדיל את תוחלת החיים. הצוות הרפואי הרב-תחומי שעובד עם חולים עם ALS מאמין שטיפול תומך חיוני כדי שהמטופלים יישארו פעילים ונוחים.
תכשירים רפואיים
רילוזול (Rilutek) - מעלה מעט את תוחלת החיים של החולים. זה מגדיל את תוחלת החיים במספר חודשים ויש לו השפעה רבה יותר על חולים עם ALS בולברי. התרופה גם מאפשרת לך לעכב את השימוש באוורור. חולים הנוטלים את התרופה צריכים לעבור בדיקת כבד (10% מהאנשים חווים נזק לכבד כאשר הם נוטלים). התרופה מאושרת על ידי משרד הבריאות האמריקאי ומומלצת לשימוש. המכון הלאומיהסמכה קלינית. רילוזול אינו מתקן נזקים שכבר נגרמו לנוירונים מוטוריים. תרופות אחרות עשויות לשמש כדי להפחית עייפות, להקל על התכווצויות שרירים, לשלוט בספסטיות ולהפחית ריור מוגברוליחה. מספר תרופות יכולות גם להקל על כאבים, דיכאון, לשפר את השינה, להפחית דיספאגיה ועצירות. בקלופן ודיאזפאם נרשמים כדי לשלוט בספסטיות של ALS. ניתן לרשום Trihexyphenidyl או amitriptyline אם לחולים יש בעיות בבליעת רוק.
תמיכה בנשימה
כאשר השרירים המעורבים בנשימה נחלשים, ניתן להשתמש באוורור (אוורור בלחץ חיובי, לחץ דרכי אוויר חיובי דו-מפלסי (BiPAP) או IVL דו-פאזי (BCV)) לתמיכה בנשימה. מכשירים כאלה מאלצים באופן מלאכותי את הריאות לתפקד בעזרת מכשירים חיצוניים הממוקמים על הפנים והגוף. כאשר השרירים כבר לא יכולים לשמור על רמות חמצן ו פחמן דו חמצני, ניתן להשתמש במכשירים אלה לצמיתות. ל-BCV היתרון המובהק שהמכשיר יכול לנקות הפרשות עם רעידות בתדירות גבוהה המתרחשות לאחר כמה נשיפות. מטופלים עשויים גם לשקול שימוש באוורור מכני (מכונות הנשמה), שבהן המכשיר מנפח ומוציא את הריאות. ל שימוש יעיליש צורך בצינור, שחייב לעבור מהאף או מהפה דרך קנה הנשימה. שימוש ארוך טווח במכשיר כזה עשוי לדרוש ניתוח, טרכאוטומיה, שבמהלכו מוחדר צינור ישירות לקנה הנשימה של האדם דרך פתח בצוואר. מטופלים ובני משפחותיהם צריכים לקחת בחשבון מספר גורמים בעת ההחלטה מתי להשתמש באחד מהמכשירים שתוארו לעיל, והאם להשתמש בו בכלל. מאווררים משתנים בהשפעתם על איכות החיים ובמחירם. אומנם אוורור עשוי לסייע בהקלה על בעיות נשימה ובכך להאריך חיים, אך הוא אינו משפיע על התקדמות ALS. לפני שמחליטים באיזה מכשיר לבחור, יש ליידע את המטופלים במלואם לגביהם והשפעתם על החיים ללא תנועה. יש אנשים עם טרכאוטומיה ממושכת, אוורור בלחץ חיובי עם מכונות מיוחדות או צינורות, יכולים לדבר אם השרירים אינם מושפעים חלל פה(אבל בכל מקרה, עם התקדמות המחלה, הדיבור יאבד). מטופלים אחרים עשויים להשתמש בשסתום דיבור (כגון שסתום דיבור Passy-Mure) בהנחיית מטפל בדיבור. מאווררים חיצוניים הפועלים במצב אוורור BiPAP משמשים לשמירה על הנשימה, תחילה בלילה ולאחר מכן במהלך היום. שימוש ב-BiPAP הוא אמצעי זמני. הרבה לפני שה-BiPAP אינו יעיל יותר, על המטופלים לשקול כריתת טרכאוטומיה ואוורור מכני לטווח ארוך. בשלב זה, חלק מהמטופלים בוחרים בטיפול בהוספיס.
תֶרַפּיָה
לפיזיותרפיה תפקיד חשוב בתהליך השיקום, יש לה השפעה מיטיבה על חולי ALS, המאפשרת לעכב את אובדן הכוח, לשמור על סיבולת, להפחית כאב, למנוע סיבוכים ולהבטיח עצמאות תפקודית. טיפול שיקומי וציוד מיוחד מסייעים גם הם להבטיח את עצמאותם ובטיחותם של החולים במהלך ALS. פעילות גופנית אירובית קלה, כגון הליכה, שחייה ורכיבה על אופניים, מחזקת שרירים לא מושפעים, משפרת את בריאות הלב וכלי הדם ומסייעת למטופלים להתמודד עם עייפות ודיכאון. תרגילי תנועה ומתיחות מתחלפים מונעים התכווצויות שרירים והתכווצות שרירים. על המטפלים לוודא שהשרירים נטענים מבלי לאפשר להם לעבוד יתר על המידה. רמפות, פלטה, הליכונים, ציוד לאמבטיה, כסאות גלגליםמה שעוזר לחולים להישאר ניידים. מטפלים עשויים להמליץ על ציוד או מכשירים שיעזרו למטופלים להישאר בטוחים ונורמליים ככל האפשר. מטופלים המתקשים בדיבור יכולים לעבוד עם מומחים ללקויות דיבור כדי לעזור ללמד את המטופלים טכניקות כגון כיצד לדבר חזק יותר וברור יותר. ככל שהמחלה מתקדמת, מומחים עשויים להמליץ על שימוש במכשירים לשיפור הדיבור, או דרכים חלופיותתקשורת, כגון רמקולים, מכשירים להפקת דיבור ו/או לוחות אלפבית, תקשורת באמצעות אותות כן/לא.
תְזוּנָה
מטופלים והמטפלים שלהם יכולים לקבל מידע נחוץמתזונאים כיצד לתכנן את התזונה ולאכול ארוחות קטנות לאורך היום שיספקו מספיק קלוריות, סיבים ונוזלים, וכן מידע מאיזה מזונות כדאי להימנע על מנת להימנע מבעיית הקושי בבליעה. מטופלים יכולים להשתמש במכשירי יניקה כדי להסיר עודפי נוזלים ורוק, ובכך למנוע חנק. מטפלים יכולים לעזור בהמלצות להאכלה עצמית. מומחי ליקויי דיבור יכולים לעזור לך לבחור מוצרים המתאימים ביותר ליכולות שלך. כשהמטופל כבר לא יכול לקבל חומרים מזיניםממזון, הרופאים עשויים להמליץ על שימוש בצינור האכלה. שימוש בצינור האכלה מונע גם את הסיכון לחנק ודלקת ריאות שעלולה לנבוע מנשימת נוזל לריאות. המכשיר לא גורם לשום דבר כְּאֵבומאפשר למטופלים לאכול בעצמם אם ירצו. החוקרים קובעים כי "לחולי ALS יש מחסור כרוני בצריכת האנרגיה" וירידה בתיאבון. מחקרים בבעלי חיים ובבני אדם מאשרים שחולים צריכים לצרוך כמה שיותר קלוריות ולעולם לא להפחית את צריכת הקלוריות שלהם. נכון לשנת 2012, אין נתונים מדויקים לגבי טיפול בירידה במשקל.
טיפול פליאטיבי
עובדים סוציאליים, מטפלים ואחיות הוספיס מסייעים לחולי ALS, משפחותיהם ומטפליהם להתמודד עם קשיים רפואיים, רגשיים וכלכליים, במיוחד בשלבים מתקדמים של המחלה. עובדים סוציאליים מעניקים תמיכה בקבלת סיוע כלכלי, כתיבת ייפוי כוח וצוואה ומסייעים במציאת תמיכה למשפחות ולמטפלים. מטפלים לא רק מספקים טיפול רפואי, אלא גם ללמד את בני משפחתו של המטופל כיצד להשתמש נכון במכונות הנשמה, להאכיל ולהניע את המטופל באופן שימנע בעיות עור כואבות ומתיחות. אחיות ההוספיס עובדות עם רופאים על מנת לספק טיפול מתאים ועזרה בנושאים אחרים הקשורים לשיפור איכות החיים של מטופלים המעוניינים להישאר בבית. עובדי ההוספיס גם מייעצים לחולים ולבני משפחותיהם בכל הנושאים הקשורים לשלב הסופי של המחלה.
אֶפִּידֶמִיוֹלוֹגִיָה
ברוב המדינות, השכיחות של ALS אינה ידועה. באירופה, המחלה פוגעת בכ-2.2 אנשים לכל 100,000 איש בשנה. בארה"ב, 5,600 אנשים מאובחנים מדי שנה, בעוד ש-30,000 אמריקאים כבר סובלים מהמחלה. מהצד טרשת אמיוטרופיתשניים מתוך 100,000 אנשים מתים מדי שנה. ALS נחשבת מחלה נדירה, אך הנפוצה ביותר מכל מחלות הנוירונים המוטוריות, המשפיעה על אנשים מכל גזע ומוצא אתני. ALS מתפתחת אצל 1-2 אנשים לכל 100,000 מדי שנה. ALS משפיעה על עד 30,000 אמריקאים. דווח כי המחלה משפיעה על 1.2-4.0 לכל 100,000 קווקזים, כאשר מספרים קטנים יותר נראים בקבוצות אתניות אחרות. לפיליפינים יש את השכיחות השנייה בגובהה של המחלה (1.1-2.8 מכל 100,000). ישנם דיווחים על מספר "קבוצות" כולל שלושה שחקני פוטבול אמריקאים מה-San Francisco 49ers, למעלה מ-50 שחקני כדורגל באיטליה, שלושה חברי כדורגל בדרום אנגליה ומקרים משפחתיים (בעל ואישה) בדרום צרפת. רוב החוקרים טוענים כי ALS מתרחשת עקב שילוב של תורשתי ו גורמים סביבתיים, למרות שהאחרון לא אושר, בניגוד לסיכון מוגבר למחלה עם הגיל.
כַּתָבָה
המחלה תוארה לראשונה בשנת 1824 על ידי צ'ארלס בל. בארצות הברית נודעה המחלה לאחר שפגעה בשחקן הבייסבול המפורסם לו גריג, ולאחר מכן לאחר קמפיין שנקרא אתגר דלי הקרח בשנת 2014. המדען האנגלי אוגוסט וולר תיאר מראה חיצוני סיבי עצבבשנת 1850. בשנת 1869 הקשר בין סימפטומים ובעיות נוירולוגיות בסיסיות תואר על ידי ז'אן-מרטין שארקו, שהציג את המושג טרשת צדדית אמיוטרופית בעבודתו בשנת 1874. בשנת 1881 תורגם המאמר ל- שפה אנגליתופורסם בשלושה כרכים של הרצאות על מחלות מערכת עצבים". ALS נודע בארצות הברית בשנת 1939 לאחר שהמחלה תקפה את אגדת הבייסבול לו גריג, שמת שנתיים לאחר מכן. בשנות החמישים התרחשה מגיפת ALS בקרב אנשי הצ'מורו בגואם. ב-1991, חוקרים כבר קישרו את כרומוזום 21 לצורה התורשתית של ALS (HALS). בשנת 1993 התגלה כי הגן SOD1 בכרומוזום 21 ממלא תפקיד חשוב במספר מקרים של הצורה התורשתית של המחלה. בשנת 1996, רילוזול אושר על ידי משרד הבריאות האמריקאי לטיפול ב-ALS. בשנת 1998 נקבע קריטריון El Escorial כסטנדרט לסיווג חולי ALS בניסויים קליניים. בשנה שלאחר מכן פורסם סולם הפונקציונליות של ALS והפך לסטנדרט להערכת המחלה בניסויים קליניים. בשנת 2011, חזרות מרובות של C9ORF72 נמצאו כגורם העיקרי ל-ALS ודמנציה פרונטו-טמפורלית.
אֶטִימוֹלוֹגִיָה
המונח "אמיוטרופי" מגיע מהמילה היוונית amyotrophia: א- פירושו "לא", מיו פירושו "שריר", וטרופיה פירושו "הזנה"; לכן אמיוטרופיה פירושה "חוסר הזנת שרירים", המתאר במדויק תכונה אופייניתמחלה, ניוון שרירים. "לרוחב" מתייחס לאזור של חוט השדרה האנושי שבו נמצאים תאי העצב הפגועים. ניוון באזור זה מוביל לדחיסה, טרשת.
תמיכה ציבורית והתייחסות תרבותית
באוגוסט 2014 התקיימה פעולה באינטרנט לתמיכה באנשים עם ALS בשם אתגר דלי הקרח של ALS. המפגין נאלץ למלא דלי מים בקרח, ואז לנקוב בשמות של מי שאתגר אותם, וגם למנות את שלושת האנשים שאותגר. ואז המשתתף הפיל על עצמו דלי מים וקרח. אבל אפשר היה לקחת חלק בפעולה בדרך אחרת. חבר רשאי לתרום מינימום של 10 דולר ארה"ב (או שווה ערך במטבע) למחקר ALS בבריטניה. זה שלא רוצה להירטב מים קריםחייב לתרום מינימום של $100 למחקר ALS. נכון ל-25 באוגוסט, האקשן גייסה 79.7 מיליון דולר, בעוד שבשנת 2013 נאספו רק 2.5 מיליון דולר, סלבריטאים רבים לקחו חלק בפעולה זו. ALS עומדת במרכז הסרט "You Are Not You" משנת 2014, בכיכובם של הילארי סוואנק, אמילי רוסום וג'וש דוהמל.
מחקר
ניסויים קליניים מתנהלים ברחבי העולם; ניתן למצוא רשימה של ניסויים קליניים בארה"ב ב-ClinicalTrials.gov. המחקר הגנטי הגדול ביותר, הנקרא פרויקט MinE, עדיין נמשך. הפרויקט ממומן על ידי גיוס כספים ציבורי ומערב מדינות רבות. שלב II של המחקר הושלם, ושלב IIb עדיין נמשך תחת השם "BENEFIT-ALS". תוצאות המחקר הראשון זמינות כאן המחקר הנוכחי הוא מחקר בינלאומי מבוקר פלצבו, הכולל 680 מטופלים. זה הופך אותו למחקר הגדול ביותר עד כה. מחקר שלב II על הנוגדן ozanezumab נמצא כעת בעיצומו. מדובר במחקר גדול בחסות החברה הבריטית GlaxoSmithKline. בית החולים הדאס בישראל עובר שלב ב' ניסוי קלינישנערך על ידי BrainStorm Cell Therapeutics, העבודה מכוונת לייצב את הפרמטרים של סולם הפונקציונלי ALS. תאי גזע מוסרים במהלך הבדיקה מח עצםאנושי ולהתמיין לחלל הפנוי של התא, מה שמפעיל גורמים נוירוטרופיים. התאים מוזרקים בחזרה לאותו חולה באמצעות זריקות תוך-תיקאליות ותוך-שריריות. מתוכנן כי החלק השני של שלב ב' יתקיים במספר מוסדות בארה"ב, כולל Mayo Clinic.
המחלה אמיוטרופית טרשת צדדית (ALS) מופיעה בשלושה מתוך מאה אלף אנשים. למרות ההתקדמות כיום ברפואה, שיעור התמותה מפתולוגיה זו הוא 100%. עם זאת, ישנם מקרים בהם החולים לא מתו עם הזמן, מצבם התייצב. דוגמה מובהקתהוא הגיטריסט המפורסם ג'ייסון בקר. הוא נלחם באופן פעיל במחלה זו במשך יותר מ-20 שנה.
מה זה BAS?
עם מחלה זו, יש מוות עקבי של הנוירונים המוטוריים של חוט השדרה וחלקים בודדים של המוח, האחראים על תנועות רצוניות. עם הזמן, השרירים אצל אנשים עם אבחנה זו ניוון, מכיוון שהם כל הזמן לא פעילים. המחלה מתבטאת בצורה של שיתוק של הגפיים, שרירי הגוף והפנים.
טרשת צדדית אמיוטרופית נקראת טרשת צדדית אמיוטרופית אך ורק בגלל שהנוירונים המוליכים דחפים לכל השרירים ממוקמים משני צידי חוט השדרה. השלב האחרון של המחלה מאובחן כאשר התהליך הפתולוגי מגיע לדרכי הנשימה. מוות מתרחש עקב ניוון שרירים או זיהום. במקרים מסוימים, שרירי הנשימה מושפעים לפני הגפיים. אדם מת מהר מאוד מבלי לחוות את כל תלאות החיים עם שיתוק.
במדינות רבות באירופה, טרשת צידית אמיוטרופית ידועה כמחלת לו גריג. שחקן הבייסבול המפורסם הזה מאמריקה אובחן עוד בשנת 1939. תוך כמה שנים בלבד, הוא איבד לחלוטין שליטה על גופו, השרירים שלו היו מותשים, והספורטאי עצמו הפך למוגבל. לו גריג נפטר ב-1941.
גורמי סיכון
בשנת 1865, שארקו (נוירולוג צרפתי) תיאר לראשונה מחלה זו. כיום, לא יותר מחמישה אנשים מתוך מאה אלף סובלים מזה בכל העולם. גיל החולים עם אבחנה זו נע בין 20 ל-80 שנים. נציגי המין החזק יותר רגישים למחלה זו.
ב-10% מהמקרים מחלת ALS עוברת בתורשה. מדענים זיהו כ-15 גנים שהמוטציה שלהם פנימה מעלות משתנותמתבטא באנשים עם פתולוגיה זו. 
90% הנותרים מהמקרים הם ספורדיים, כלומר אינם קשורים לתורשה, בטבע. מומחים לא יכולים לנקוב בשמות סיבות ספציפיותמה שמוביל להתפתחות המחלה. ההנחה היא שגורמים מסוימים עדיין עשויים להגביר את הסיכון למחלה, כלומר:
- לעשן.
- עבודה בתעשייה מסוכנת.
- שירות בצבא (מדענים מתקשים להסביר את התופעה).
- אכילת מזונות שגודלו עם חומרי הדברה.
הגורמים העיקריים למחלה
תהליך פתולוגי חמור יכול להתחיל לחלוטין גורמים שוניםשאנו נתקלים בהם ביום יום החיים האמיתיים. מדוע מתרחשת ALS? הסיבות עשויות להיות כדלקמן:
- שיכרון הגוף עם מתכות כבדות.
- מחלות מדבקות.
- מחסור בויטמינים מסוימים.
- פגיעה חשמלית.
- הֵרָיוֹן.
- ניאופלזמות ממאירות.
- התערבויות כירורגיות (הסרת חלק מהקיבה).
צורות המחלה
הצורה הצווארית מאופיינת בהתפשטות התהליך הפתולוגי לאזור השכמות, הזרועות והכל חגורת כתפיים. בהדרגה קשה לאדם לבצע תנועות רגילות (לדוגמה, להדק כפתורים), בהן לא היה צריך להתרכז לפני המחלה. כאשר הידיים מפסיקות "לציית", מתרחשת ניוון שרירים מוחלט. 
הצורה הלומבוסקראלית מאופיינת בתבוסה גפיים תחתונותכמו ידיים. בהדרגה מתפתחת חולשה של השרירים באזור זה, מופיעים עוויתות ועוויתות. חולים מתחילים לחוות קושי בהליכה, מועדים כל הזמן.
צורת Bulbar היא אחד הביטויים החמורים ביותר של המחלה. לעיתים רחוקות מאוד חולים מצליחים לשרוד יותר מארבע שנים מהופעת התסמינים הראשוניים. הסימנים למחלת ALS מתחילים בבעיות בדיבור ובהבעות פנים בלתי נשלטות. החולים מתקשים בבליעה, מה שהופך לחוסר יכולת מוחלט לאכול באופן עצמאי. התהליך הפתולוגי, לוכד את כל גוף האדם, משפיע לרעה על עבודת דרכי הנשימה ו מערכות לב וכלי דם. לכן חולים עם צורה זו מתים לפני מתפתח שיתוק.
הצורה המוחית מאופיינת במעורבות בו-זמנית בתהליך הפתולוגי של הגפיים העליונות והתחתונות כאחד. בנוסף, מטופלים עשויים לבכות או לצחוק ללא סיבה. לפי כוח המשיכה צורה מוחיתלא נחות מהבולבר, אז המוות ממנו מגיע באותה מהירות.
תמונה קלינית
על פי נתונים מסוימים, אפילו בשלב הפרה-קליני, כ-80% מהנוירונים המוטוריים מתים. כל עבודתם משתלטת על ידי תאים סמוכים. הם מגדילים בהדרגה את מספר הענפים הסופיים, והקוד היוני כביכול מתחיל להיות מתורגם למספר רב של שרירים. עקב העומס שנוצר, גם נוירונים אלו מתים. כך מתחילה טרשת צידית אמיוטרופית. תסמיני המחלה אינם מופיעים מיד לאחר מותם של נוירונים מוטוריים.
זה עלול לקחת 5-7 חודשים עד שאדם ישים לב שינויים חיצונייםשל הגוף שלך. לחולים, ככלל, יש ירידה במשקל הגוף וחולשת השרירים, ישנם קשיים ביישום הפעילויות היומיומיות. זה הופך להיות קשה לנוע כרגיל, לשאת חפצים בידיים, לנשום, לבלוע ולדבר. מופיעים עוויתות ועוויתות. תסמינים כאלה אופייניים למחלות רבות, מה שמסבך באופן משמעותי את האבחנה של ALS בשלבים המוקדמים של ההתפתחות.
עם פתולוגיה זו, המערכות לעולם אינן מושפעות איברים פנימיים(כליות, כבד, לב), שרירים האחראים על תנועתיות המעיים.
מחלת ALS היא פרוגרסיבית במהותה, ועם הזמן היא תופסת יותר ויותר אזורים בגוף. אדם מאבד בהדרגה את יכולת התנועה ללא קושי, עקב הפרה רפלקסים של בליעהאוכל כל הזמן בפנים כיווני אווירמה שגורם להפרעות בנשימה. בשלבים האחרונים, פעילות חיונית נתמכת רק בזכות תזונה מלאכותית ומאוורר. 
אבחון
אבחון המחלה קשה ביותר. כל העניין הוא זה בשלבים הראשוניםלמחלת ALS יש מאפיינים דומים להפרעות נוירולוגיות אחרות. רק לאחר בדיקה יסודית של המטופל, הרופא יכול לבצע אבחנה סופית.
אבחון מרמז על מחקר רב-גוני של בריאות המטופל, החל באיסוף אנמנזה וכלה בניתוח גנטי מולקולרי. חוץ מזה, ב בלי להיכשלבדיקה נוירולוגית, MRI, סרולוגית ו ניתוחים ביוכימייםדָם. 
מה צריך להיות הטיפול?
נכון לעכשיו, מומחים אינם יכולים להציע שיטות יעילותיַחַס. כל הסיוע של הרופאים מופחת כדי להקל ככל האפשר על ביטויי המחלה.
הטיפול בטרשת צדדית אמיוטרופית כולל נטילת תרופות אנטי-כולינאסטראז (Galantamine, Prozerin) לשיפור איכות הדיבור והבליעה, מרפי שרירים (Diazepam), תרופות נוגדות דיכאון ותרופות הרגעה. בנגעים זיהומיים, טיפול אנטיביוטי נקבע. מתי כאב חמוררופאים ממליצים ליטול תרופות נוגדות דלקת לא סטרואידיות, לאחר מכן הן מוחלפות בתרופות נרקוטיות.
היחיד תרופה יעילהפעולה מכוונת היא Rilutek. זה לא רק מאריך את חיי המטופל, אלא גם מאפשר לך להגביר את העיכוב בהעברה למכונת ההנשמה. 
טיפול טוב משפר משמעותית את איכות החיים
כמובן שכל אדם שאובחן עם ALS צריך טיפול הולם. החולה בוחן בצורה ביקורתית את מצבו, כי כל יום גופו ממש דוהה. בסופו של דבר, אנשים כאלה מפסיקים לשרת את עצמם באופן עצמאי, מתקשרים עם קרובי משפחה וחברים ונכנסים לדיכאון.
ללא יוצא מן הכלל, כל חולי ALS זקוקים ל:
- במיטה פונקציונלית עם מנגנון הרמה מיוחד.
- במושב האסלה.
- בכיסא גלגלים עם שליטה אוטומטית.
- באמצעי תקשורת, למשל, בלפטופ.
גם תזונה של מטופלים דורשת תשומת לב מיוחדת. עדיף לתת מזון שנבלע היטב עשיר בויטמינים וחלבונים. לאחר מכן, תזונה ללא עזרה של בדיקה מיוחדת אינה אפשרית.
טרשת צדדית אמיוטרופית מתפתחת במהירות אצל אנשים מסוימים. לקרובים ולחברים קשה מאוד, כי אדם ממש מתפוגג לנגד עינינו. לעתים קרובות אנשים המטפלים בחולים זקוקים לעזרה נוספת מפסיכולוג, כמו גם נטילת תרופות הרגעה.
תַחֲזִית
אם הרופא אישר טרשת צדדית אמיוטרופית, התסמינים רק מתגברים מיום ליום, מחמירים מצב כללימטופל, הפרוגנוזה במקרה זה מאכזבת. בכל ההיסטוריה של הרפואה המודרנית נרשמו רק שני מקרים שבהם חולים הצליחו לשרוד. כבר דיברנו על הראשון במאמר זה. והשני הוא הפיזיקאי המפורסם סטיבן הוקינג, שהמשיך להתקיים בהצלחה עם מחלה כזו במשך 50 השנים האחרונות לחייו. המדען עובד באופן פעיל ונהנה מכל יום חדש, למרות שהוא מסתובב בכיסא מצויד במיוחד, ומתקשר עם אחרים באמצעות סינתיסייזר דיבור מחשב. 
צעדי מנע
על אודות מניעה עיקריתאין צורך לדבר על פתולוגיה, שכן הסיבות המדויקות להופעתה עדיין אינן ברורות. מניעה משנית צריכה להיות מכוונת להאט את התקדמות המחלה ולהאריך את חיי החולה. זה כולל:
- התייעצות קבועה עם נוירולוג ונטילת תרופות.
- דחייה מוחלטת של כולם הרגלים רעיםכי הם רק מחמירים את מחלת ה-ALS.
- הטיפול צריך להיות הולם ומוכשר.
- תזונה מאוזנת ורציונלית.
סיכום
במאמר זה, דיברנו על מהי מחלת ALS. תסמינים וטיפול בזה מצב פתולוגילא צריך להתעלם. למרבה הצער, הרפואה המודרנית אינה יכולה להציע טיפול יעיל נגד מחלה זו. עם זאת, קרובי משפחה וחברים צריכים לעשות כל מאמץ כדי להשתפר חיי היום - יוםאדם עם אבחנה זו.
טרשת צדדית אמיוטרופית (ALS, "מחלת הריג", "מחלת נוירונים מוטוריים") תוארה לראשונה על ידי הפסיכיאטר הצרפתי מרטין שארקו ב-1869.
בארה"ב ובקנדה יש מונח נוסף - "מחלת לו גריג", שחקן בייסבול מפורסם שנאלץ לסיים את הקריירה שלו בגיל 36 בגלל טרשת צדדית אמיוטרופית.
מהי טרשת צדדית אמיוטרופית?
טרשת צדדית אמיוטרופית היא מחלה של מערכת העצבים המשפיעה במהירות על הנוירונים המוטוריים של חוט השדרה, גזע המוח וקורטקס.
IN תהליך פתולוגילְהִשְׂתַתֵף עצבים מוטורייםנוירונים גולגולתיים (פנים, טריריים, גלוסופרינגל).
טרשת צדדית אמיוטרופית היא נדירה (2-3 אנשים לכל 100,000) ומתקדמת במהירות.
ברפואה קיים מושג נוסף - תסמונת טרשת צדדית אמיוטרופית. זה מעורר על ידי מחלה אחרת, ולכן הטיפול במקרה זה מכוון לחיסול הפתולוגיה הבסיסית. אם למטופל יש תסמינים של ALS, אך הגורמים להם אינם ידועים, הרופאים אינם מדברים על התסמונת, אלא על המחלה.
ב-ALS, נוירונים מוטוריים נהרסים, הם מפסיקים לשלוח אותות מהמוח לשרירים, כתוצאה מכך, האחרונים מתחילים להיחלש ולהתנוון.
גורם ל

הסיבות המעוררות את הופעתה של מחלה זו טרם הוכחו. עם זאת, מדענים מציעים מספר תיאוריות:
תוֹרַשְׁתִי
הוכח כי ב-10-15% מהמקרים המחלה היא תורשתית.
נְגִיפִי
תיאוריה זו הפכה לנפוצה בשנות ה-60 של המאה ה-20 בארה"ב ובברה"מ. בשלב זה נערכו ניסויים בקופים. לבעלי חיים הוזרקו תמציות של חוט השדרה של אנשים חולים. כמו כן, ההנחה הייתה כי המחלה יכולה להיות מעוררת על ידי נגיף הפוליו.
ג'נאיה
הפרעה בגנים נמצאת ב-20% מהחולים עם ALS. הם מקודדים לאנזים Superoxide dismutase-1, שהופך למסוכן עבורו תאי עצביםסופראוקסיד לחמצן.
אוטואימונית
מדענים ערכו מחקר ומצאו נוגדנים שהורגים תאי עצב מוטוריים. הוכח כי נוגדנים אלו יכולים להיווצר כאשר מחלה רצינית(לימפומה של הודג'קין, סרטן ריאות וכו').
עֲצַבִּי
תיאוריה זו פותחה על ידי מדענים בריטים המאמינים כי היווצרות ALS יכולה לעורר אלמנטים של גליה - תאים האחראים לפעילות החיונית של נוירונים. אם תפקודם של אסטרוציטים שמוציאים גלוטמט מקצות העצבים נפגע, הסיכון למחלת שארקוט עולה פי כמה.
בין גורמי הסיכון מבחינים הרופאים: נטייה תורשתית, גיל מעל 50 שנים, עישון, עבודה הקשורה בשימוש בעופרת ושירות צבאי.
תסמיני ALS
ללא קשר לצורת המחלה, כל החולים חשים בחולשת שרירים, מופיעים עוויתות שרירים ומסת השריר יורדת.
חולשת השרירים גוברת במהירות, אך שרירי העיניים והסוגר שַׁלפּוּחִית הַשֶׁתֶןאינם מושפעים.
בשלב מוקדם של המחלה מתרחשת:
- חולשת שרירים בקרסוליים וברגליים;
- ניוון יד;
- מיומנויות מוטוריות ודיבור לקויים;
- קושי בבליעה;
- התכווצויות שרירים;
- עוויתות של הלשון, הידיים והכתפיים.
עם התפתחות ALS מופיעים התקפי צחוק ובכי, שיווי משקל מופר, ניוון של הלשון מופיע.
התפקודים הקוגניטיביים מחמירים רק ב-1-2% ממקרי המחלה, אצל חולים אחרים הפעילות הנפשית אינה משתנה.
בשלבים המאוחרים יותר המטופל מפתח דיכאון, מתחילות הפרעות בנשימה והיכולת לנוע באופן עצמאי אובדת.
חולים עם ALS מפסיקים להתעניין ביקיריהם ובעולם החיצון, הם הופכים לקפריזיים, חסרי מעצורים, לאביליים רגשית ותוקפניים. כאשר שרירי הנשימה מפסיקים לעבוד, האדם זקוק לאוורור מכני.
מהלך המחלה
בתחילה מופיעים תסמינים המונעים מאדם לנהל חיים מלאים: חוסר תחושה בשרירים, עוויתות, עוויתות, קושי בדיבור. אבל, ככלל, בהתחלה קשה לקבוע את הגורם המדויק להפרעות אלה.
ברוב המקרים, ALS נמצא בשלב של ניוון שרירים.
בהדרגה, חולשת השרירים מתפשטת ומכסה חלקים חדשים בגוף, המטופל לא יכול לנוע באופן עצמאי, בעיות נשימה מתחילות.
חולי ALS סובלים רק לעתים רחוקות מדמנציה, אך מצבם מוביל לדיכאון חמור בציפייה למוות. בשלב האחרון, אדם כבר לא יכול לאכול, ללכת ולנשום בעצמו, הוא זקוק למכשירים רפואיים מיוחדים.
צורות המחלה
צורות המחלה נבדלות על ידי מיקום השרירים הפגועים.
בולברנאיה
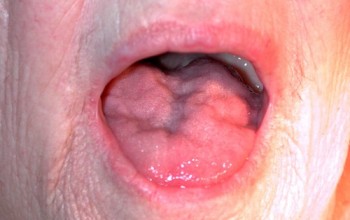
עצבי הגולגולת מושפעים (9,10,12 זוגות).
חולים עם הצורה הבולברית של ALS מתחילים לסבול מבעיות בדיבור, הם מתלוננים על קושי בהגייה, קשה להם להזיז את הלשון.
עם התקדמות המחלה, פעולת הבליעה מופרעת, מזון יכול לשפוך החוצה דרך האף. בשלב המאוחר של המחלה, ניוון מוחלט של שרירי הפנים והצוואר, הבעות הפנים נעלמות וחולים עם ALS אינם יכולים לפתוח את הפה וללעוס מזון.
cervicothoracic

המחלה מתקדמת בגפיים העליונות משני הצדדים.
בתחילה, מופיעה אי נוחות בידיים, לאדם קשה לבצע תנועות מורכבות בידיו, לכתוב, לנגן בכלי נגינה. בבדיקה, הרופא שם לב ששרירי זרועותיו של המטופל מתוחים, ורפלקס הגידים מוגבר.
בשלבים מתקדמים של המחלה חולשת השרירים מתקדמת ומתפשטת לאמות הידיים והכתפיים.
lumbosacral
התסמין הראשון הוא חולשה בגפיים התחתונות.
למטופל קשה יותר לבצע עבודה בעמידה, לטפס במדרגות, לרכוב על אופניים וללכת מרחקים ארוכים.
עם הזמן, כף הרגל מתחילה לצנוח, ההליכה משתנה, ואז שרירי הרגליים מתנוונים לחלוטין, האדם אינו יכול ללכת, מתפתחת בריחת שתן וצואה.
כמעט 50% מהחולים סובלים מהצורה צוואר הרחם של ALS, 25% כל אחד הם לומבו-סקראליים ובולבריים.
אבחון
הנוירולוג משתמש כשיטות האבחון העיקריות:
MRI של המוח וחוט השדרה
בשיטה זו ניתן לזהות ניוון של מבנים פירמידליים וניוון של החלקים המוטוריים של המוח.
בדיקות נוירופיזיולוגיות
כדי לזהות ALS, נעשה שימוש ב-TKMS (גירוי מגנטי טרנסגולגולתי), ENG (אלקטרונורוגרפיה), EMG (אלקטרומיוגרפיה).
ניקור מוחי
רמת תכולת החלבון (נורמלית או מוגברת) נקבעת.
בדיקות דם ביוכימיות
בחולים עם ALS נמצאה עלייה של קריאטין פוספוקינאז פי 5 או יותר, הצטברות של קריאטינין ואוריאה ועלייה ב-AST וב-ALT.
ניתוח גנטי מולקולרי
הגן המקודד ל-Superoxide dismutase-1 נחקר.
אך אין די בשיטות הללו כדי לזהות את האבחנה, במקביל בשימוש אבחנה מבדלת כדי לאשר או לשלול מחלות:
- מוֹחַ: אנצפלופתיה לקויה במחזור הדם, גידולים של הפוסה הגולגולת האחורית, ניוון רב מערכתי.
- עמוד שדרה: גידולים, סירינגומיליה, לוקמיה לימפוציטית, אמיוטרופיה בעמוד השדרה וכו'.
- שרירים: דלקת שרירי שריר, מיודיסטרופיה אוקולופארינגאלית, מיוטוניה Rossolimo-Steiner-Kurshman.
- עצבים היקפיים: נוירופתיה מוטורית מולטיפוקל, תסמונת Parsonage-Turner וכו'.
- סינפסה עצבית-שרירית: תסמונת למברט-איטון, מיאסטניה גרביס.
יַחַס
אין תרופה ל-ALS, אך ניתן להאט את התקדמות מחלה זו, להעלות את תוחלת החיים ולהקל על מצבו של אדם.
לשם כך, נעשה שימוש בטיפול מורכב:
התרופה, אשר שימשה לראשונה לטיפול ב-ALS בבריטניה ובארה"ב. חומרים פעילים חוסמים את שחרור הגלוטמין ומאטים את תהליך הנזק הנוירוני. יש ליטול את התרופה 2 פעמים ביום למשך 0.05 גרם.
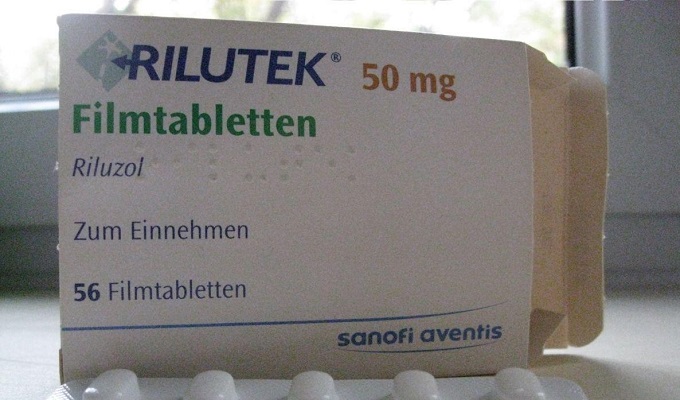
מרפי שרירים ואנטיביוטיקהלעזור עם חולשת שרירים. כדי לחסל התכווצויות שרירים ועוויתות, נקבעים Mydocalm, Baclofen, Sirdalud.
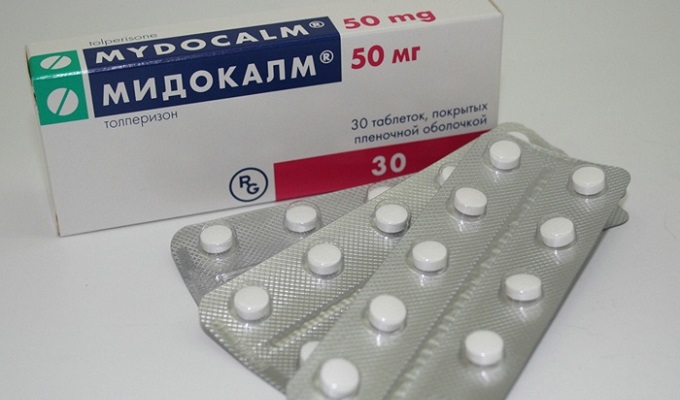

להגדלה מסת שרירמשתמשים ב"רטבולין" אנבוליים.
אנטיביוטיקה אם מתפתח אלח דם או סיבוכים זיהומיים. רופאים רושמים fluoroquinolones, cephalosporins, carbopenes.
ויטמיניםקבוצות B, E, A, C לשיפור הדחף לאורך סיבי העצב.
תרופות אנטיכולינאסטראז, אשר מאטים את תהליך ההרס של אצטילכולין ("Kalimin", "Prozerin", "Pyridostigmine").

במקרים מסוימים משתמשים בו השתלת תאי גזע. הוא מונע מוות של תאי עצב, מקדם את הצמיחה של סיבי עצב ומשקם קשרים עצביים.
בשלבים מאוחרים יותר, השתמש תרופות נוגדות דיכאון ותרופות הרגעה, משככי כאבים לא סטרואידים ואופיאטים.
אם השינה מופרעת, רושמים תכשירי בנזודיאזפינים.
כדי להקל על התנועה, כיסאות ומיטות עם פונקציות שונות, קנים, תיקון צווארונים. רופאים מייעצים לטיפול בדיבור. בשלבים המאוחרים של המחלה, יהיה צורך בפליט רוק ולאחר מכן בטרכאוסטומיה כדי שהחולה יוכל לנשום.
שיטות טיפול לא מסורתיות ב-ALS אינן נותנות תוצאה חיובית.
תחזית והשלכות
פרוגנוזה לחולי ALS שְׁלִילִי. תוצאה קטלנית מתרחשת תוך 2-12 שנים, כמו דלקת ריאות חמורה, כשל נשימתי או אחר מחלה רציניתנגרמת על ידי מחלת גריג.
עם צורת הבולבר ובמטופלים מבוגרים, התקופה מצטמצמת ל-3 שנים.
מְנִיעָה
אמצעים למניעת רפואת ALS עדיין לא ידועים.
המחלה מתקדמת מהר מאוד, אין מקרים של טיפול מוצלח ושיקום התפקודים המוטוריים של הגוף. חולשת שרירים, שמתגברת בהדרגה, משנה לחלוטין את חייו של אדם ומשפחתו.
אבל למרות הפרוגנוזה המאכזבת והמחקר הבלתי מספק של המחלה, יקיריהם צריכים לקוות שטיפולים יעילים יפותחו בעתיד הקרוב. שיטות טיפוליותיַחַס. בינתיים, יש צורך לנקוט באמצעים להקלת מצבו של אדם עם ALS.
טרשת צדדית אמיוטרופית - מחלה מסוכנתשעלול לנטרל אדם ולהוביל למוות.
הרופאים עדיין לא יכולים לקבוע את הגורמים המדויקים למחלה ולמצוא טיפולים יעילים. כרגע, כל מה שהרפואה יכולה לעשות הוא להקל על מצבם של חולי ALS. אף חולה לא הצליח להחלים לחלוטין מהמחלה הזו. חשוב להבחין בין "מחלת ALS" ל"תסמונת ALS". במקרה השני, הפרוגנוזה להתאוששות הרבה יותר טובה.
(ALS), הידועה גם כמחלת לו גריג, היא מחלה ניוונית המתקדמת לאט וחשוכת מרפא של מערכת העצבים המרכזית. לפי מדינת האגודה, רק מחצית מתושבי ארה"ב שמעו על המחלה, אותו דפוס נצפה במדינות אחרות.
דרך אחת למשוך תשומת לב לבעיה של טרשת צדדית אמיוטרופיתהפך לאתגר דלי הקרח, שבו אנשים צריכים לכבות את עצמם בדלי מי קרח ולתרום. באוגוסט 2014, הקמפיין זכה לפופולריות מיוחדת ברחבי העולם, והצליח למשוך תרומות של 50 מיליון דולר ויותר מ-1.5 מיליון משתתפים. נשיא ו מנכ"לחברת 3 M Inge Thulin הצטרפה למספר המשתתפים והתייחסה להשתתפותו בפעולה:
"טרשת צדדית אמיוטרופית(BAS) - מחלה איומה. נעניתי לאתגר ממשפחתו של עובד 3M שלנו, אלן וולגרן, שסובל ממצב זה למעלה מ-32 שנים. הוא אובחן בתחילת השנה, וכיום הוא כבר משותק כמעט לחלוטין. לפני שנה בדיוק, איבדנו גם את אחד המנהיגים הטובים ביותר בעסקי רפואת השיניים של 3M, לארי ליר, שנפטר מ-ALS. ראיתי כמה מהר הוא "נשרף", זה היה נורא. וקיבלתי את האתגר הזה לא רק לכבודם של אלן ולארי, אלא לכבוד כל המשפחות שמתמודדות עם המחלה הנוראה הזו".
גורמים למחלת ALS
הגורם ל-ALS הוא מוטציה של חלבונים מסוימים (אוביקוויטין) עם הופעת אגרגטים תוך תאיים. צורות משפחתיות של המחלה נצפות ב-5% מהמקרים. בעיקרון, מחלת ALS פוגעת באנשים מעל גיל ארבעים ושישים שנה, מתוכם לא יותר מ-10% הם נשאים של הצורה התורשתית, מדענים עדיין לא יכולים להסביר את שאר המקרים בהשפעת כל השפעות חיצוניות- אקולוגיה, פציעות, מחלות וגורמים נוספים.
תסמינים של המחלה
תסמינים מוקדמים של המחלה הם עוויתות, עוויתות, חוסר תחושה וחולשה בגפיים, כמו גם קושי בדיבור, אך סימנים כאלה חלים על מספר רב של מחלות. זה מקשה מאוד על האבחנה עד לתקופה האחרונה, המחלה כבר עוברת לשלב של ניוון שרירים.
נגעי ALS ראשוניים עשויים להופיע ב- חלקים שוניםהגוף, בעוד עד 75% מהחולים, המחלה מתחילה בגפיים, בעיקר התחתונות.
מה זה? איך זה בא לידי ביטוי
ביטויים ראשוניים של המחלה:
חולשה בחלקים הרחוקים של הידיים, סרבול בעת ביצוע תנועות עדינות עם האצבעות, ירידה במשקל בידיים ופסיקולציות (עוויתות שרירים)
פחות שכיח, המחלה מתחילה עם חולשה בזרועות הפרוקסימליות ובחגורת הכתפיים, ניוון בשרירי הרגליים בשילוב עם פרפרזיס ספסטי תחתון
ייתכן גם הופעת המחלה עם הפרעות בולבריות - דיסארטריה ודיספגיה (25% מהמקרים)
התכווצויות (התכווצויות כואבות, התכווצויות שרירים), בדרך כלל כלליות, מתרחשות כמעט בכל החולים עם ALS, ולעתים קרובות הן הסימן הראשון למחלה
מאפיין ביטויים קלינייםבַּס
טרשת צדדית אמיוטרופית מאופיינת בנגע משולב של הנוירון המוטורי התחתון (פריפרי) ונגע של הנוירון המוטורי העליון (מסלולי פיטמיד ו/או תאים פירמידליים של הקורטקס המוטורי של המוח.
סימנים של נזק לנוירון המוטורי התחתון:
- חולשת שרירים (פרזיס)
- היפורפלקסיה (ירידה ברפלקסים)
- ניוון שרירים
- פאסיקולציות (התכווצויות ספונטניות, מהירות, לא קצביות של צרורות של סיבי שריר)
סימנים של נזק לנוירון המוטורי העליון:
- חולשת שרירים (פארזיס).
- ספסטיות (טונוס שרירים מוגבר)
- היפרפלקסיה (רפלקסים מוגברים)
- סימני כף רגל וידיים פתולוגיים
עבור ALS ברוב המקרים אסימטריה של סימפטומים.
בשרירים מנוונים או אפילו שלמים כלפי חוץ, פאסיקולציות(עוויתות שרירים), שעשויות להיות בקבוצת שרירים מקומית או להיות נפוצה.
IN מקרה טיפוסיהופעת המחלה עם ירידה במשקל של השרירים הנרייםאחת הידיים עם התפתחות חולשת אדוקציה (אדדוקציה) והתנגדות של האגודל, (בדרך כלל בצורה א-סימטרית), מה שמקשה על אחיזה עם האגודל אצבעות מורהומוביל להפרות של שליטה מוטורית עדינה בשרירי היד. המטופל חש קושי בעת הרמת חפצים קטנים, בעת הידוק כפתורים, בעת כתיבה.
לאחר מכן, ככל שהמחלה מתקדמת, שרירי האמה מעורבים בתהליך, והיד לובשת מראה של "כפה עם טפרים". כמה חודשים לאחר מכן, מתפתח נגע דומה של היד השנייה. אטרופיה, המתפשטת בהדרגה, לוכדת את שרירי הכתפיים וחגורת הכתפיים.
באותו זמן או מאוחר יותרלעיתים קרובות מתפתחת פגיעה בשרירים הבולבריים: פאסיקולציות וניוון של הלשון, פרזיס של החיך הרך, ניוון של שרירי הגרון והלוע, המתבטא בצורה של דיסארטריה (הפרעות דיבור), דיספאגיה (הפרעות בליעה), הַפרָשָׁת רִיר.
מחקה ו שרירי לעיסהבדרך כלל מושפע מאוחר יותר מקבוצות שרירים אחרות. ככל שהמחלה מתפתחת, זה הופך להיות בלתי אפשרי לבלוט את הלשון, לנפח את הלחיים ולמתוח את השפתיים לצינור.
לפעמים מתפתחת חולשה של פושטי הראשעקב כך החולה אינו יכול לשמור על ראשו ישר.
כאשר מעורב בתהליך של הסרעפתנשימה פרדוקסלית נצפית (בהשראה הבטן שוקעת, בנשיפה היא בולטת).
רגליים בדרך כלל ניוון קודםקבוצות שרירים קדמיות וצדדיות, המתבטאות ב"רגל תלויה" והליכה מסוג צעד (המטופל מרים את רגלו גבוה וזורק אותה קדימה, מוריד אותה בחדות).
באופן אופייני, ניוון שרירים הוא סלקטיבי.
- אטרופיה נצפית על הידיים:
tenara
hypothenar
שרירים בין-רוחביים
שרירי דלתא
- ברגליים מעורבים השרירים המבצעים את כיפוף הגב של כף הרגל.
- בשרירי הבולברי נפגעים שרירי הלשון והחך הרך.
תסמונת פירמידליתמתפתח, ככלל, בשלב מוקדם של ALS ומתבטא בהחייאת רפלקסים בגידים. בעקבות זאת, לעתים קרובות מתפתח paraparesis ספסטי תחתון. בידיים, עלייה ברפלקסים משולבת עם ניוון שרירים, כלומר. יש נגע משולב בו-זמני של המסלולים המרכזיים (הפירמידליים) והנוירון המוטורי ההיקפי, האופייני ל-ALS. רפלקסים שטחיים בבטן נעלמים ככל שהתהליך מתקדם. הסימפטום של בבינסקי (עם גירוי מקווקו של הסוליה, הבוהן הגדולה לא מתכופפת, האצבעות האחרות בצורת מניפה מתפצלות ולא מתכופפות) נצפה במחצית ממקרי המחלה.
ייתכנו הפרעות חושיות. ב-10% מהחולים נצפות פרסטזיה בחלקים הרחוקים של הידיים והרגליים. כאב, לעיתים חמור, לרוב לילי, עלול להיות קשור לנוקשות מפרקים, חוסר תנועה ממושך, עוויתות עקב ספסטיות גבוהה, עם התכווצויות (עוויתות שרירים כואבות), דיכאון. אובדן רגישות אינו אופייני.
הפרעות אוקולומוטוריותאינם אופייניים ומתרחשים בשלבים סופניים של המחלה.
תפקוד לקוי של איברי האגן אינו אופייני, אך בשלבים מתקדמים עלולה להתרחש אצירת שתן או בריחת שתן.
ליקוי קוגניטיבי בינוני(ירידה בזיכרון ובביצועים הנפשיים) באים לידי ביטוי במחצית מהמטופלים. ב-5% מהחולים מתפתח סוג פרונטלי, שניתן לשלבו עם פרקינסוניזם.
תכונה של ALS היא היעדר פצעי שינה אפילו בחולים מרותקים למיטה.
היכן שהם מופיעים סימנים ראשונים של ALS, חולשת שרירים מועברת בהדרגה לחלקים גדולים יותר של הגוף, אם כי עם הצורה הבולברית של ALS, חולים עשויים שלא לשרוד עד להשלמת פרזיס של הגפיים, עקב עצירת נשימה.
עם הזמן, המטופל מאבד את היכולת לנוע באופן עצמאי. מחלת ALSאינו משפיע על התפתחות נפשית, אולם, לרוב, הוא מתחיל דיכאון עמוקהאדם מחכה למוות. בשלבים האחרונים של המחלה נפגעים גם השרירים המבצעים את פעולת הנשימה, ויש לתמוך בחיי החולים על ידי אוורור מלאכותי של הריאות תזונה מלאכותית. זה לוקח 3-5 שנים מהתבוננות בסימנים הראשונים של ALS ועד למוות. עם זאת, מקרים ידועים באופן נרחב כאשר מצבם של חולים עם מחלת ALS מוכרת באופן חד משמעי התייצב לאורך זמן.
למי יש ALS?
יש יותר מ-350,000 חולי ALS בעולם.
ALS מאובחנת ב-5-7 אנשים בשנה לכל 100,000 אוכלוסייה. יותר מ-5,600 אמריקאים מאובחנים עם ALS מדי שנה. זה 15 מקרים חדשים של בס ליום
ALS יכולה להשפיע על כל אחד. שיעור ההיארעות (מספר החדשים) ALS - 100,000 איש בשנה
פחות מ-10% ממקרי ה-ALS הם תורשתיים. ALS יכולה להשפיע על גברים ונשים כאחד. ALS משפיעה על כל הקבוצות האתניות והחברתיות-כלכליות
ALS יכולה להשפיע על מבוגרים צעירים או מבוגרים מאוד, אך לרוב מאובחנת בבגרות האמצעית והמאוחרת.
אנשים עם ALS דורשים ציוד יקר, טיפול וטיפול מתמיד 24/7
90% מנטל הטיפול נופל על כתפיהם של בני משפחה של חולי ALS. ALS מוביל בסופו של דבר לחולשה של הגוף, הרגשי והגוף משאבים פיננסייםישנם יותר מ-8,500 חולי ALS ברוסיה ויותר מ-600 חולי ALS במוסקבה, אם כי מספר זה זוכה להערכה מתמדת באופן רשמי. הרוסים המפורסמים ביותר עם ALS הם דמיטרי שוסטקוביץ', ולדימיר מיגוליה.
הגורמים למחלה אינם ידועים. אין תרופה ל-ALS. חלה האטה במהלך המחלה. הארכת חיים אפשרית בעזרת מכשיר הנשמה ביתי.
תסמונות שאינן ניתנות להבחנה קלינית מ-ALS קלאסי עשויות לנבוע מ:
נגעים מבניים:
גידולים פרסאגיטליים
גידולי מגנום פורמן
ספונדילוזיס צוואר הרחםעַמוּד הַשִׁדרָה
תסמונת ארנולד-קיארי
הידרומיאליה
אנומליה arteriovenous של חוט השדרה
זיהומים:
חיידקי - טטנוס, מחלת ליים
ויראלי - פוליומיאליטיס, שלבקת חוגרת
מיאלופתיה רטרו-ויראלית
שיכרון, חומרים פיזיים:
רעלים - עופרת, אלומיניום, מתכות אחרות.
תרופות - סטריכנין, פניטואין
התחשמלות
צילומי רנטגן
מנגנונים אימונולוגיים:
דיסקרזיה של פלסמוציטים
polyradiculoneuropathy אוטואימונית
תהליכים פאראנופלסטיים:
פרקרצינומטי
פרלימפומטי
הפרעות מטבוליות:
היפוגליקמיה
היפרפאראתירואידיזם
תירוטוקסיקוזיס
מחסור בחומצה פולית,
ויטמינים B12, E
חוסר ספיגה
הפרעות ביוכימיות תורשתיות:
פגם בקולטן אנדרוגן - מחלת קנדי
מחסור בהקסוזמינידאז
מחסור ב-a-glucosidase - מחלת פומפה
היפרליפידמיה
היפרגליקינוריה
methylcrotonylglycinuria
כל המצבים הללו יכולים לגרום לתסמינים הנראים ב-ALS ויש לקחת בחשבון באבחנה המבדלת.
אין טיפול יעיל למחלה. התרופה היחידה, מעכב שחרור הגלוטמט רילוזול (Rilutek), מעכבת את המוות ב-2 עד 4 חודשים. הוא רושם 50 מ"ג פעמיים ביום.
טיפול במחלת ALS
בסיס הטיפול הוא טיפול סימפטומטי:
- פִיסִיוֹתֶרָפִּיָה.
פעילות גופנית. המטופל צריך, במידת האפשר, לשמור פעילות גופניתככל שהמחלה מתקדמת, יש צורך בכיסא גלגלים ובמכשירים מיוחדים נוספים.
.דִיאֵטָה. דיספאגיה יוצרת סכנה של כניסת מזון לדרכי הנשימה. לפעמים יש צורך במזון דרך צינורית או בגסטרוסטומיה.
- שימוש במכשירים אורטופדיים: צווארון צווארי, סדים שונים, מכשירים לאחיזה בחפצים.
עם התכווצויות (כואבות התכווצות שרירים): כינין סולפט 200 מ"ג פעמיים ביום, או פניטואין (דיפנין) 200-300 מ"ג ליום, או קרבמזפין (פינלפסין, טגרטול,) 200-400 מ"ג ליום, ו/או ויטמין E 400 מ"ג פעמיים ביום, גם כן. כמו תכשירי מגנזיום, ורפמיל (Isoptin).
כאשר ספסטיות: בקלופן (Baclosan) 10 - 80 מ"ג ליום, או טיזאנידין (Sirdalud) 6 - 24 מ"ג ליום, כמו גם קלונאזפאם 1 - 4 מ"ג ליום, או ממנטין 10 - 60 מ"ג ליום.
- עבור ריור, אטרופין 0.25 - 0.75 מ"ג שלוש פעמים ביום, או Hyoscine (Buscopan) 10 מ"ג שלוש פעמים ביום.
אם אי אפשר לאכול בגלל הפרה של בליעה, מבצעים גסטרוסטומיה או מחדירים צינור אף. גסטרוסטומיה אנדוסקופית מלעורית מוקדמת מאריכה את חיי החולים ב-6 חודשים בממוצע.
- בְּ תסמונות כאבלהשתמש בכל הארסנל של משככי כאבים. כולל משככי כאבים נרקוטיים בשלבים האחרונים.
- לפעמים מביאים שיפור זמני כלשהו על ידי תרופות אנטיכולינאסטראז (ניאוסטיגמין מתיל סולפט - פרוזרין).
Cerebrolysin במינונים גבוהים (10-30 מ"ל טפטוף IV למשך 10 ימים בקורסים חוזרים). ישנם מספר מחקרים קטנים המראים את היעילות הנוירו-פרוטקטיבית של סרברוליזין ב-ALS.
תרופות נוגדות דיכאון: סרטלין 50 מ"ג ליום או פקסיל 20 מ"ג ליום או אמיטריפטילין 75-150 מ"ג ליום תופעות לוואי- זה גורם ליובש בפה, ולכן מפחית ריר יתר (ריור), אשר לעתים קרובות מייסר חולי ALS).
במקרה של הפרעות בדרכי הנשימה: אוורור מלאכותיריאות בבית חולים, ככלל, לא מתבצע, אבל חלק מהחולים רוכשים מאווררים ניידים ומבצעים אוורור מכני בבית.
- נערכים פיתוחים לשימוש בהורמון גדילה, גורמים נוירוטרופיים ב-ALS.
- לאחרונה, הפיתוח של טיפול בתאי גזע נערך באופן פעיל. שיטה זו מבטיחה להיות מבטיחה, אבל היא עדיין בשלב של ניסויים מדעיים.
תרופותתרופות שעוזרות להאט את מחלת ה-ALS:
הרפואה המודרנית מתפתחת כל הזמן. מדענים יוצרים תרופות חדשות למחלות חשוכות מרפא בעבר. עם זאת, כיום מומחים אינם יכולים להציע טיפול הולם כנגד כל המחלות. אחת הפתולוגיות הללו היא מחלת ALS. הגורמים למחלה זו עדיין לא נחקרו, ומספר החולים רק גדל מדי שנה. במאמר זה, נסתכל מקרוב על פתולוגיה זו, הסימפטומים העיקריים שלה ושיטות הטיפול.
מידע כללי
טרשת צדדית אמיוטרופית (ALS, מחלת שארקוט) היא פתולוגיה רצינית של מערכת העצבים, שבה יש נזק למה שנקרא נוירונים מוטוריים בחוט השדרה, כמו גם בקליפת המוח. זוהי מחלה כרונית וחשוכת מרפא, המובילה בהדרגה לניוון של מערכת העצבים כולה. בשלבים האחרונים של המחלה, אדם הופך חסר אונים, אך יחד עם זאת הוא שומר על בהירות נפשית ובריאות נפשית.
מחלת ALS, שהסיבות והפתוגנזה שלה לא נחקרו במלואן, אינה שונה בשיטות ספציפיות לאבחון וטיפול. מדענים ממשיכים לחקור אותו באופן פעיל היום. כעת ידוע בוודאות שהמחלה מתפתחת בעיקר אצל אנשים בגילאי 50 עד כ-70 שנים, אך ישנם מקרים של נגעים מוקדמים יותר.
מִיוּן
בהתאם לוקליזציה של הביטויים העיקריים של המחלה, מומחים מבחינים בין הצורות הבאות:
- צורה Lumbosacral (יש הפרה של התפקוד המוטורי של הגפיים התחתונות).
- צורה בולברית (חלק מהגרעינים של המוח מושפעים, מה שגורר אופי).
- צורה צוואר הרחם ( תסמינים ראשונייםמתבטא בשינויים בתפקוד המוטורי הרגיל גפיים עליונות).
מצד שני, מומחים מבחינים בעוד שלושה סוגים של מחלת ALS:
מדוע מתרחשת ALS?
גורם ל המחלה הזולמרבה הצער עדיין לא מובן. מדענים מזהים כיום מספר גורמים, בנוכחותם הסבירות לחלות עולה פי כמה:
מחלת ALS. תסמינים
ניתן לראות תמונות של חולים במחלה זו בספרי עיון מיוחדים. לכולם יש רק דבר אחד במשותף - תסמינים חיצונייםמחלה בשלבים מאוחרים יותר.
לגבי ראשוני סימנים קלינייםפתולוגיות, לעתים נדירות מאוד הן גורמות לעירנות מצד החולים. יתרה מכך, מטופלים פוטנציאליים מסבירים אותם לרוב במתח מתמיד או בחוסר מנוחה משגרת העבודה. להלן תסמיני המחלה המופיעים בשלבים הראשונים:
- חולשת שרירים;
- dysarthria (קושי בדיבור);
- התכווצויות שרירים תכופות;
- חוסר תחושה וחולשה של הגפיים;
- עוויתות שרירים קלות.
כל הסימנים הללו צריכים להזהיר את כולם ולהפוך לסיבה לפנות למומחה. אחרת, המחלה תתקדם, מה שמגדיל מספר פעמים את הסבירות לסיבוכים.
מהלך המחלה
איך ALS מתפתחת? המחלה שתסמיניה פורטו לעיל מתחילה בהתחלה חולשת שריריםוחוסר תחושה של הגפיים. אם הפתולוגיה מתפתחת מהרגליים, אז החולים עלולים לחוות קושי בהליכה, למעוד כל הזמן.
אם המחלה מתבטאת בהפרה של הגפיים העליונות, יש בעיות בביצוע המשימות הבסיסיות ביותר (כפתור חולצה, סיבוב המפתח במנעול). 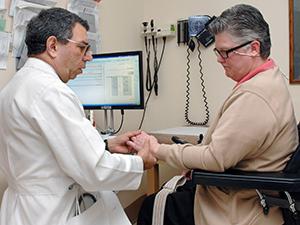
איך עוד ניתן לזהות ALS? הגורמים למחלה ב-25% מהמקרים נעוצים בנגע medulla oblongata. בתחילה, יש קשיים בדיבור, ולאחר מכן בבליעה. כל זה כרוך בבעיות בלעיסת מזון. כתוצאה מכך, אדם מפסיק לאכול כרגיל ויורד במשקל. כתוצאה מכך, חולים רבים נופלים לתוך דִכָּאוֹן, שכן המחלה בדרך כלל אינה משפיעה
חלק מהמטופלים מתקשים ביצירת מילים ואף בריכוז תקין. הפרות קלות מסוג זה מוסברות לרוב על ידי נשימה לקויה בלילה. עובדים רפואייםכבר עכשיו עליהם לספר לחולה על תכונות מהלך המחלה, אפשרויות הטיפול, כדי שיוכל לקבל החלטה מושכלת לגבי עתידו מראש.
רוב החולים מתים כשל נשימתיאו דלקת ריאות. ככלל, מוות מתרחש תוך חמש שנים ממועד אישור המחלה.
אבחון
רק מומחה יכול לאשר את נוכחותה של מחלה זו. בעניין זה, התפקיד העיקרי ניתן לפרשנות מוסמכת של הקיים תמונה קליניתבמטופל מסוים. האבחנה המבדלת של מחלת ALS היא חשובה ביותר.
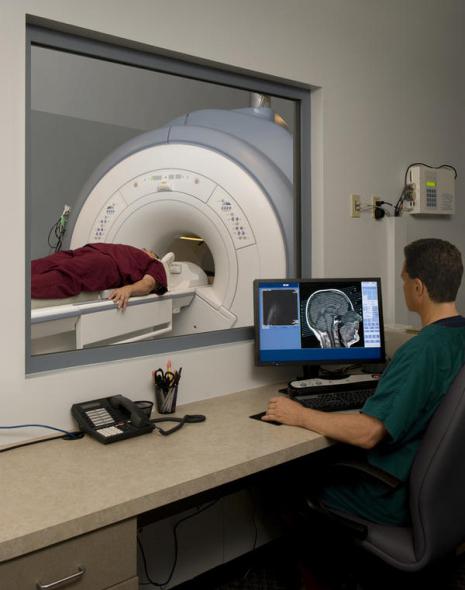
מה צריך להיות הטיפול?
למרבה הצער, הרפואה כיום אינה יכולה להציע טיפול יעיל נגד מחלה זו. כיצד ניתן לרפא ALS? הטיפול צריך להיות מכוון בעיקר להאטת מהלך הפתולוגיה. למטרות אלה, נעשה שימוש באמצעים הבאים:

טיפול בתאי גזע
במדינות רבות באירופה, חולי ALS מטופלים כעת בתאי גזע משלהם, מה שגם מאט את התקדמות המחלה. סוג זה של טיפול נועד לשפר את התפקודים העיקריים של המוח. מושתלים באזור הנזק, משחזרים נוירונים, משפרים את אספקת החמצן למוח ומקדמים את המראה של כלי דם חדשים.
בידוד תאי הגזע עצמם והשתלתם הישירה, ככלל, מתבצעים על בסיס אשפוז. לאחר הטיפול, המטופל נשאר בבית החולים למשך יומיים נוספים, שם מומחים עוקבים אחר מצבו. 
במהלך ההליך עצמו, תאים מוזרקים לתוכם נוזל מוחיאסור להם להתרבות בעצמם באמצעות מחוץ לגוף, והשתלה מחדש מתבצעת רק לאחר ניקוי מפורט.
חשוב לציין שסוג זה של טיפול יכול להאט משמעותית את מחלת ה-ALS. תמונות של מטופלים 5-6 חודשים לאחר ההליך מוכיחות בבירור הצהרה זו. זה לא יעזור להיפטר מהמחלה לחלוטין. למרבה הצער, ישנם גם מקרים בהם הטיפול אינו נותן השפעה כלל.
סיכום
הפרוגנוזה של מחלה זו היא כמעט תמיד שלילי. הִתקַדְמוּת הפרעות תנועהכרוך בהכרח (2-6 שנים).
במאמר זה, דיברנו על מה מהווה פתולוגיה כזו כמו ALS. מחלה שתסמיניה עשויים שלא להופיע במשך זמן רב, כיום בלתי אפשרי לרפא לחלוטין. מדענים ברחבי העולם ממשיכים לחקור באופן פעיל מחלה זו, הסיבות שלה ומהירות התפתחותה, בניסיון למצוא תרופה יעילה.


